已知可逆反应:AsO +2I-+2H+
+2I-+2H+ AsO
AsO +I2+H2O。
+I2+H2O。
(Ⅰ)如图所示,若向B中逐滴加入浓盐酸,发现电流表指针偏转。
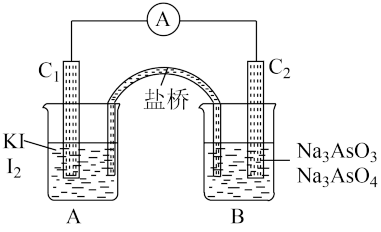
(Ⅱ)若改为向B中滴加40%的NaOH溶液,发现电流表指针与(Ⅰ)中偏转方向相反。
试回答问题:
(1)两次操作中电流表指针为什么会发生偏转?_______ 。
(2)两次操作过程中电流表指针偏转方向为什么相反?_______ 。
(3)操作(Ⅰ)中,C1棒上的反应为_______ 。
(4)操作(Ⅱ)中,C2棒上的反应为_______ 。
 +2I-+2H+
+2I-+2H+ AsO
AsO +I2+H2O。
+I2+H2O。(Ⅰ)如图所示,若向B中逐滴加入浓盐酸,发现电流表指针偏转。

(Ⅱ)若改为向B中滴加40%的NaOH溶液,发现电流表指针与(Ⅰ)中偏转方向相反。
试回答问题:
(1)两次操作中电流表指针为什么会发生偏转?
(2)两次操作过程中电流表指针偏转方向为什么相反?
(3)操作(Ⅰ)中,C1棒上的反应为
(4)操作(Ⅱ)中,C2棒上的反应为
21-22高二下·云南楚雄·阶段练习 查看更多[2]
云南省楚雄彝族自治州民族中学2021-2022学年高二下学期3月月考化学试题(已下线)4.1.1 原电池的工作原理-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
更新时间:2022-03-31 09:16:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.判断:
(1)下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
Ⅱ.常温下,将除去表面氧化膜的Al、Cu片插入浓 中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。
中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。

(2)O~t1时,原电池的负极是Al片,此时,正极的电极反应式是_______ ,溶液中的 向
向_______ 移动(填“正极”或“负极”);t1时,原电池中电子流动方向发生改变,其原因是_______ 。
(1)下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A. | B. |
C.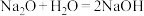 | D. |
Ⅱ.常温下,将除去表面氧化膜的Al、Cu片插入浓
 中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。
中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。
(2)O~t1时,原电池的负极是Al片,此时,正极的电极反应式是
 向
向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池.请你利用下列反应“Cu + 2Ag+ = 2Ag + Cu2+”设计一个化学电池:
①画出合理的原电池装置图_____________________________ (标明正负极、电极材料和电解质溶液)
②正极质量_____ (填“增加”、“减少”或“不变”,下同),负极质量______
(2)甲烷燃料电池的工作原理如图所示.
①该电池工作时,b口通入的物质为______ ,c口通入的物质为______ ;
②该电池负极的电极反应式为:_____________________________ ;
③工作一段时间后,当3.2g甲烷完全反应生成CO2时,有_______ 个电子转移。
①画出合理的原电池装置图
②正极质量
(2)甲烷燃料电池的工作原理如图所示.

①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为:
③工作一段时间后,当3.2g甲烷完全反应生成CO2时,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
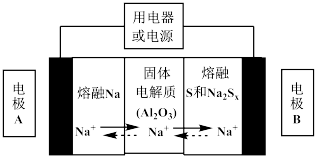
①根据上右表数据,请你判断该电池工作的适宜应控制在_________ (填字母)范围内。
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为_________ 极,电极B发生_________ 反应(填“氧化或还原”)
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:________________ 。
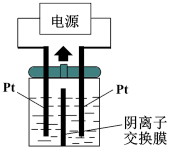
(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:___________ ;试分析左侧溶液蓝色逐渐变浅的可能原因是:___________ 。
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:
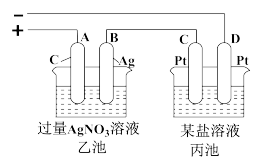
当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加__________ g;此时丙装置中___________ (填“C”或“D”)电极析出7.20g金属,则丙装置中的某盐溶液可能是_______ (填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:

①根据上右表数据,请你判断该电池工作的适宜应控制在
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:

(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:

当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1) 辅助的
辅助的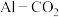 电池工作原理如图所示,该电池容量大,能有效利用
电池工作原理如图所示,该电池容量大,能有效利用 ,电池反应产物
,电池反应产物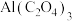 是重要的化工原料,电池的正极反应式为
是重要的化工原料,电池的正极反应式为_______ ,反应过程中 的作用是
的作用是_______ 。

(2)一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇-氧化钠,其中 可以在固体介质NASICON中自由移动,传感器中通过的电流越大,尾气中一氧化碳的含量越高。
可以在固体介质NASICON中自由移动,传感器中通过的电流越大,尾气中一氧化碳的含量越高。

则a极的电极反应式为_______ ,工作时 由电极
由电极_______ (填“a”或“b”,下同)向电极_______ 移动。
(3)减排是各个国家都在努力为之的事, 和
和 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将 、
、 转化为重要的化工原料。
转化为重要的化工原料。
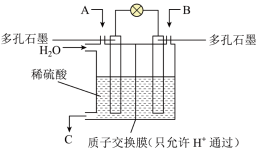
①若A为 ,B为
,B为 ,C为
,C为 ,电池总反应为
,电池总反应为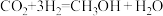 ,则正极的电极反应式为
,则正极的电极反应式为_______ 。
②若A为 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为_______ 。
(1)
 辅助的
辅助的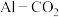 电池工作原理如图所示,该电池容量大,能有效利用
电池工作原理如图所示,该电池容量大,能有效利用 ,电池反应产物
,电池反应产物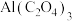 是重要的化工原料,电池的正极反应式为
是重要的化工原料,电池的正极反应式为 的作用是
的作用是
(2)一种一氧化碳分析仪的工作原理如图所示,该装置中电解质为氧化钇-氧化钠,其中
 可以在固体介质NASICON中自由移动,传感器中通过的电流越大,尾气中一氧化碳的含量越高。
可以在固体介质NASICON中自由移动,传感器中通过的电流越大,尾气中一氧化碳的含量越高。
则a极的电极反应式为
 由电极
由电极(3)减排是各个国家都在努力为之的事,
 和
和 的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将
的处理是许多科学家都在着力研究的重点。有学者想以如图所示装置利用原电池原理将 、
、 转化为重要的化工原料。
转化为重要的化工原料。
①若A为
 ,B为
,B为 ,C为
,C为 ,电池总反应为
,电池总反应为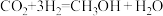 ,则正极的电极反应式为
,则正极的电极反应式为②若A为
 ,B为
,B为 ,C为
,C为 ,则负极的电极反应式为
,则负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸。工作时该电池总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O,据此判断:
①铅蓄电池的负极材料是___________ 。
②工作时,电解质溶液的酸性___________ (填“增大”、“减小”或“不变”)。
③工作时,电解质溶液中阳离子移向___________ 极。
①铅蓄电池的负极材料是
②工作时,电解质溶液的酸性
③工作时,电解质溶液中阳离子移向
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A._____ ,B._____ 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是____________ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲________ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的负极电极反应式_________________________ 。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入__ 极(填a或b),电子从____ (填a或b)极流出。
(1)现有如下两个反应:
A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑
判断能否设计成原电池A.
(2)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,氢气为燃料,采用氢氧化钠溶液为电解液;则氢气应通入
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
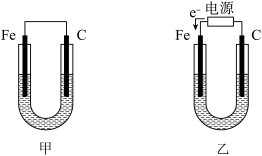
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________ 腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________ ;
②甲池铁棒腐蚀的速率比乙池铁棒_____ (填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________ ;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。

(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生
②甲池铁棒腐蚀的速率比乙池铁棒
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化形式主要是___________ ,在导线中电子流动方向为_____ (用a、b 和箭头表示)。
(2)负极反应式为______________________________________ 。
(3)电极表面镀铂粉的原因为____________________________________________________ 。
(4)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

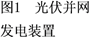

① 图1中N型半导体为________ (填“正极”或“负极”)
② 该系统工作时,A极的电极反应式为____________________ 。
③ 若A极产生7.00g N2,则此时B极产生________ L H2(标准状况下)。

(1)氢氧燃料电池的能量转化形式主要是
(2)负极反应式为
(3)电极表面镀铂粉的原因为
(4)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

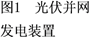

① 图1中N型半导体为
② 该系统工作时,A极的电极反应式为
③ 若A极产生7.00g N2,则此时B极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求对图中两极进行必要的连接 并填空:
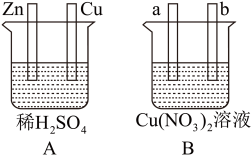
(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫____ 。电极反应式:锌板:____ ;铜板:_____ 。
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫____ 。电极反应式,a极:____ ;b极:_____ 。经过一段时间后,停止反应,溶液的pH值____ (升高、降低、不变),加入一定量的____ 后,溶液能恢复至与电解前完全一致。

(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫
您最近一年使用:0次



