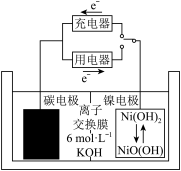
按要求对图中两极进行必要的连接 并填空:
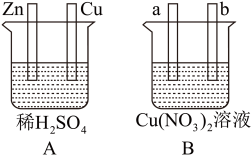
(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫____ 。电极反应式:锌板:____ ;铜板:_____ 。
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫____ 。电极反应式,a极:____ ;b极:_____ 。经过一段时间后,停止反应,溶液的pH值____ (升高、降低、不变),加入一定量的____ 后,溶液能恢复至与电解前完全一致。

(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫
更新时间:2020-02-12 09:52:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流表。原电池工作时电子是从_____ 到______ (填锌片或银片),锌片电极上发生的是_______________ 反应(“氧化”或“还原”)。电极反应式为_________________________________ ,锌片上观察到的现象为___________
(2)银片上发生的是____________ 反应(“氧化”或“还原”),电极反应式是__________ ,银片上观察到的现象是______________________ 溶液中的C(H+)____________ (填“增大”或“减小”)。
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为________ L(标准状况);导线中通过的电子数为______ 。
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以__________ (写名称)为电解质溶液,铁为______ 极,电极反应式为_______ ,
(2)在该原电池中,选__________ (写名称)作正极,电极反应式是__________________________
(3)画出装置图,标出正、负极材料及电解质溶液名称____________________ 。
(2)银片上发生的是
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以
(2)在该原电池中,选
(3)画出装置图,标出正、负极材料及电解质溶液名称
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】目前,液流电池是电化学储能领域的一个研究热点,优点是储能容量大、使用寿命长。一种简单钒液流电池的电解液存储在储液罐中,放电时的结构及工作原理如图:
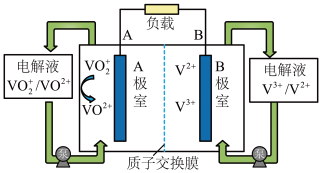
回答下列问题:
(1)放电时,导线中电流方向为_______ ,质子通过质子交换膜方向为_______ (填“从A到B”或“从B到A”)。
(2)用该电池作为电源电解饱和食盐水,电解反应的化学方程式为_______ ;若欲利用电解所得产物制取含149kgNaClO的消毒液用于环境消毒,理论上电解过程中至少需通过电路_____ mol电子。
(3)若将该电池电极连接电源充电,则A极连接电源的___ 极,发生的电极反应为______ 。

回答下列问题:
(1)放电时,导线中电流方向为
(2)用该电池作为电源电解饱和食盐水,电解反应的化学方程式为
(3)若将该电池电极连接电源充电,则A极连接电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】锌银电池比能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器。电解质溶液是KOH溶液,电池总反应为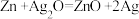 。请回答下列问题:
。请回答下列问题:
(1)该电池的正极材料是___________ ;电池工作时,阳离子向___________ (填“正极”或“负极”)移动;负极的反应式为___________ 。
(2)①电极材料锌可由闪锌矿在空气中煅烧成氧化锌,然后用碳还原来制取,化学反应方程式为 ,此法为
,此法为___________ 。
A.电解法
B.热还原法
C.热分解法
②电极材料氧化银可回收利用得到银,其化学方程式为___________ 。
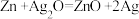 。请回答下列问题:
。请回答下列问题:(1)该电池的正极材料是
(2)①电极材料锌可由闪锌矿在空气中煅烧成氧化锌,然后用碳还原来制取,化学反应方程式为
 ,此法为
,此法为A.电解法
B.热还原法
C.热分解法
②电极材料氧化银可回收利用得到银,其化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】锌—空气燃料电池具有携带方便、成本低及安全无污染等优点,在汽车电源等领域有广阔的应用前景,其工作原理如图所示。采用锌—空气燃料电池作为电源,用离子交换膜控制溶液中氢氧根浓度制备具有高催化性能的纳米 。
。
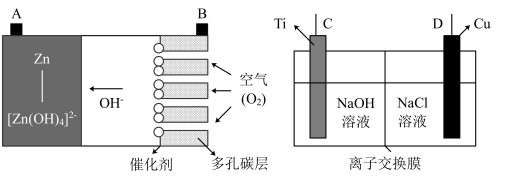
请回答下列问题:
(1)锌—空气燃料电池中多孔碳层具有较大的表面积,有利于_______ 。
(2)锌—空气燃料电池中负极的电极反应式为_______ 。
(3)锌—空气燃料电池作为电源制备纳米 时,B电极应与电极相连
时,B电极应与电极相连_______ (填“C”或“D”)。
(4)理论上,当 空气(标准状况下)通入B电极后,可制备纳米
空气(标准状况下)通入B电极后,可制备纳米 的质量为
的质量为_______ g。
(5)炼锌的方法之一为 ,在恒温的真空密闭反应器中发生反应,此时该反应的化学平衡常数为
,在恒温的真空密闭反应器中发生反应,此时该反应的化学平衡常数为 (
( 为分压表示的平衡常数),平衡后将部分锌蒸汽移走,再次达到平衡时,反应器内压强为
为分压表示的平衡常数),平衡后将部分锌蒸汽移走,再次达到平衡时,反应器内压强为_______  。
。
 。
。
请回答下列问题:
(1)锌—空气燃料电池中多孔碳层具有较大的表面积,有利于
(2)锌—空气燃料电池中负极的电极反应式为
(3)锌—空气燃料电池作为电源制备纳米
 时,B电极应与电极相连
时,B电极应与电极相连(4)理论上,当
 空气(标准状况下)通入B电极后,可制备纳米
空气(标准状况下)通入B电极后,可制备纳米 的质量为
的质量为(5)炼锌的方法之一为
 ,在恒温的真空密闭反应器中发生反应,此时该反应的化学平衡常数为
,在恒温的真空密闭反应器中发生反应,此时该反应的化学平衡常数为 (
( 为分压表示的平衡常数),平衡后将部分锌蒸汽移走,再次达到平衡时,反应器内压强为
为分压表示的平衡常数),平衡后将部分锌蒸汽移走,再次达到平衡时,反应器内压强为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现所期待的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率。
(1)控制条件,让反应在恒容密闭穼器中进行反应: 。用传感器测得不同时间
。用传感器测得不同时间 和
和 的浓度如表。
的浓度如表。
前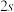 内的平均反应速率
内的平均反应速率
___________ ,从表格看,已达化学平衡的时间段为___________ s;
(2)在一定温度下,某固定容积的密闭容器中充入一定量的 气体后,发生反应
气体后,发生反应 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。如图所示是反应速率(
是无色气体。如图所示是反应速率(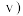 与时间
与时间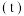 的关系曲线。下列叙述正确的是
的关系曲线。下列叙述正确的是___________ ;

a. 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小
b. 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行
c. 各物质浓度不再变化
各物质浓度不再变化
d. 各物质浓度相等
各物质浓度相等
e.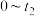 ,
, 浓度增大
浓度增大
f.反应过程中气体的颜色不变
(3)使用 时也要注意防止污染环境。电化学气敏传感器可用于监测环境中
时也要注意防止污染环境。电化学气敏传感器可用于监测环境中 的含量,其工作原理如图:
的含量,其工作原理如图:

①Pt电极(b)上的电极反应式为___________ ;
②电池总反应的化学反应方程式为___________ ,反应一段时间后, 溶液的浓度将
溶液的浓度将___________ (填“增大”“减小”或“不变”)。
(1)控制条件,让反应在恒容密闭穼器中进行反应:
 。用传感器测得不同时间
。用传感器测得不同时间 和
和 的浓度如表。
的浓度如表。时间 | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
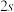 内的平均反应速率
内的平均反应速率
(2)在一定温度下,某固定容积的密闭容器中充入一定量的
 气体后,发生反应
气体后,发生反应 ,已知
,已知 是红棕色气体,
是红棕色气体, 是无色气体。如图所示是反应速率(
是无色气体。如图所示是反应速率(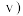 与时间
与时间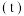 的关系曲线。下列叙述正确的是
的关系曲线。下列叙述正确的是
a.
 时,反应未达到平衡,
时,反应未达到平衡, 浓度在减小
浓度在减小b.
 时,反应达到平衡,反应不再进行
时,反应达到平衡,反应不再进行c.
 各物质浓度不再变化
各物质浓度不再变化d.
 各物质浓度相等
各物质浓度相等e.
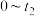 ,
, 浓度增大
浓度增大f.反应过程中气体的颜色不变
(3)使用
 时也要注意防止污染环境。电化学气敏传感器可用于监测环境中
时也要注意防止污染环境。电化学气敏传感器可用于监测环境中 的含量,其工作原理如图:
的含量,其工作原理如图:
①Pt电极(b)上的电极反应式为
②电池总反应的化学反应方程式为
 溶液的浓度将
溶液的浓度将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为___________ ,该电池总反应的离子方程式为______________ 。
(2)尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为____ 。可将该反应设计成碱性燃料电池除去烟气中的氮氧化物,该燃料电池负极的电极反应式是______________ ,正极的电极反应式是__________________ 。
(2)尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】图中的A为直流电源,B为渗透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色。请填空:

(1)电源A中a点为________ 极。
(2)滤纸B上发生氧化反应的电极反应方程式为:____________________ 。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路:
①电极e上发生的反应为:__________________ ;
②在此过程中电解液的浓度(填“始终不变”、“略微增大”、“略微减小”)___________ ;
③电镀槽中盛放的电镀液可以是________ 或________ (只要求填两种电解质溶液)。

(1)电源A中a点为
(2)滤纸B上发生氧化反应的电极反应方程式为:
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路:
①电极e上发生的反应为:
②在此过程中电解液的浓度(填“始终不变”、“略微增大”、“略微减小”)
③电镀槽中盛放的电镀液可以是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。

①Y中总反应的化学方程式为___ ,滤纸上c点附近会变___ 色。
②电解一段时间后,Z产生280mL的气体(标准状况下),此时Z中溶液的体积为500mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是___ ,需加入___ g的__ (填化学式)可使溶液复原。
(2)用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图甲所示,电解过程中的实验数据如图乙所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

①OQ段电解过程中生成O2的物质的量是___ 。
②下列说法不正确的是___ (填字母)。
A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的电极反应式为4OH--4e-=2H2O+O2↑
C.OP段表示H2和O2混合气体的体积变化
D.从P点到Q点时收集到的气体为H2和O2
(1)图中X为电源,Y为浸透滴有酚酞试液的饱和食盐水的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。

①Y中总反应的化学方程式为
②电解一段时间后,Z产生280mL的气体(标准状况下),此时Z中溶液的体积为500mL,假设溶液中还有AgNO3存在,则溶液中氢离子的物质的量是
(2)用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图甲所示,电解过程中的实验数据如图乙所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。

①OQ段电解过程中生成O2的物质的量是
②下列说法不正确的是
A.电解过程中,a电极表面先有红色物质析出,后有气泡产生
B.b电极上发生的电极反应式为4OH--4e-=2H2O+O2↑
C.OP段表示H2和O2混合气体的体积变化
D.从P点到Q点时收集到的气体为H2和O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)以甲烷、氧气为原料,KOH溶液作为电解质构成燃料电池,总反应式为____ ,如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为:____ ;如果电解一段时间后NaCl溶液的体积为1L,溶液中的OH﹣物质的量浓度为0.01mol•L﹣1(25℃下测定),则理论上消耗氧气的体积为____ mL(标况下)。
(2)用铂电极电解CuSO4溶液,当C(Cu2+)降至原来的一半时停止通电,则加入下列物质中的__ (填序号)物质能使溶液恢复成原来浓度;
A.CuO B.Cu(OH)2 C.Cu D.H2O
电解后电解质溶液的pH值__ (填“增大”“减小”或“不变”);写出电解总离子方程式____ 。
(3)用Pt作电极电解硝酸银溶液,如图甲所示,则左边Pt电极名称是__ ;发生的电极反应式为__ 。

(2)用铂电极电解CuSO4溶液,当C(Cu2+)降至原来的一半时停止通电,则加入下列物质中的
A.CuO B.Cu(OH)2 C.Cu D.H2O
电解后电解质溶液的pH值
(3)用Pt作电极电解硝酸银溶液,如图甲所示,则左边Pt电极名称是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
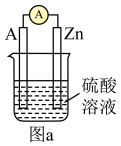
【推荐1】电化学在生活中的应用广泛,请根据电化学原理回答下列问题。
(1)图a中,电流表指针发生偏转,Zn作负极,则A电极上发生的电极反应式为___________ ;反应进行一段时间后溶液酸性将___________ (填“增强”或“减弱”或“基本不变”)。
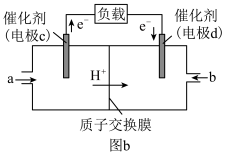
(2)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池的结构示意图如图b,电池总反应为 ,则d电极是
,则d电极是___________ (填“正极”或“负极”),c电极的电极反应式为___________ 。
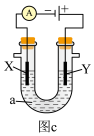
(3)按图c所示装置,以石墨为电极电解氯化钠溶液,阳极为___________ (填“X”或“Y”),实验开始时,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是___________ 。若将X电极材料换为Cu,则X电极上的电极反应式将___________ (填“发生变化”或“不变”)
(4)某原电池装置初始状态如下图所示,电池总反应为2Ag+Cl2=2AgCl。
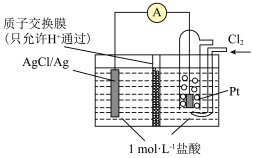
当电路中转移amole-时,交换膜左侧溶液中约减少___________ mol离子。交换膜右侧溶液中c(HCl)___________ (填“>”、“<”或“=”)lmol·L-1(忽略溶液体积变化和Cl2溶于水)。
(1)图a中,电流表指针发生偏转,Zn作负极,则A电极上发生的电极反应式为

(2)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池的结构示意图如图b,电池总反应为
 ,则d电极是
,则d电极是
(3)按图c所示装置,以石墨为电极电解氯化钠溶液,阳极为

(4)某原电池装置初始状态如下图所示,电池总反应为2Ag+Cl2=2AgCl。

当电路中转移amole-时,交换膜左侧溶液中约减少
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:s2--2e-=S、(n-1)S+S2-=Sn2-
①写出电解时阴极的电极反应式:____________ 。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成:____________ 。

①写出电解时阴极的电极反应式:
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成:
您最近一年使用:0次