目前,液流电池是电化学储能领域的一个研究热点,优点是储能容量大、使用寿命长。一种简单钒液流电池的电解液存储在储液罐中,放电时的结构及工作原理如图:
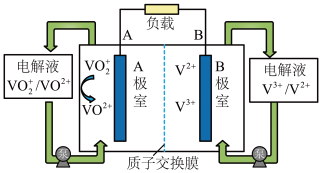
回答下列问题:
(1)放电时,导线中电流方向为_______ ,质子通过质子交换膜方向为_______ (填“从A到B”或“从B到A”)。
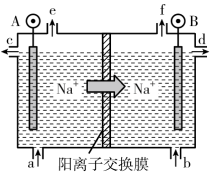
(2)用该电池作为电源电解饱和食盐水,电解反应的化学方程式为_______ ;若欲利用电解所得产物制取含149kgNaClO的消毒液用于环境消毒,理论上电解过程中至少需通过电路_____ mol电子。
(3)若将该电池电极连接电源充电,则A极连接电源的___ 极,发生的电极反应为______ 。

回答下列问题:
(1)放电时,导线中电流方向为
(2)用该电池作为电源电解饱和食盐水,电解反应的化学方程式为
(3)若将该电池电极连接电源充电,则A极连接电源的
更新时间:2020-12-06 09:31:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池。

①当电解质溶液为稀硫酸时:Cu电极是____ (填“正”或“负”)极,其电极反应为____ 。
②当电解质溶液为浓硝酸时:Cu电极是____ 极,其电极反应为____ 。
(2)请写出电解硫酸铜溶液的总化学方程式_____ 。
(1)如图所示,组成一个原电池。

①当电解质溶液为稀硫酸时:Cu电极是
②当电解质溶液为浓硝酸时:Cu电极是
(2)请写出电解硫酸铜溶液的总化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铅蓄电池(原电池)工作时,总反应为:PbO2+Pb+2H2SO4=2PbSO4+2H2O,由此可以判断:
(1)铅蓄电池的电极材料:正极为___________ ,负极为___________ 。
(2)两极的电极反应式:正极为___________ ,负极为___________ 。
(3)工作一段时间后,铅蓄电池电解质溶液的pH___________ (填“变大”、“变小”或“不变”)。
(1)铅蓄电池的电极材料:正极为
(2)两极的电极反应式:正极为
(3)工作一段时间后,铅蓄电池电解质溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是________ (填序号)。
b.盐酸与碳酸氢钠
c.碳酸钙分解
d. 固体与
固体与 固体
固体
e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼( )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:
该反应属于________ 反应(填“放热”或“吸热”), 和
和 的总能量
的总能量________ (填“>”“=”或“<”) 和
和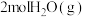 的总能量。
的总能量。
(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。________ (填化学式),负极的电极反应式为________ 。
②电池工作时, 移向
移向________ 电极(填“a”或“b”)。
③当b电极上消耗标况下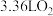 时,电路中转移的电子数为
时,电路中转移的电子数为________ 。
(4)肼( )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式________ 。
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是
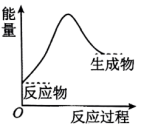
b.盐酸与碳酸氢钠
c.碳酸钙分解
d.
 固体与
固体与 固体
固体e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼(
 )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:化学键 | N-H | N-N | N≡N | O=O | O-H |
能量 | 391 | 154 | 942 | 500 | 463 |
 和
和 的总能量
的总能量 和
和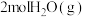 的总能量。
的总能量。(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。
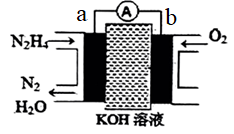
②电池工作时,
 移向
移向③当b电极上消耗标况下
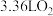 时,电路中转移的电子数为
时,电路中转移的电子数为(4)肼(
 )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。

已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO -2e-=PbSO4
-2e-=PbSO4
正极PbO2+4H++SO +2e-=PbSO4+2H2O
+2e-=PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式_____________ 。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为________ 极。
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量)时,
①若收集到11.2 L(标准状况下)氯气,溶液pH=____________ 。
②若铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为________ L。

已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO
 -2e-=PbSO4
-2e-=PbSO4正极PbO2+4H++SO
 +2e-=PbSO4+2H2O
+2e-=PbSO4+2H2O(1)请写出电解饱和食盐水的化学方程式
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量)时,
①若收集到11.2 L(标准状况下)氯气,溶液pH=
②若铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Zn-MnO2干电池广泛应用,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是_____ 。电池工作时,电流流向___________ (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀。请解释原因_________ 。欲除去Cu2+,最好选用下列试剂中的_________ (填代号)。
A.NaOH B. Zn C. Fe D. NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阳极反应式为________ 。若电路中通过2 mole-,MnO2的理论产量为________ g。
(1)该电池的负极材料是
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀。请解释原因
A.NaOH B. Zn C. Fe D. NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阳极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“循环经济”是目前备受关注的课题,对保护环境和资源的综合利用意义重大。
(1)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用如图1表示。
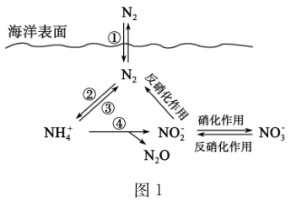
①海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是_______ (填图中数字序号)。
②有氧时,在硝化细菌作用下, 可实现过程④的转化,若产物
可实现过程④的转化,若产物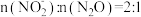 ,则反应中氧化剂与还原剂的物质的量之比为
,则反应中氧化剂与还原剂的物质的量之比为_______ 。
(2)氮循环的过程中产生有毒氧化物 。工业上常用
。工业上常用 溶液吸收法处理。
溶液吸收法处理。
发生的反应有: (Ⅰ)
(Ⅰ)
 (Ⅱ)
(Ⅱ)
将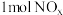 通入
通入 溶液中,被完全吸收,溶液中生成的
溶液中,被完全吸收,溶液中生成的 、
、 两种离子的物质的量随x变化关系如图所示。图2中线段b表示
两种离子的物质的量随x变化关系如图所示。图2中线段b表示_______ (填离子符号)随x值变化的关系;若用溶质质量分数为21.2%的 溶液吸收,则需要
溶液吸收,则需要 溶液至少
溶液至少_______ g。

(3)采用电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收 的装置如图3所示(图中电极均为石墨电极)。
的装置如图3所示(图中电极均为石墨电极)。
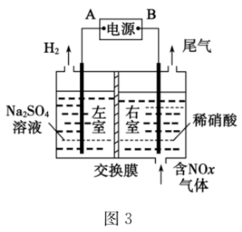
①直流电源的负极为_______ (“A”或“B”);该电解装置应选择_______ (填“阳”或“阴”)离子交换膜。
②若以处理 为模拟实验,阳极发生的电极反应为
为模拟实验,阳极发生的电极反应为_______ 。
(1)氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用如图1表示。

①海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是
②有氧时,在硝化细菌作用下,
 可实现过程④的转化,若产物
可实现过程④的转化,若产物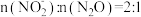 ,则反应中氧化剂与还原剂的物质的量之比为
,则反应中氧化剂与还原剂的物质的量之比为(2)氮循环的过程中产生有毒氧化物
 。工业上常用
。工业上常用 溶液吸收法处理。
溶液吸收法处理。发生的反应有:
 (Ⅰ)
(Ⅰ) (Ⅱ)
(Ⅱ)将
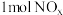 通入
通入 溶液中,被完全吸收,溶液中生成的
溶液中,被完全吸收,溶液中生成的 、
、 两种离子的物质的量随x变化关系如图所示。图2中线段b表示
两种离子的物质的量随x变化关系如图所示。图2中线段b表示 溶液吸收,则需要
溶液吸收,则需要 溶液至少
溶液至少
(3)采用电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益。实验室模拟电解法吸收
 的装置如图3所示(图中电极均为石墨电极)。
的装置如图3所示(图中电极均为石墨电极)。
①直流电源的负极为
②若以处理
 为模拟实验,阳极发生的电极反应为
为模拟实验,阳极发生的电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
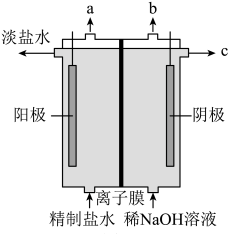
(1)氯气是制备系列含氯化合物的主要原料,请写出化学家舍勒发现氯气的化学方程式:_______ 。也可采用如图所示的装置来制取氯气,装置中氯气的逸出口是_______ (填标号)。
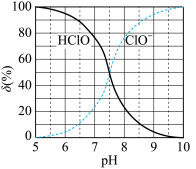
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ,δ(X)=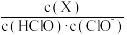 ,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为
,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为____ 。
(3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_______ 。
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为_______ mol;产生“气泡”的化学方程式为_______ 。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是_______ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为_______ kg(保留整数)。
(1)氯气是制备系列含氯化合物的主要原料,请写出化学家舍勒发现氯气的化学方程式:

(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ,δ(X)=
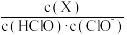 ,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为
,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为
(3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
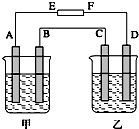
【推荐2】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 X 为阳离子交换膜。

请按要求回答下列问题:
(1)甲烷燃料电池的负极反应式是_______ 。
(2)石墨(C)极的电极反应式是_______ 。
(3)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁极上生成的气体体积为_____ L;丙装置中阴极析出铜的质量为_______ g。

请按要求回答下列问题:
(1)甲烷燃料电池的负极反应式是
(2)石墨(C)极的电极反应式是
(3)若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁极上生成的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如下图所示,甲烧杯中盛有100mL0.50mol•L-1AgNO3溶液,乙烧杯中盛有100mL0.25mol•L-1CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重3.8g,求此时甲、乙装置中共产生多少升气体?(标准状况下)

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
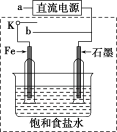
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
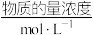 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列小题。
(1)目前已开发出电解法制取ClO2的新工艺。

①用石墨作电极,在一定条件下电解饱和食盐水制取ClO2(如图所示),写出阳极产生ClO2的电极反应式:__________ 。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为________ mol;用平衡移动原理解释阴极区pH增大的原因:_________ 。
(2)粗银精炼装置如图所示,电解液为稀H2SO4,下列说法正确的是________ (填字母)。
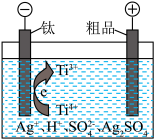
a.体系中存在沉淀溶解平衡:Ag2SO4(s) 2Ag+(aq)+SO
2Ag+(aq)+SO (aq)
(aq)
b.阳极的电极反应式为Ag-e-=Ag+
c.钛电极电势高
d.阴极区可获得超细银粉的原理:Ti3++Ag+=Ag+Ti4+
e.电解液中添加Ti3+/Ti4+,可实现Ti3+/Ti4+循环利用
(3)工业上用PbSiF6、H2SiF6混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、Fe、Zn,杂质总质量分数约为4%)提纯,装置示意图如图所示。

①电解产生的阳极泥的主要成分为________ ,工作一段时间后,溶液中c(Pb2+)__________ (填“增大”“减小”或“不变”)。
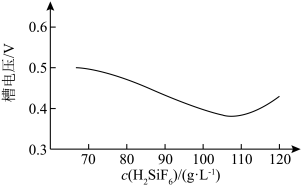
②铅的电解精炼需要调控好电解液中的c(H2SiF6)。其他条件相同时,测得槽电压(槽电压越小,对应铅产率越高)随起始时溶液中c(H2SiF6)的变化趋势如图所示。由图可推知,随c(H2SiF6)增大,铅产率先增大后减小,减小的原因可能是___________ 。
(1)目前已开发出电解法制取ClO2的新工艺。

①用石墨作电极,在一定条件下电解饱和食盐水制取ClO2(如图所示),写出阳极产生ClO2的电极反应式:
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,则通过阳离子交换膜的阳离子的物质的量为
(2)粗银精炼装置如图所示,电解液为稀H2SO4,下列说法正确的是

a.体系中存在沉淀溶解平衡:Ag2SO4(s)
 2Ag+(aq)+SO
2Ag+(aq)+SO (aq)
(aq)b.阳极的电极反应式为Ag-e-=Ag+
c.钛电极电势高
d.阴极区可获得超细银粉的原理:Ti3++Ag+=Ag+Ti4+
e.电解液中添加Ti3+/Ti4+,可实现Ti3+/Ti4+循环利用
(3)工业上用PbSiF6、H2SiF6混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、Fe、Zn,杂质总质量分数约为4%)提纯,装置示意图如图所示。

①电解产生的阳极泥的主要成分为
②铅的电解精炼需要调控好电解液中的c(H2SiF6)。其他条件相同时,测得槽电压(槽电压越小,对应铅产率越高)随起始时溶液中c(H2SiF6)的变化趋势如图所示。由图可推知,随c(H2SiF6)增大,铅产率先增大后减小,减小的原因可能是

您最近一年使用:0次