回答下列问题
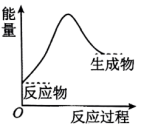
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是________ (填序号)。
b.盐酸与碳酸氢钠
c.碳酸钙分解
d. 固体与
固体与 固体
固体
e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼( )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:
该反应属于________ 反应(填“放热”或“吸热”), 和
和 的总能量
的总能量________ (填“>”“=”或“<”) 和
和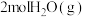 的总能量。
的总能量。
(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。________ (填化学式),负极的电极反应式为________ 。
②电池工作时, 移向
移向________ 电极(填“a”或“b”)。
③当b电极上消耗标况下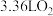 时,电路中转移的电子数为
时,电路中转移的电子数为________ 。
(4)肼( )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式________ 。
(1)化学反应中伴随着能量变化,符合下图能量变化的化学反应是
b.盐酸与碳酸氢钠
c.碳酸钙分解
d.
 固体与
固体与 固体
固体e.硝酸铵溶于水
f.甲烷燃烧
(2)在一定温度和压强下,肼(
 )和
)和 发生如下反应:
发生如下反应: 。已知断裂1mol化学键吸收的能量如下表:
。已知断裂1mol化学键吸收的能量如下表:化学键 | N-H | N-N | N≡N | O=O | O-H |
能量 | 391 | 154 | 942 | 500 | 463 |
 和
和 的总能量
的总能量 和
和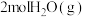 的总能量。
的总能量。(3)以肼为原料的燃料电池具有容量大、能量转化率高、产物无污染等特点,其工作原理如图所示。电解质溶液为20%-30%的KOH溶液。
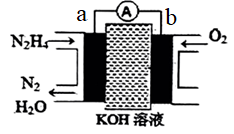
②电池工作时,
 移向
移向③当b电极上消耗标况下
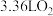 时,电路中转移的电子数为
时,电路中转移的电子数为(4)肼(
 )还是一种良好的火箭推进剂,与助燃剂液态
)还是一种良好的火箭推进剂,与助燃剂液态 发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
发生反应,放出大量热且对环境无污染,写出该反应的化学方程式
更新时间:2024-05-04 15:45:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列各空。
(1)已知数据如图,写出工业合成氨的热化学方程式:___________ 。

(2)0.5 mol甲烷与一定量水蒸气在一定条件下,完全反应生成一氧化碳和氢气,吸热a kJ,则反应物总能量___________ (填“ ”、“
”、“ ”或“=”)生成物总能量。
”或“=”)生成物总能量。
(3)使Cl2和H2O(g)通过灼热炭层,生成气态HCl和CO2,当反应中转移1mol电子时释放145kJ热量。当有1molCO2生成时,ΔH =___________ kJ/mol。
(4)反应mA(g)+nB(g) = pC(g) +qD(g)过程中的能量变化如图所示:

①该反应ΔH =___________ kJ/mol(用含E1、E2式子表示)。
②在反应体系中加入催化剂,ΔH___________ (填“增大”、“减小”、“不变”)。
(1)已知数据如图,写出工业合成氨的热化学方程式:

(2)0.5 mol甲烷与一定量水蒸气在一定条件下,完全反应生成一氧化碳和氢气,吸热a kJ,则反应物总能量
 ”、“
”、“ ”或“=”)生成物总能量。
”或“=”)生成物总能量。(3)使Cl2和H2O(g)通过灼热炭层,生成气态HCl和CO2,当反应中转移1mol电子时释放145kJ热量。当有1molCO2生成时,ΔH =
(4)反应mA(g)+nB(g) = pC(g) +qD(g)过程中的能量变化如图所示:

①该反应ΔH =
②在反应体系中加入催化剂,ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)乙炔的电子式为_____________ ;芒硝的化学式为_______________ 。
(2)在日常生活中我们常使用冷敷袋有两种,第一种所盛装的物质为NH4NO3和水,第二种为过量NH4NO3和Na2CO3·10H2O,使用方法均为将两种原本隔开的物质混合即可降温,第二种还同时产生两种气体,请根据所学知识写出第二种冰袋中发生的化学方程式____________ ,解释其实现降温的原因______________ 。
(1)乙炔的电子式为
(2)在日常生活中我们常使用冷敷袋有两种,第一种所盛装的物质为NH4NO3和水,第二种为过量NH4NO3和Na2CO3·10H2O,使用方法均为将两种原本隔开的物质混合即可降温,第二种还同时产生两种气体,请根据所学知识写出第二种冰袋中发生的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据相关的知识,回答下列问题:
(1)下列变化:①碘的升华②冰熔化③氯化钠溶于水④氯化氢溶于水⑤氢氧化钠溶于水
化学键未被破坏的是_______ (填序号),仅离子键被破坏的是_______ (填序号)。
(2)已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
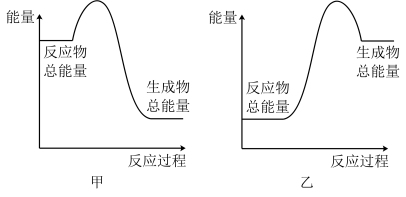
在25℃、1.013×105Pa时,H2(g)与O2(g)反应生成1molH2O(g)的热化学反应方程式为_______ ,该反应为_______ 反应(填“吸热”或“放热”),反应的能量变化可用图_______ 表示(填“甲”或“乙”)。
(3)已知:①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH1=akJ/mol
②2H2O(1)=2H2(g)+O2(g)ΔH2=bkJ/mol
③H2O(l)=H2O(g)ΔH3=ckJ/mol
则甲烷的燃烧热ΔH=_______ kJ/mol(用含a、b、c的式子表示)。
(4)下列变化中,属于吸热反应的是_______ (填序号)。
①铝片与稀盐酸的反应
②Ba(OH)2·8H2O晶体与NH4Cl晶体混合反应
③铁在氯气中燃烧,
④氯酸钾分解制氧气
⑤生石灰与水反应生成熟石灰
(1)下列变化:①碘的升华②冰熔化③氯化钠溶于水④氯化氢溶于水⑤氢氧化钠溶于水
化学键未被破坏的是
(2)已知一定条件下,1mol化学键断裂时吸收的能量相关数据如下表:
| 化学键 | H-H | O=O | H-O |
| 能量(kJ) | 436 | 496 | 463 |
在25℃、1.013×105Pa时,H2(g)与O2(g)反应生成1molH2O(g)的热化学反应方程式为

(3)已知:①CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH1=akJ/mol
②2H2O(1)=2H2(g)+O2(g)ΔH2=bkJ/mol
③H2O(l)=H2O(g)ΔH3=ckJ/mol
则甲烷的燃烧热ΔH=
(4)下列变化中,属于吸热反应的是
①铝片与稀盐酸的反应
②Ba(OH)2·8H2O晶体与NH4Cl晶体混合反应
③铁在氯气中燃烧,
④氯酸钾分解制氧气
⑤生石灰与水反应生成熟石灰
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从__ 口通入(填“a”或“b”),X极为电池的___ (填“正”或“负”)极。
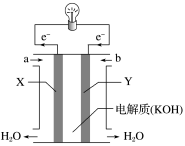
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的___ 极;电子从该极__ (填“流入”或“流出”)。电池总反应为:___ 。

(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H2+2O2--4e-=2H2O
B极:O2+4e-=2O2-
则A极是电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用。某学习小组按如下图所示装置探究化学能与电能的相互转化:
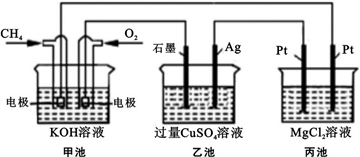
(1) 甲池是_____ 装置,通入CH4气体的电极上的反应式为_____ 。乙池中SO42- 移向_____ 电极(填“石墨”或“Ag”)
(2) 当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化_____ mol,乙池若要恢复电解前的状态则需要加入_____ g _____ (填物质名称)。
(3) 丙池中发生的电解反应的离子方程式为_____ 。

(1) 甲池是
(2) 当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化
(3) 丙池中发生的电解反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】原电池揭示了氧化还原反应的本质是电子转移,实现了化学能转化成电能,使氧化还原反应在现代生活中获得重大应用,从而改变了人们的生活方式。某兴趣小组为探究原电池工作原理,利用金属Zn与稀H2SO4反应,通过如图所示装置A、B进行实验,实验过程中装置A内溶液的温度升高,装置B的电流计指针发生偏转。
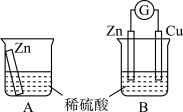
根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作______ (填“正”或“负”)极,Zn电极上的电极反应式为_____ 。
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为______ 。
(3)从能量转化的角度来看,装置A中反应物的总能量______ (填“高于”、“低于”或“=”)生成物的总能量;从反应速率的角度上看,可以观察到A中反应比B中______ (填“快”或“慢”)。
(4)该小组同学由此得出的结论错误的是______ 。(多选)

根据所学知识,完成下列各题:
(1)装置B为原电池,则Cu作
(2)一般把金属导线称为“电子导体”,把电解质溶液称为“离子导体”。装置B中电池工作时“电子导体”中电子的流动方向可描述为
(3)从能量转化的角度来看,装置A中反应物的总能量
(4)该小组同学由此得出的结论错误的是
| A.任何自发进行的氧化还原反应均可以设计成原电池 |
| B.装置B中Cu电极不可用碳棒代替 |
| C.原电池的负极发生还原反应 |
| D.原电池装置中化学能全部转化为电能 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图为相互串联的三个装置,试回答:

(1)写出甲池负极的电极反应式:___________ 。
(2)若利用乙池在铁片上镀银,则B电极反应式是___________ 。
(3)若利用乙池进行粗铜的电解精炼,则___________ 极(填“A”或“B”)是粗铜。
(4)向丙池溶液中滴加几滴酚酞试液,___________ 电极(填“石墨”或“Fe”)周围先出现红色;若甲池消耗3.2g CH3OH气体,则丙池中阳极上产生气体的体积(标准状态)为___________ 。

(1)写出甲池负极的电极反应式:
(2)若利用乙池在铁片上镀银,则B电极反应式是
(3)若利用乙池进行粗铜的电解精炼,则
(4)向丙池溶液中滴加几滴酚酞试液,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如图所示,E为浸有Na2SO4溶液的滤纸,并加入几滴酚酞。A、B均为Pt片,压在滤纸两端,R、S为电源的电极。M、N为惰性电极。G为电流计,K为开关。试管C、D和电解池中都充满KOH溶液。若在滤纸E上滴一滴紫色的KMnO4溶液,断开K,接通电源一段时间后,C、D中有气体产生。

(1)R为电源的_______ 极。
(2)A极附近的溶液变为红色,B极的电极反应式为_______ 。
(3)滤纸上的紫色点移向_______ (填"A极"或"B极")。
(4)当试管C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,主要是因为_______ ,写出C极的电极反应式:_______ 。

(1)R为电源的
(2)A极附近的溶液变为红色,B极的电极反应式为
(3)滤纸上的紫色点移向
(4)当试管C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,主要是因为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于____
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式________________ 。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

__________________
正极反应___________________________
负极反应___________________________
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

______________________
(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式_____________ 。教材中引发铝热反应的试剂是__________ 。

(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于
(填选项序号)
A.金属的导电性强弱B.金属在地壳中的含量多少
C.金属的化合价高低D.金属的活动性大小
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矾等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。

正极反应
负极反应
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请参照元素①一④在表中的位置回答下列问题:
(1)③、⑤、⑥的离子半径由大到小的顺序为____________ '(用离子符号表示)。
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式_______________
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是______
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小_____
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式______
(6)①和④的单质可组成燃料电池,正极反应物为_____ (用化学式表示,下同),若电解溶液为稀硫酸,写出负极的电极反应__________
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③、⑤、⑥的离子半径由大到小的顺序为
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式
(6)①和④的单质可组成燃料电池,正极反应物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以甲烷燃料电池为例来分析在不同的环境中电极反应的书写方法:
(1)碱性条件下燃料电池的负极反应:______________ 。
(2)碱性条件下燃料电池的正极反应:______________ 。
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:______________ 。
(4)固体电解质(高温下能传导O2-)环境中电池的正极反应:______________ 。
(1)碱性条件下燃料电池的负极反应:
(2)碱性条件下燃料电池的正极反应:
(3)固体电解质(高温下能传导O2-)环境中电池的负极反应:
(4)固体电解质(高温下能传导O2-)环境中电池的正极反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:___________ 。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置______ (填“能”或“不能”)
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:__________ 。当反应中收集到标准状况下224mL气体时,消耗的电极质量为________ g。
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入____ 极(填a或b,下同),电子从____ 极流出,电解质溶液中OH-向____ 极移动。
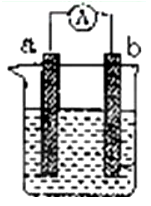
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置
形成原电池,若不能,请说明理由;若能,请指出正、负极材料:
(3)燃料电池工作原理是将燃料和氧化剂(如O2)反应产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入
您最近一年使用:0次



