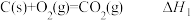如下图所示,在101 kPa时,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1。下列说法中正确的是

| A.断裂金刚石和石墨中的化学键要放出能量 |
| B.石墨转化成金刚石需要吸收能量,是物理变化 |
| C.石墨比金刚石稳定 |
| D.1 mol金刚石与1 mol O2的总能量低于1 mol CO2的总能量 |
21-22高二下·云南丽江·阶段练习 查看更多[5]
云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题陕西省西安市第三中学2021-2022学年高一下学期期中考试化学试题(已下线)1.1.1 反应热 焓变-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)辽宁省营口市第二高级中学2021-2022学年高一下学期第一次月考化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期开学考试化学试题
更新时间:2022-03-28 19:27:11
|
相似题推荐
【推荐1】下列说法不正确的是
| A.化学反应除了生成新物质外,还伴随着能量的变化 |
| B.△H<0的反应不加热可能不发生,对于△H>0的反应不加热也可能发生 |
| C.石墨转变为金刚石是吸热反应,则金刚石比石墨更稳定 |
| D.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
您最近一年使用:0次
【推荐2】下列有关热化学方程式的叙述正确的是
| A.若C(s)+O2(g)=CO2(g) △H1,CO2(g)+C(s)=2CO(g) △H2,2CO(g)+O2(g)=2CO2(g) △H3,则反应热的关系:△H1=△H2+△H3 |
B.若2H2(g)+O2(g)=2H2O(1) △H4,H2(g)+ O2(g)=H2O(1) △H5,则反应热的关系:△H4=△H5 O2(g)=H2O(1) △H5,则反应热的关系:△H4=△H5 |
| C.若2SO2(g)+O2(g)=2SO3(g) △H<0,则物质的稳定性:SO2>SO3 |
| D.若一个化学反应中反应物总键能大于生成物总键能,则该反应的△H<0 |
您最近一年使用:0次
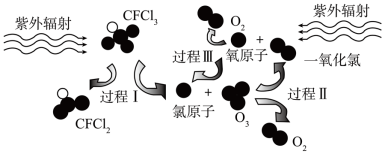
【推荐1】炭黑是雾霾的重要颗粒物,研究发现它可以活化氧分子,生成活化氧。活化过程的能量变化模拟计算结果如右图所示。活化氧具有极强氧化性,能快速氧化SO2。对于由多个步骤构成的复杂反应,总反应活化能由决速步(活化能最高的步骤)及决速步之前所有步骤的活化能共同决定。下列说法不正确的是
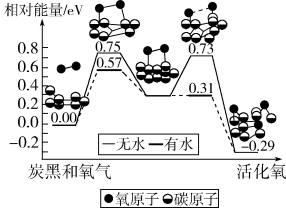

| A.每活化一个氧分子放出0.29 eV能量 |
| B.水可使氧分子活化反应的活化能降低0.42 eV |
| C.氧分子的活化是O=O的断裂与C-O 键形成的过程 |
| D.炭黑颗粒是大气中SO2转化为SO3的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】二氟卡宾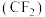 作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注.硫单质与二氟卡宾可以形成
作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注.硫单质与二氟卡宾可以形成 ,反应历程如图所示:
,反应历程如图所示:
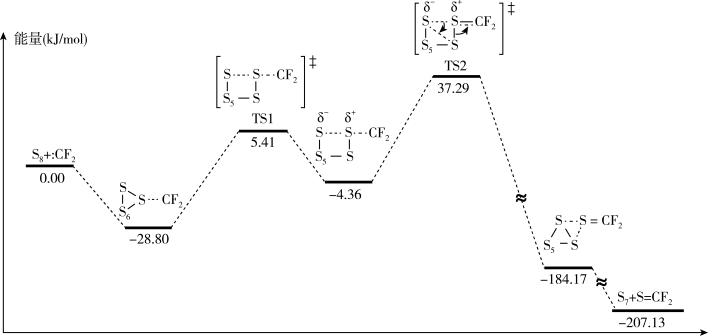
下列叙述错误的是
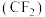 作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注.硫单质与二氟卡宾可以形成
作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注.硫单质与二氟卡宾可以形成 ,反应历程如图所示:
,反应历程如图所示:
下列叙述错误的是
A. 和 和 生成 生成 反应的 反应的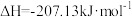 |
B.由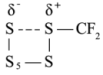 生成 生成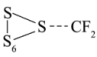 的活化能为 的活化能为 |
C.上述反应历程中存在 键的断裂和生成 键的断裂和生成 |
D.决定反应速率的基元反应的活化能为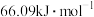 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知热化学方程式2NO(g)+2CO(g) N2(g)+2CO2(g) △H=a kJ/mol。T K时,在2 L恒容密闭容器中充入2mol NO 和2mol CO,保持温度不变,5 min后反应达到平衡状态,此时c(N2)=0.4mol/L。下列说法中错误的是
N2(g)+2CO2(g) △H=a kJ/mol。T K时,在2 L恒容密闭容器中充入2mol NO 和2mol CO,保持温度不变,5 min后反应达到平衡状态,此时c(N2)=0.4mol/L。下列说法中错误的是
 N2(g)+2CO2(g) △H=a kJ/mol。T K时,在2 L恒容密闭容器中充入2mol NO 和2mol CO,保持温度不变,5 min后反应达到平衡状态,此时c(N2)=0.4mol/L。下列说法中错误的是
N2(g)+2CO2(g) △H=a kJ/mol。T K时,在2 L恒容密闭容器中充入2mol NO 和2mol CO,保持温度不变,5 min后反应达到平衡状态,此时c(N2)=0.4mol/L。下列说法中错误的是| A.若该反应是放热反应,则a<0 |
| B.用NO表示的平均化学反应速率v(NO)为0.16mol/(L·min) |
| C.达到化学平衡时,CO的转化率是80% |
| D.保持温度不变,若再向上述达到平衡的体系中充入2mol NO 和2mol CO,则反应重新达到平衡时c(N2)等于0.8mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】近年来,利用电化学催化方法进行CO2转化的研究引起了世界范围内的高度关注。下图是以Cu作为催化剂CO2转化为甲酸的反应过程,下列有关说法不正确 的是
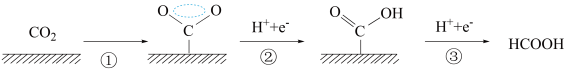
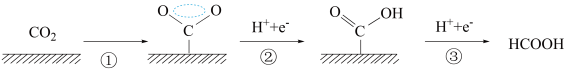
| A.过程①说明在催化剂作用下,O-C-O之间形成了一种特殊的化学键 |
| B.过程②和③吸收了能量并形成了O-H键和C-H键 |
| C.CO2和HCOOH中均只含有极性共价键 |
| D.每1molCO2完全转化为甲酸需得2mole- |
您最近一年使用:0次
【推荐2】环戊二烯之( ) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是

 ) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
) 是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产,根据能量循环图和表格中的键能,下列说法正确的是
| 共价键 | 键能/ |
| H-H | 436 |
| H-I | 299 |
| I-I | 151 |
| A.△H1+△H2+△H3=0 |
| B.△H1<△H3 |
C.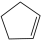 (g)转化为 (g)转化为 (g)的过程中,有C-H的断裂和形成 (g)的过程中,有C-H的断裂和形成 |
| D.在相同条件下,生成 2molHCl(g) 的△H2′<△H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于反应热的说法正确的是( )
| A.已知甲烷的燃烧热为890.3kJ·mol-1,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1 |
B.将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-38.6kJ·mol-1 2NH3(g) ΔH=-38.6kJ·mol-1 |
| C.已知C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1,说明金刚石具有的能量比石墨低 |
| D.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.4kJ·mol-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:100 kPa,1 mol石墨完全燃烧放热393.5 kJ;1 mol金刚石完全燃烧放热395.4 kJ,下列说法错误的是
| A.石墨比金刚石稳定 |
| B.石墨与金刚石互为同素异形体 |
| C.相同质量的石墨比金刚石总能量高 |
| D.100 kPa,1 mol CO2(g)完全分解为石墨和O2(g)吸热393.5 kJ |
您最近一年使用:0次

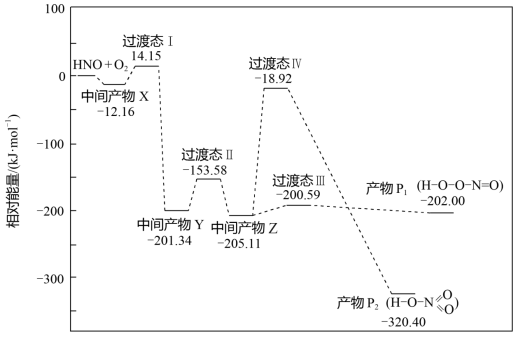
 (P1)>
(P1)>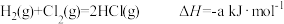
 的燃烧热
的燃烧热
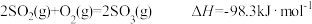
 的能量一定比
的能量一定比 能量高
能量高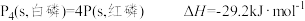
 (s,白磷)比P(s,红磷)稳定
(s,白磷)比P(s,红磷)稳定