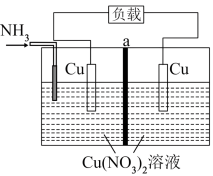
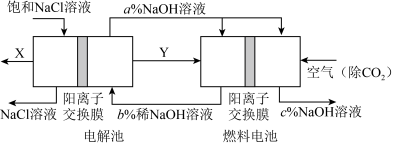游泳池水质普遍存在尿素超标现象,一种电化学除游泳池中尿素的实验装置如图所示,其中钌钛常用作析氯电极,不参与电解。已知:3NaClO+CO(NH2)2=3NaCl+2H2O+N2↑+CO2↑,下列说法正确的是
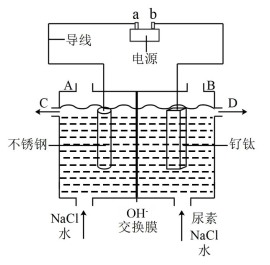

| A.a为电源正极,b为电源负极 |
| B.阳极区反应涉及Cl2+2NaOH=NaCl+NaClO+H2O |
| C.电解过程中不锈钢电极附近溶液pH降低 |
| D.电解过程中每逸出22.4LN2,电路中至少通过6mol电子 |
更新时间:2022-04-09 13:15:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于工业生产的说法中正确的是
| A.氯碱工业中阳离子交换膜的主要作用是防止氯气和氢气以及氢氧化钠反应 |
| B.硫酸工业中合成SO3通常采用常压,是因为常压比高压更有利于SO3的生成 |
| C.电解精炼铜时,纯铜作为阳极,粗铜作为阴极 |
| D.工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为阳离子交换膜法电解饱和食盐水原理示意图,下列说法不正确的是( )
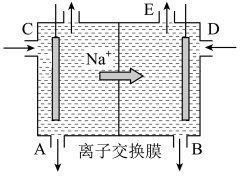

| A.从E口逸出的气体是H2 |
| B.从D口加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH |
| D.粗盐水中含Ca2+、Mg2+、Fe3+、SO42-等离子,精制时先加Na2CO3溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】硼酸(H3BO3)是一种重要的化工原料,以下是电解NaB(OH)4溶液制备H3BO3的原理示意图,下列叙述不正确的是


| A.X 为电源正极,Y 为电源负极 |
| B.N室发生的电极反应式:2H2O-4e -=O2↑+4H+ |
| C.a、c为阳离子交换膜,b为阴离子交换膜 |
| D.理论上每生成1 mol H3BO3,两极室共产生标准状况下16.8 L 气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】通过下列实验可以从废银催化剂(Ag、 和少量
和少量 )中回收银:
)中回收银:
 和少量
和少量 )中回收银:
)中回收银: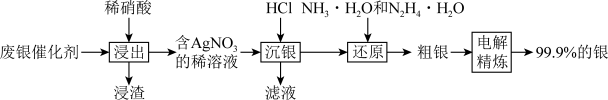
A.滤渣的主要成分是 |
B.还原过程反应的离子方程式: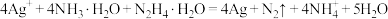 |
C.浸出生成等物质的量的 ,若使用浓硝酸, ,若使用浓硝酸, 利用率会降低 利用率会降低 |
| D.若使用电解法电解废银催化剂制取银,该催化剂应与直流电源的正极连接 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
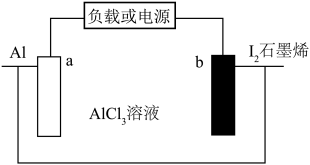
【推荐1】松山湖材料实验室李洪飞首次研究了碘正极在水系铝离子电池中的转化反应化学( )。下列叙述错误的是
)。下列叙述错误的是
 )。下列叙述错误的是
)。下列叙述错误的是
A.放电时, 在正极上发生还原反应 在正极上发生还原反应 |
B.放电时, 极质量减少 极质量减少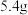 理论上转移约 理论上转移约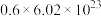 个电子 个电子 |
C.充电时, 极反应之一为 极反应之一为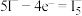 |
D.充电时, 参与反应生成 参与反应生成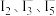 物质的量之比一定为 物质的量之比一定为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图,甲池的总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法不正确的是
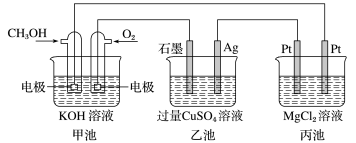

| A.甲池中每消耗2mol CH3OH,电解液中通过12mol电子 |
| B.反应一段时间后,向乙池中加入一定量CuO固体能使CuSO4溶液恢复原浓度 |
| C.反应一段时间后,丙池中会产生白色沉淀且不会溶解 |
| D.反应一段时间后,甲、乙两池pH均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是
| A.Al、Cu、浓H2SO4组成原电池,负极反应式为:Al-3eˉ=Al3+ |
| B.Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3eˉ+4OHˉ=AlO2ˉ+2H2O |
| C.由Fe、Cu、浓硝酸组成原电池,负极反应式为:Fe-3eˉ=Fe3+ |
| D.由Fe、Cu、FeCl3溶液组成原电池,负极反应式:Cu-2eˉ=Cu2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】次磷酸钴[Co(H2PO2)2]广泛应用于化学电镀,工业上利用电渗析法制取次磷酸钴的原理如图所示。
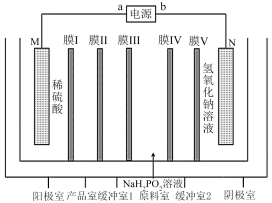
已知:①该装置的电极材料分别为金属钴和不锈钢;
②Co(H2PO2)2溶液在强碱性条件下通过自身催化发生氧化还原反应,实现化学镀钴。
下列说法中正确的是

已知:①该装置的电极材料分别为金属钴和不锈钢;
②Co(H2PO2)2溶液在强碱性条件下通过自身催化发生氧化还原反应,实现化学镀钴。
下列说法中正确的是
| A.M电极材料为不锈钢 |
| B.膜Ⅰ、膜Ⅴ为阳离子交换膜,膜Ⅱ、膜Ⅲ为阴离子交换膜 |
| C.M电极反应为2H2O-4e-=O2↑+4H+ |
D.化学镀钴过程中反应可能为Co2++ +3OH-=Co+ +3OH-=Co+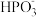 +2H2O +2H2O |
您最近一年使用:0次

 的形式存在,并存在电离平衡
的形式存在,并存在电离平衡 。
。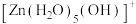 浓度增大
浓度增大 电极附近可能有
电极附近可能有 产生
产生 ,Ⅲ室溶液质量理论上减少
,Ⅲ室溶液质量理论上减少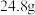
 [Cu(NH3)4]2+ ΔH<0。下列说法正确的是(
[Cu(NH3)4]2+ ΔH<0。下列说法正确的是(