W、X、Y、R为依次增大的短周期主族元素,X的一种同位素可用于文物年代的测定,X核外电子数与Y的核外最外层电子数相等,R为地壳中含量最高的金属元素。含这四种元素的一种阴离子结构如图所示。下列叙述正正确的是


| A.由W、X和Y三种元素可形成18电子结构分子 |
| B.该阴离子具有很强的氧化性 |
| C.简单氢化物稳定性:Y<X |
| D.原子半径:W<X<Y |
21-22高三下·湖南·阶段练习 查看更多[2]
更新时间:2022-04-11 17:32:28
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】W、X、Y、Z是原子序数依次增大的短周期主族元素,化合物X2W2的颜色为淡黄色,W和Y同族。下列叙述正确的是
| A.Z的氧化物的水化物是强酸 |
| B.原子半径:X>W>Y>Z |
| C.X的单质是周期表中最容易失去电子的金属 |
| D.W与Z形成的一种化合物可用于自来水消毒 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期元素形成的化合物(W2XYZ4M2)作为电池的电解液添加剂,能显著提高电池的容量和性能。X、Y、Z、W为同周期元素且原子序数依次增大,其中X的最外层电子数为最内电子数的1/2,化合物YZ2的总电子数为奇数,且易形成二聚物Y2Z4(常温下为无色气体),化合物MZ2中M的质量分数分别为50%。下列说法错误的是
| A.简单离子的半径:Z>X |
| B.简单氢化物的热稳定性:M>W |
| C.YZ2与水反应可以生成化合物YZ |
| D.Y、M的最高价氧化物的水化物均为强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向盛有SO2水溶液的试管中滴加几滴酸性KMnO4溶液,振荡,观察溶液颜色变化 | SO2具有漂白性 |
| B | 将20℃0.5mol·L-1CH3COONa溶液加热到40℃,用pH传感器测量溶液的pH | 温度对CH3COO-水解平衡的影响 |
| C | 向Na2CO3溶液中滴加浓盐酸,反应产生的气体直接通入Na2SiO3溶液中 | 非金属性:C>Si |
| D | 向浓度均为0.01mol·L-1的Na2CO3和Na2SO4的混合液中滴少量0.01mol·L-1的BaCl2溶液 | Ksp(BaCO3)>Ksp(BaSO4) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,X和Z两元素的原子序数之和等于W元素的原子序数。下列说法正确的是
X | Y | Z |
W |
| A.X、W分别与Y都能形成两种或两种以上的化合物,这些化合物都是酸性氧化物 |
| B.X、Y、Z都能形成10电子的氢化物,其中Z的最简单氢化物沸点最高 |
| C.X、Y、W与氢四种元素能组成离子化合物,该化合物一定能发生水解 |
| D.X和W两元素的氧化物对应的水化物的酸性:X>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R为元素周期表中的电负性最强的元素。则下列判断正确的是( )
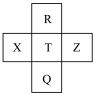

| A.非金属性:Z<T<X |
| B.R与Q的电子数相差24 |
| C.气态氢化物的沸点:R<T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
您最近一年使用:0次



