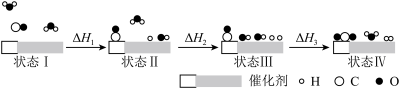
已知反应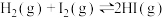 中,每生成
中,每生成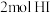 时会有akJ的能量放出,又知有关化学键键能如下,下列说法正确的是
时会有akJ的能量放出,又知有关化学键键能如下,下列说法正确的是
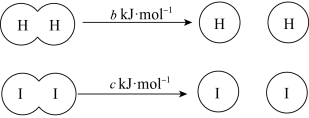
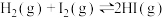 中,每生成
中,每生成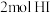 时会有akJ的能量放出,又知有关化学键键能如下,下列说法正确的是
时会有akJ的能量放出,又知有关化学键键能如下,下列说法正确的是
A. 的能量比 的能量比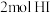 的能量高 的能量高 |
B.将 与 与 混合,充分反应后放出的热量为0.5akJ 混合,充分反应后放出的热量为0.5akJ |
C. 是吸热变化 是吸热变化 |
D.H-I键的键能为 |
更新时间:2022-04-20 15:40:07
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业上用催化氧化法制取SO3,再用浓硫酸吸收SO3得到发烟硫酸(H2SO4·SO3),发烟硫酸加水可以得到浓硫酸。催化氧化法制取SO3的反应为:2SO2(g)+O2(g)⇌2SO3(g) 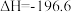 kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
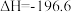 kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是
kJ·mol-1,下列关于工业上制取浓硫酸的说法正确的是| A.2molSO2(g)和1molO2(g)所含化学键的键能总和比2molSO3(g)大196.6kJ·mol-1 |
| B.催化氧化法制取SO3能够自发进行的原因是∆S>0 |
| C.工业上用浓硫酸吸收SO3时是将SO3从吸收塔底部通入,浓硫酸从塔顶喷淋下来,这样操作的目的是为了提高SO3的吸收率 |
| D.将1molH2SO4·SO3全部转化为H2SO4需消耗水2mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关热化学方程式及其叙述正确的是
| A.氢气的燃烧热为285.5 kJ/mol,则电解水的热化学方程式为:2H2O(1)=2H2(g) +O2(g)△H=+285.5kJ/mol |
| B.甲烷的燃烧热为890kJ/mol,则甲烷燃烧的热化学方程式为:CH4(g) +2O2(g) =CO2(g) +2H2O(g)△H=-890kJ/mol |
| C.已知:2C(s) +O2(g) =2CO(g)△H=-221kJ/mol,则C的燃烧热△H<-110.5kJ/mol |
| D.HF与NaOH溶液反应:H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】理论研究表明,在101kPa和298K下,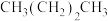 (正丁烷)
(正丁烷)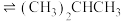 (异丁烷)异构化反应过程的能量变化如图所示。下列说法错误的是
(异丁烷)异构化反应过程的能量变化如图所示。下列说法错误的是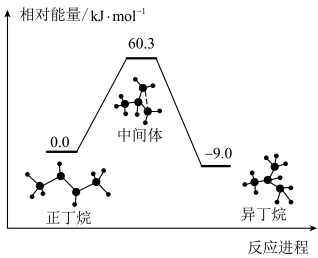
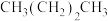 (正丁烷)
(正丁烷)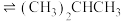 (异丁烷)异构化反应过程的能量变化如图所示。下列说法错误的是
(异丁烷)异构化反应过程的能量变化如图所示。下列说法错误的是
A.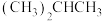 比 比 稳定 稳定 |
B.该异构化反应的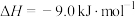 |
| C.正反应的活化能小于逆反应的活化能 |
| D.使用催化剂,可以改变反应的反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子( );第二步Br- 进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4加成产物的比例分别为70:30和15:85。下列说法错误的是
);第二步Br- 进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4加成产物的比例分别为70:30和15:85。下列说法错误的是

 );第二步Br- 进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4加成产物的比例分别为70:30和15:85。下列说法错误的是
);第二步Br- 进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4加成产物的比例分别为70:30和15:85。下列说法错误的是
| A.1,4-加成产物比1,2-加成产物稳定 |
| B.两种产物的化学键种类和数目相同,但1,2-加成产物的总键能更大 |
| C.相同条件下,第二步正反应(或逆反应)比较:1,2-加成较1,4-加成更易发生 |
| D.从0℃升至40℃,1,2-加成正反 应速率的增大程度小于其逆反应速率的增大程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ·mol-1

下列说法不正确的是

下列说法不正确的是
| A.H2的燃烧热是483.6kJ/mol |
| B.破坏1molH-O键需要的能量是463.4kJ |
| C.H2O(g)=H2(g)+1/2O2(g) ΔH=+241.8kJ·mol-1 |
| D.H2(g)中的H-H键比H2O(g)中的H-O键弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应可逆反应:2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.达到平衡时SO2的消耗速率等于O2的生成速率 |
| B.使用合适的催化剂可将SO2全部转化为SO3 |
| C.2mol SO2气体和1mol O2气体的总能量大于2mol SO3气体的能量 |
| D.断开2mol SO2和1mol O2中共价键所吸收的能量大于形成2mol SO3中共价键所放出的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.干冰汽化需要吸收大量的热,这个变化是吸收能量的化学反应 |
| B.木炭需要加热到一定温度才能燃烧,所以木炭燃烧是吸收能量的反应 |
| C.酒精可用作燃料,酒精燃烧是释放能量的反应 |
| D.铝热反应放出大量的热(金属熔化),说明该反应常温下即可发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据如图提供的信息,下列所得结论正确的是
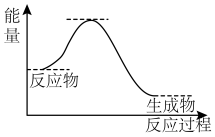

| A.该反应为吸热反应 |
| B.反应物比生成物稳定 |
| C.只有在加热条件下反应才能进行 |
| D.反应中断开化学键吸收的总能量低于形成化学键释放的总能量 |
您最近一年使用:0次

 的燃烧热不同
的燃烧热不同
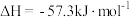 ,则稀
,则稀 溶液与浓硫酸完全反应生成
溶液与浓硫酸完全反应生成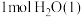 时,放出的热量少于
时,放出的热量少于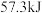
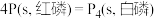
 ,可知红磷比白磷稳定
,可知红磷比白磷稳定
 )。下列有关说法正确的是
)。下列有关说法正确的是
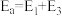

 的反应,必须加热才能进行
的反应,必须加热才能进行

