工业上用CO2制备甲醇,反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49kJ·mol-1。下列有关该反应的说法正确的是
CH3OH(g)+H2O(g) △H=-49kJ·mol-1。下列有关该反应的说法正确的是
 CH3OH(g)+H2O(g) △H=-49kJ·mol-1。下列有关该反应的说法正确的是
CH3OH(g)+H2O(g) △H=-49kJ·mol-1。下列有关该反应的说法正确的是| A.每生成18gH2O(l),放出能量大于49kJ | B.选择合适的催化剂能减小反应的焓变 |
| C.正反应活化能小于逆反应活化能 | D.化学键的键能之和:反应物大于生成物 |
更新时间:2022-04-19 10:18:59
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】溴分子易极化,使分子内溴原子分别带部分正电荷和部分负电荷。在一定条件 下CH2=CH-CH=CH2与Br2 发生加成反应会得到两种产物,且两种产物可通过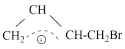 互相转化,反应历程可表示为:
互相转化,反应历程可表示为:
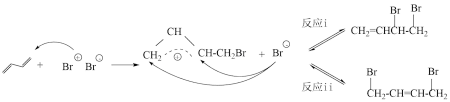
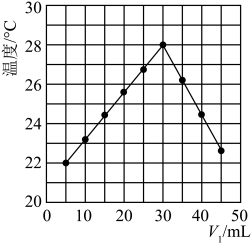
CH2 =CHCHBrCH2Br与CH2BrCH =CHCH2Br相互转化的能量变化如下图所示。已知,同一反应在不同温度下反应速率常数与活化能的关系如下: (其中R为常数)。下列叙述错误的是
(其中R为常数)。下列叙述错误的是
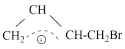 互相转化,反应历程可表示为:
互相转化,反应历程可表示为:
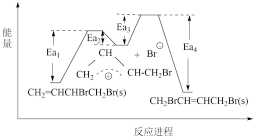
CH2 =CHCHBrCH2Br与CH2BrCH =CHCH2Br相互转化的能量变化如下图所示。已知,同一反应在不同温度下反应速率常数与活化能的关系如下:
 (其中R为常数)。下列叙述错误的是
(其中R为常数)。下列叙述错误的是
| A.相同条件下,反应i的速率比反应ii快 |
| B.升高反应温度,更有利于CH2 = CHCHBrCH2Br的生成 |
| C.反应CH2 =CHCHBrCH2Br(s) →CH2BrCH =CHCH2Br(s)的ΔH=Ea4 +Ea2-Ea1 –Ea3 |
| D.相同条件下,反应达平衡后产物中CH2 BrCH = CHCH2Br含量更大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】根据Ca(OH)2/CaO体系的能量循环图,下列说法正确的是
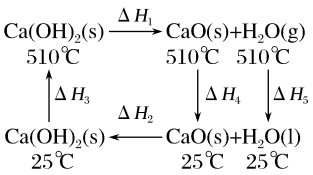

| A.ΔH5<0 | B.ΔH1+ΔH2=0 |
| C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5=0 | D.ΔH3=ΔH4+ΔH5 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列各组热化学方程式中,∆H的比较正确的是
①C(s)+O2(g)=CO2(g) ∆H1 C(s)+ O2(g)=CO (g) ∆H2
O2(g)=CO (g) ∆H2
②S(s)+O2(g)=SO2(g) ∆H3 S(g)+O2(g)=SO2(g) ∆H4
③H2(g)+ O2(g)=H2O(l) ∆H5 2H2(g)+O2(g)=2H2O(l) ∆H6
O2(g)=H2O(l) ∆H5 2H2(g)+O2(g)=2H2O(l) ∆H6
④CaO(s)+H2O(l)=Ca(OH)2(s) ∆H7 CaCO3(s)=CaO(s)+CO2(g) ∆H8
①C(s)+O2(g)=CO2(g) ∆H1 C(s)+
 O2(g)=CO (g) ∆H2
O2(g)=CO (g) ∆H2②S(s)+O2(g)=SO2(g) ∆H3 S(g)+O2(g)=SO2(g) ∆H4
③H2(g)+
 O2(g)=H2O(l) ∆H5 2H2(g)+O2(g)=2H2O(l) ∆H6
O2(g)=H2O(l) ∆H5 2H2(g)+O2(g)=2H2O(l) ∆H6④CaO(s)+H2O(l)=Ca(OH)2(s) ∆H7 CaCO3(s)=CaO(s)+CO2(g) ∆H8
| A.∆H1<∆H2 | B.∆H3<∆H4 | C.∆H5>∆H6 | D.∆H7>∆H8 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】甲烷重整制备合成气的传统方法:

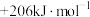 。厦门大学温在恭在实验室中采用
。厦门大学温在恭在实验室中采用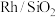 作催化剂,以
作催化剂,以 、
、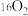 、
、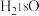 、He为原料气的同位素示踪实验结果表明,生成物
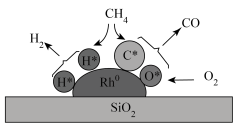
、He为原料气的同位素示踪实验结果表明,生成物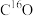 的含量占CO生成总量的92.3%,氧化反应机理如图所示。下列说法正确的是
的含量占CO生成总量的92.3%,氧化反应机理如图所示。下列说法正确的是


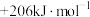 。厦门大学温在恭在实验室中采用
。厦门大学温在恭在实验室中采用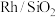 作催化剂,以
作催化剂,以 、
、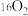 、
、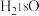 、He为原料气的同位素示踪实验结果表明,生成物
、He为原料气的同位素示踪实验结果表明,生成物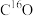 的含量占CO生成总量的92.3%,氧化反应机理如图所示。下列说法正确的是
的含量占CO生成总量的92.3%,氧化反应机理如图所示。下列说法正确的是
A.消耗等物质的量 ,甲烷传统重整方法比 ,甲烷传统重整方法比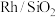 催化剂法生成的 催化剂法生成的 多 多 |
B.甲烷传统重整方法和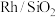 催化剂上重整反应的 催化剂上重整反应的 相等 相等 |
C.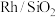 催化剂上 催化剂上 与 与 不反应 不反应 |
D.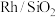 催化剂上甲烷重整反应存在极性键和非极性键的断裂 催化剂上甲烷重整反应存在极性键和非极性键的断裂 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,H2(g)+I2(g) 2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是
2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是

 2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是
2HI(g)反应达到了化学平衡,其反应过程对应的能量变化如图所示。下列说法正确的是
| A.该反应为放热反应 |
| B.该反应的△H=Ea'-Ea |
| C.该反应中加入催化剂,可增大反应速率,同时改变焓变 |
| D.温度升高,单位体积的活化分子百分数增加,反应速率加快,且平衡逆向移动 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知在相同状况下,同一化学键断裂需要吸收的能量等于形成该化学键放出的能量。下列说法错误的是( )
| A.电解熔融的Al2O3可以制得金属铝和氧气,该反应是一个放出能量的反应 |
| B.H2(g)+F2(g)=2HF(g) △H="-270" kJ/mol ,1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
C.相同状况下,反应2SO2+O2 2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应 2SO3是一个放热反应,则反应2SO3=2SO2+O2是一个吸热反应 |
| D.破坏1 mol氢气中的化学键消耗的能量为Q1kJ,破坏1 mol氯气中的化学键消耗的能量为Q2kJ,形成1 mol氯化氢中的化学键释放的能量为Q3kJ,则Q1+Q2<2Q3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】以CO和H2为原料合成甲醇是工业上的成熟方法,直接以CO2为原料生产甲醇是目前的研究热点。我国科学家用CO2人工合成淀粉时,第一步就需要CO2转化为甲醇。
已知:①CO(g)+2H2(g) CH3OH(g) △H1=-90.5kJ·mol-1
CH3OH(g) △H1=-90.5kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.1kJ·mol-1
CO2(g)+H2(g) △H2=-41.1kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
下列说法正确的是
已知:①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.5kJ·mol-1
CH3OH(g) △H1=-90.5kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.1kJ·mol-1
CO2(g)+H2(g) △H2=-41.1kJ·mol-1③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
下列说法正确的是
| A.若温度不变,反应①中生成1molCH3OH(l)时,放出的热量大于90.5kJ |
| B.对于②反应,选用高效催化剂,可降低反应的焓变 |
C.CO2与H2合成甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.4kJ·mol-1 CH3OH(g)+H2O(g) △H=-49.4kJ·mol-1 |
| D.以CO2和H2O为原料合成甲醇,同时生成O2,该反应放出能量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】计算机模拟催化剂表面发生反应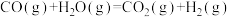 过程中能量的变化如下图。
过程中能量的变化如下图。


下列说法错误的是
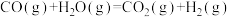 过程中能量的变化如下图。
过程中能量的变化如下图。

下列说法错误的是
| A.过程Ⅰ、Ⅱ均需要吸收能量 | B.过程Ⅲ有极性键和非极性键形成 |
C.由图可知 比CO稳定 比CO稳定 | D.催化剂改变了反应历程,降低反应热 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】已知:① 中的化学键断裂时需要吸收
中的化学键断裂时需要吸收 的能量;②
的能量;② 中的化学键断裂时需要吸收
中的化学键断裂时需要吸收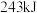 的能量;③由
的能量;③由 和
和 形成
形成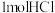 时释放
时释放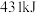 的能量。下列叙述正确的是
的能量。下列叙述正确的是
 中的化学键断裂时需要吸收
中的化学键断裂时需要吸收 的能量;②
的能量;② 中的化学键断裂时需要吸收
中的化学键断裂时需要吸收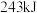 的能量;③由
的能量;③由 和
和 形成
形成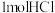 时释放
时释放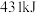 的能量。下列叙述正确的是
的能量。下列叙述正确的是A.氢气和氯气反应生成 氯化氢气体,反应的 氯化氢气体,反应的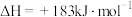 |
B.氢气和氯气反应生成 氯化氢气体,反应的 氯化氢气体,反应的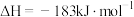 |
C.氢气和氯气反应生成 氯化氢气体,反应的 氯化氢气体,反应的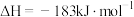 |
D. 和 和 的总能量比 的总能量比 的总能量高 的总能量高 |
您最近一年使用:0次
【推荐2】已知: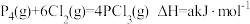 ,
,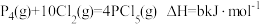 已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为
已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为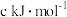 ,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
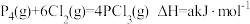 ,
,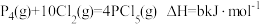 已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为
已知P4具有六键的正四面体结构,经测定PCl5中P-Cl与PCl3中的P-Cl键能不同。PCl5中P-Cl键的键能为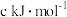 ,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是
,而PCl3中P-Cl键的键能为1.2c kJ/mol,下列叙述正确的是| A.P-P键的键能大于P-Cl键的键能 |
B.可求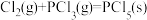 的反应热△H 的反应热△H |
C.P-P键的键能为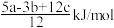 |
D.Cl-Cl键的键能为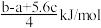 |
您最近一年使用:0次

 的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是
的氯化、溴化反应势能图及产物选择性如下图,下列叙述错误的是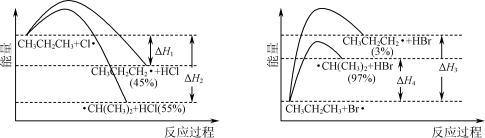
 比伯氢
比伯氢 活性强
活性强 反应速率加快、与
反应速率加快、与 反应速率减慢
反应速率减慢 和
和 的键能差=△H1-△H3
的键能差=△H1-△H3

