常温下,过量块状铁与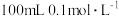 稀硫酸反应,下列方法中,一定能加快反应速率且不改变
稀硫酸反应,下列方法中,一定能加快反应速率且不改变 的产量的是
的产量的是
①通入适量 气体 ②加少量
气体 ②加少量 固体 ③加
固体 ③加 固体 ④适当升高温度 ⑤将块状铁改为铁粉 ⑥将稀硫酸改用98%的浓硫酸
固体 ④适当升高温度 ⑤将块状铁改为铁粉 ⑥将稀硫酸改用98%的浓硫酸
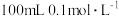 稀硫酸反应,下列方法中,一定能加快反应速率且不改变
稀硫酸反应,下列方法中,一定能加快反应速率且不改变 的产量的是
的产量的是①通入适量
 气体 ②加少量
气体 ②加少量 固体 ③加
固体 ③加 固体 ④适当升高温度 ⑤将块状铁改为铁粉 ⑥将稀硫酸改用98%的浓硫酸
固体 ④适当升高温度 ⑤将块状铁改为铁粉 ⑥将稀硫酸改用98%的浓硫酸| A.①②④ | B.②④⑤ | C.④⑤⑥ | D.④⑤ |
更新时间:2022-04-23 18:45:38
|
【知识点】 影响化学反应速率的外因
相似题推荐
单选题
|
较易
(0.85)
【推荐1】碳是生命的核心元素,碳及其化合物在工农业生产中有着广泛的应用。工业上用CO2生产CH3OH燃料,其热化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列有关说法正确的是
CH3OH(g)+H2O(g),下列有关说法正确的是
 CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。燃煤燃烧时生成的CO2用氨的饱和NaCl溶液吸收,可得到NaHCO3等化工产品。CO2会引起温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO2实现“零排放”。对于反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列有关说法正确的是
CH3OH(g)+H2O(g),下列有关说法正确的是A.增大 的值,可提高H2的转化率 的值,可提高H2的转化率 |
| B.升高温度能提高CO2的反应速率和转化率 |
C.达平衡时缩小容器体积, (正)增大, (正)增大, (逆)减小 (逆)减小 |
| D.1molCO2和3molH2充分反应时放出的热量为49.0kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】升高温度反应速度加快的主要原因是
| A.分子运动速度加快 | B.活化能增加 |
| C.体系能量增加 | D.活化分子的百分数增加 |
您最近一年使用:0次

 2HI(g),增大压强,反应速率加快
2HI(g),增大压强,反应速率加快

