《环境科学》刊发了我国科研部门采用零价铁活化过二硫酸钠(Na2S2O8) 去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。下列叙述不正确的是
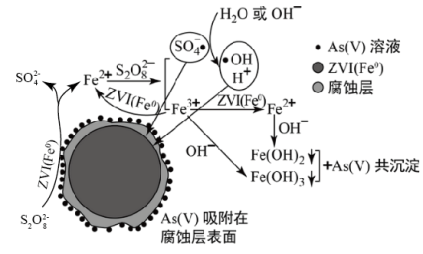

A.56gFe参加反应,消耗的S2O 大于1 mol 大于1 mol |
| B.过二硫酸钠(Na2S2O8) 中S的化合价为+6 |
| C.pH越大,越有利于去除废水中的正五价砷 |
D.碱性条件下,硫酸根自由基发生反应的方程式为:  +H2O= SO +H2O= SO + + +H+ +H+ |
2022·湖南衡阳·二模 查看更多[3]
湖南省百校联考(衡阳市二模)2022届髙三化学试题(已下线)2022年湖南卷高考真题变式题(1-10)(已下线)专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2022-04-29 11:37:40
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】有下列三个在溶液中发生的氧化还原反应:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后下列不正确的是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后下列不正确的是
| A.Fe2+、I-、Cl-、Cr3+的还原性由强到弱依次是I->Fe2+>Cl->Cr3+ |
| B.③反应中HCl的作用有还原性和酸性,氧化剂和起还原剂作用的HCl的数目之比1:6 |
| C.向FeI2溶液中通入一定量Cl2反应的离子方程式可能为2Fe2++2I-+2Cl2=I2+4Cl-+2Fe3+ |
D.常用NaHSO3将酸性废液中的 还原成Cr3+,反应的离子方程式为 还原成Cr3+,反应的离子方程式为 +3 +3 +5H+=2Cr3++3 +5H+=2Cr3++3 +4H2O +4H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列反应的离子方程式书写正确的是
| A.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| B.金属铝溶于氢氧化钠溶液 Al+2OH-=AlO2-+H2↑ |
| C.金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ |
| D.磁性氧化铁跟稀硫酸反应:Fe3O4+8H+=3Fe3++4H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】下列A~D四组反应中,其中I和II可用同一个离子方程式表示的是
| I | II | |
| A | Ca(OH)2溶液中加入足量的NaHCO3溶液 | Ca(HCO3)2溶液中加入足量的NaOH溶液 |
| B | NaHSO4溶液Ba(OH)2溶液反应恰好呈中性 | NaHSO4溶液Ba(OH)2溶液反应使 恰好沉淀 恰好沉淀 |
| C | 将3molCl2通入含1molFeBr2的溶液 | 将1molCl2通入含3molFeBr2的溶液 |
| D | 把金属铁放入稀硫酸中 | 把金属铁放入稀硝酸中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】往含有H+、Fe2+、Cu2+、Ag+四种离子的溶液中加入足量镁粉,最先得到的还原产物是
| A.H2 | B.Fe | C.Cu | D.Ag |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某离子反应涉及到 H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法不正确 的是
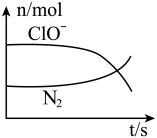

| A.该反应中Cl-为还原产物 |
| B.氧化剂与还原剂物质的量比为3:2 |
| C.消耗1 mol还原剂,转移6 mol电子 |
| D.氧化性:ClO-比 N2强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】向含有1molHNO3和1molH2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断不正确的是
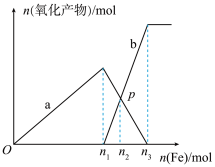

| A.a是表示Fe3+的关系曲线 |
| B.P点时,n(Fe2+)=0.60mol |
| C.n1=0.75 |
| D.向P点溶液加入铜粉,最多可溶解14.4g |
您最近一年使用:0次
【推荐2】足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是
| A.此反应过程中转移了0.5mol的电子 | B.消耗氧气的体积为1.12L(标准状况) |
| C.参加反应的HNO3是0.4mol | D.混合气体中含2.24L(标准状况)NO |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】工业上用Fe2(SO4)3酸性溶液处理SO2废气的工艺流程如下,下列说法不正确的是
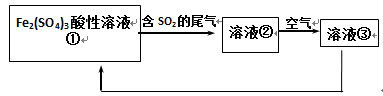
| A.溶液的pH:①>②>③ |
| B.整个过程中Fe2(SO4)3溶液可以循环利用 |
| C.溶液②转化为溶液③发生反应的离子方程式为4H++4Fe2++O2=4Fe3++2H2O |
| D.向②溶液中滴加KSCN溶液,溶液可能变为血红色 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】为探究某些硫的含氧酸盐的部分性质,进行如下实验,并记录实验现象:
①测得0.01mol·L-1NaHSO3溶液的pH约为5。
②向0.01mol·L-1NaHSO3溶液中滴加少量酸性KMnO4溶液,溶液的紫红色褪去。
③向0.1mol·L-1Na2S2O3溶液中滴加稀盐酸,产生无色刺激性气味的气体,且出现淡黄色沉淀。
④在Ag+催化条件下,向0.1mol·L-1K2S2O8无色溶液中滴加MnSO4溶液,溶液变为紫红色。
由上述实验现象得出的结论不合理是
①测得0.01mol·L-1NaHSO3溶液的pH约为5。
②向0.01mol·L-1NaHSO3溶液中滴加少量酸性KMnO4溶液,溶液的紫红色褪去。
③向0.1mol·L-1Na2S2O3溶液中滴加稀盐酸,产生无色刺激性气味的气体,且出现淡黄色沉淀。
④在Ag+催化条件下,向0.1mol·L-1K2S2O8无色溶液中滴加MnSO4溶液,溶液变为紫红色。
由上述实验现象得出的结论不合理是
| A.实验①说明:Ka1(H2SO3)·Ka2(H2SO3)<Kw |
B.实验②中发生反应:5HSO +2MnO +2MnO +H+=5SO +H+=5SO +2Mn2++3H2O +2Mn2++3H2O |
| C.实验③中的淡黄色沉淀为S,无色刺激性气味的气体为SO2 |
D.实验④说明:该条件下,S2O 的氧化性强于MnO 的氧化性强于MnO |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
 MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是| A.若产物为NaClO、NaCl,则吸收后的溶液中n(ClO-)=n(Cl-) |
| B.若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5 |
| C.若产物为NaClO、NaClO3、NaCl,则由吸收后的溶液中n(Cl-)和n(ClO-)可计算吸收的n(Cl2) |
| D.若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1 |
您最近一年使用:0次




