X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如表:
(1)元素X的原子中能量最高的电子其电子云在空间有____ 方向;它的氢化物的电子式是____ 。
(2)元素Y位于元素周期表的位置为____ 。
(3)W的基态原子核外电子排布式是____ 。
(4)元素Y与元素Z相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ 。
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且最高能级是半充满状态 |
| Y | 第三周期元素,它的单质是良好的半导体材料 |
| Z | Z和Y同周期,Z是本周期原子半径最小的主族元素 |
| W | W的一种核素的质量数为63,中子数为34 |
(1)元素X的原子中能量最高的电子其电子云在空间有
(2)元素Y位于元素周期表的位置为
(3)W的基态原子核外电子排布式是
(4)元素Y与元素Z相比,非金属性较强的是
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
更新时间:2022-05-06 12:02:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W、R为原子序数依次增大的前20号主族元素,且分属于四个周期。Y的最外层电子数是电子层数的3倍,Z、W为同周期相邻元素,Y、W可形成如图所示的离子,R原子核外无未成对电子。回答下列问题:
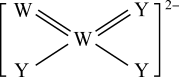
(1)画出W的原子结构示意图____ ,第六周期与W同族元素的原子序数为____ 。
(2)Z、W、R简单离子的半径由大到小顺序为____ (用离子符号表示)。
(3)Z与W的最高价氧化物对应的水化物酸性较强的是____ (写化学式),Z与W形成的简单气态氢化物还原性较强的是____ (写化学式)。
(4)用电子式表示X与R组成的物质的形成过程____ 。
(5)Y、W的简单氢化物沸点较高的是____ (填化学式),判断依据是____ 。
(6)图中离子能与稀硫酸反应,产生淡黄色沉淀和刺激性气味的气体,试写出该反应的离子方程式_____ 。

(1)画出W的原子结构示意图
(2)Z、W、R简单离子的半径由大到小顺序为
(3)Z与W的最高价氧化物对应的水化物酸性较强的是
(4)用电子式表示X与R组成的物质的形成过程
(5)Y、W的简单氢化物沸点较高的是
(6)图中离子能与稀硫酸反应,产生淡黄色沉淀和刺激性气味的气体,试写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答问题:
(1)②的最高价氧化物的结构式为_______ 。
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:_______ 。
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是_______ (填化学式,用“>”连接)。
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式_______ 。
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
(6)元素周期表中,某些主族元素与右下方的主族元素的性质具有相似性,如Be与Al,这种规律称为“对角线原则”。Be(OH)2与NaOH溶液反应的离子方程式为_______ 。
族 周期 | IA | 0 | |||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ② | ③ | ④ | ⑤ | |||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)④⑥元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:
(3)⑤和⑨的简单氢化物的稳定性强弱顺序是
(4)写出⑨的单质与⑥的最高价氧化物对应的水化物反应的离子方程式
(5)硒(Se)被誉为“生命元素”,科学补硒可以减少疾病的发生。Se是第四周期与④同主族的元素,下列推断正确的是_______(填字母)。
| A.SeO2具有还原性 | B.Se的最低负化合价为-1 |
| C.H2SeO3的酸性强于H2SO4 | D. SeO2在一定条件下可与NaOH溶液反应 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y,Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示 的形成过程:
的形成过程:____________________ 。
(2)W在周期表中的位置是____________________ 。
(3)ZYX的电子式为__________ , 中含有的化学键类型为
中含有的化学键类型为__________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是____________________ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是__________ (填字母)。
a.简单阴离子的还原性:Q>R b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R d.Q的单质能从 溶液中置换出R单质
溶液中置换出R单质
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是_______________________________ 。
(7)35号元素溴(Br)和Q位于同一主族,被称为“海洋元素”,高溴酸( )的酸性比
)的酸性比
_______ (填“强”或“弱”),请从位—构—性角度分析原因____________________________ 。
(1)用电子式表示
 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R d.Q的单质能从
 溶液中置换出R单质
溶液中置换出R单质(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(7)35号元素溴(Br)和Q位于同一主族,被称为“海洋元素”,高溴酸(
 )的酸性比
)的酸性比
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为含有22个电子的分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。人体缺E元素会得软骨病,D与E位于同主族。请根据以上情况,回答下列问题:(A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C非金属性由强到弱的顺序为_______ 。
(2)B的氢化物的分子式是_______ ,B的氢化物溶于水的电离方程式为_______ 。
(3)写出化合物AC2的电子式:_______ ,它是_______ (填“极性”或“非极性”)键形成的分子。
(4)E的某常见化合物,它的溶解度随温度升高而降低,它可用于实验室和另一种铵盐制取氨气, 该铵盐的电子式为_______ ,该反应的化学方程式为_______ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,生成B所对应的单质,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(1)A、B、C非金属性由强到弱的顺序为
(2)B的氢化物的分子式是
(3)写出化合物AC2的电子式:
(4)E的某常见化合物,它的溶解度随温度升高而降低,它可用于实验室和另一种铵盐制取氨气, 该铵盐的电子式为
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,生成B所对应的单质,该反应中氧化剂与还原剂的物质的量之比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
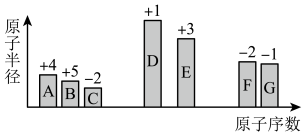
【推荐2】元素周期律和周期表有力地论证了事物变化中量变引起质变的规律性,以及结构决定性质的化学观念。随着原子序数的递增,七种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示,请回答下列问题:___________ 。
(2)C、D、E、G四种元素对应的简单离子半径由大到小的顺序为___________ (用元素的离子符号表示)。
(3)用电子式表示元素D与F形成化合物的过程___________ 。
(4)元素A与C形成的电子总数为22的分子的结构式为___________ 。
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为___________ 。
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为___________ 。
(7)下列有关物质性质的推断,正确的是___________ (填标号)。
a.单质的氧化性: b.金属性:
b.金属性:
c.气态氢化物的稳定性: d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
(2)C、D、E、G四种元素对应的简单离子半径由大到小的顺序为
(3)用电子式表示元素D与F形成化合物的过程
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)D的最高价氧化物的水化物与E的最高价氧化物反应的离子方程式为
(6)元素C与D按原子个数比1∶1形成的化合物所含的所有化学类型为
(7)下列有关物质性质的推断,正确的是
a.单质的氧化性:
 b.金属性:
b.金属性:
c.气态氢化物的稳定性:
 d.最高价氧化物的水化物酸性:
d.最高价氧化物的水化物酸性:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】化合物X是一种维生素,对维持人体基本机能具有重要作用。化合物X由元素A、D、E、G、M、Q组成,它们是原子序数依次增大的前四周期元素,相关信息如下:
(1)A的元素符号为___________ 。
(2)D在元素周期表中的位置为___________ 。
(3)第一电离能:E>G,从基态原子的核外电子排布角度解释原因:___________ 。
(4)E、M的最高价氧化物对应的水化物的酸性:E___________ M(填“>”或“<”),并从元素周期律角度解释原因:___________ 。
(5)Q处于元素周期表中的___________ 区(填“s”“p”“d”或“ds”),基态Q3+的价电子排布式为___________ 。
| 元素 | 信息 |
| A | 核外电子只有一种自旋取向 |
| D | 基态原子价电子排布式为nsnnpn |
| E | 基态原子中的未成对电子数是同周期中最多的 |
| G | 基态原子有8个不同运动状态的电子 |
| M | 与E互为同主族元素 |
| Q | 在化合物X中呈+3价,Q3+与Fe2+具有相同的核外电子排布 |
(2)D在元素周期表中的位置为
(3)第一电离能:E>G,从基态原子的核外电子排布角度解释原因:
(4)E、M的最高价氧化物对应的水化物的酸性:E
(5)Q处于元素周期表中的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D、E、F六种元素,试按下述所给的条件推断:①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;②D、E是周期表中位置相邻的非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;③F是除氢外原子半径最小的主族元素。
(1)A元素的名称___ ,B元素在周期表中的位置为___ ,C元素的离子结构示意图_____ 。
(2)E元素的单质颜色_____ 。
(3)在上述六种元素最高价氧化物对应的水化物中,碱性最强的化学式______ ,酸性最强的化学式____ ,气态氢化物最稳定的化学式______ 。
(4)A、C元素最高价氧化物对应的水化物反应的离子方程式_______ 。
(5)用电子式表示A元素与D元素形成化合物的过程___________ 。
(6)F元素的单质与水反应的化学方程式__________ 。
(1)A元素的名称
(2)E元素的单质颜色
(3)在上述六种元素最高价氧化物对应的水化物中,碱性最强的化学式
(4)A、C元素最高价氧化物对应的水化物反应的离子方程式
(5)用电子式表示A元素与D元素形成化合物的过程
(6)F元素的单质与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2两种离子化合物。
(1)写出Y2O和Y2O2的电子式:_______________________ 、________________________ ,其中后者含有的化学键是______________ (填“离子键”、“极性键”或“非极性键”);
(2)XH3、H2Z和HW三种化合物,沸点最高的是____________ (填化学式);
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是_________ (填化学式);
(4)用电子式表示Y2O的形成过程______________________________________________ 。
(1)写出Y2O和Y2O2的电子式:
(2)XH3、H2Z和HW三种化合物,沸点最高的是
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)用电子式表示Y2O的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】a、b、c、d、e、f、g为七种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c__________ ;②d__________ ;③e__________ ;④a__________ 。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:__________ >__________ (用化学式表示)。
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:________________ 。

其中b的离子半径大于e的离子半径;d是由极性键构成的四原子分子;试写出:
(1)写出下列粒子的电子式:
①c
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:
(3)用电子式表示b元素与氧形成的化合物b2O的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】I.按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:Mg(OH)2___________ ,NH3___________ ,Na2O2___________ 。
(3)用电子式表示下列化合物的形成过程:Na2S___________ ;CO2___________ 。
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是___________ (填化学式)。
(2)10种元素中,简单离子半径最大的是___________ 填离子符号)。
(3)元素⑦的简单氢化物与过量的元素⑧的单质反应的化学方程式为___________ 。
(4)元素⑩的原子序数为___________ ,其单质与水在高温下反应的化学方程式为___________ 。
(5)元素①⑦⑧形成的常见化合物的化学式___________ ,含有化学键类型___________ 、___________ 。
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:Mg(OH)2
(3)用电子式表示下列化合物的形成过程:Na2S
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
| ① | |||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
| ② | ④ | ⑤ | ⑧ | ||||||||||||||
| ③ | ⑩ | ||||||||||||||||
| ⑨ |
(2)10种元素中,简单离子半径最大的是
(3)元素⑦的简单氢化物与过量的元素⑧的单质反应的化学方程式为
(4)元素⑩的原子序数为
(5)元素①⑦⑧形成的常见化合物的化学式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】百余种不同的元素,构成了大千世界中所有物质。科学家们根据元素的性质递变规律、电子排布规律等对元素进行编排设计元素周期表。
(1)地壳中含量最多的元素的基态原子的轨道表示式_____ ,能量最高的电子所在的轨道呈_____ 形。
(2)研究发现,正离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是_____ 。
(3)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
预测X值的区间:_____ ;上表中五种元素的第一电离能由大到小的顺序是_____ (写元素符号)。
(4)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。Li位于周期表中_____ 区;基态Ti原子的价电子排布式为_____ ;基态Fe3+、Fe2+离子中未成对的电子数之比为_____ 。
(5)单质Sn与干燥的Cl2反应生成SnCl4,常温常压下SnCl4为无色液体,SnCl4空间构型为_____ ,其固体的晶体类型为_____ 。
(6)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24.下列有关叙述错误的是_____。
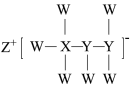
(7)1962年首个稀有气体化合物XePtF6问世,目前已知的稀有气体化合物中,含氙(54Xe)的最多,氪(36Kr)次之,氩(18Ar)极少。XeF2室温下易升华,其中心原子的价层电子对数为_____ 。[BrOF2][AsF6]•xKrF2是[BrOF2]+、[AsF6]﹣与KrF2分子形成的加合物,你认为[BrOF2][AsF6]•xKrF2晶体中的化学键类型有_____
(1)地壳中含量最多的元素的基态原子的轨道表示式
(2)研究发现,正离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是
(3)随着科技的不断发展,人类对原子结构的认识不断深入,新型材料层出不穷。下表中列出了第三周期的几种元素的部分性质:
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 | ﹣1,+7 | ﹣2,+6 | ﹣3,+5 | +3 | +1 |
(4)Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂、钛酸锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。Li位于周期表中
(5)单质Sn与干燥的Cl2反应生成SnCl4,常温常压下SnCl4为无色液体,SnCl4空间构型为
(6)一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24.下列有关叙述错误的是_____。
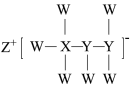
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.Y的最高化合价氧化物的水化物为强酸 |
| D.X的氟化物XF3中原子均为8电子稳定结构 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D四种短周期元素,A元素原子的外围电子排布式为2s22p2;B元素与A元素位于同一周期,其原子的原子核外有三个未成对电子;C元素位于第2周期,电负性仅次于氟;D元素在短周期元素中第一电离能最小。
(1)A、B、C、D四种元素分别是_______ 。
(2)A的最高价氧化物的电子式是_______ 。
(3)A、B、C、D四种元素电负性由大到小的顺序是_______ 。
(4)B、C两种元素气态氢化物的稳定性大小的顺序是_______ 。
(1)A、B、C、D四种元素分别是
(2)A的最高价氧化物的电子式是
(3)A、B、C、D四种元素电负性由大到小的顺序是
(4)B、C两种元素气态氢化物的稳定性大小的顺序是
您最近一年使用:0次



