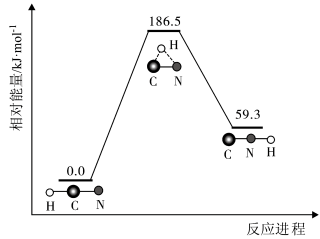
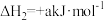理论研究表明,在101kPa和298K下,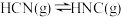 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
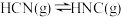 异构化反应过程的能量变化如图所示。下列说法错误的是
异构化反应过程的能量变化如图所示。下列说法错误的是
| A.HCN为直线型分子 |
| B.升高温度,该异构化反应正向移动 |
| C.正反应的活化能大于逆反应的活化能 |
D.使用催化剂,能加快化学反应速率,反应的 减小 减小 |
更新时间:2022-05-04 07:13:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】参照反应Br+H2→HBr+H的能量—反应历程的示意图,下列叙述中正确的是( )


| A.正反应为放热反应 |
| B.加入催化剂,该化学反应的反应热不变 |
| C.反应物总能量高于生成物总能量 |
| D.升高温度可增大正反应速率,降低逆反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知: (g) ⇌
(g) ⇌  (g) ΔH>0.下列说法正确的是
(g) ΔH>0.下列说法正确的是
 (g) ⇌
(g) ⇌  (g) ΔH>0.下列说法正确的是
(g) ΔH>0.下列说法正确的是| A.表示丁烯燃烧热的热化学方程式为C4H8(g) + 6O2(g)=4CO2(g) + 4H2O(g) ΔH=Q kJ·mol-1(Q<0) |
| B.该反应正反应的活化能小于逆反应的活化能 |
| C.反-2-丁烯燃烧热的数值更大 |
| D.稳定性:反-2-丁烯>顺-2-丁烯 |
您最近一年使用:0次
【推荐3】苯与卤素发生取代反应可细分为:
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
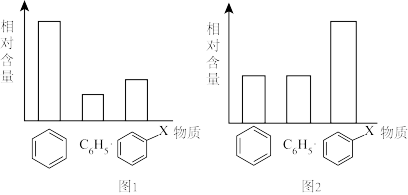
下列说法正确的是
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。

X | Cl | Br |
△H1(kJ∙mol-1) | 10 | 20 |
△H2(kJ∙mol-1) | -111 | -100 |
| A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1 |
| B.1mol苯与1mol氯气反应将会向环境释放101kJ热量 |
| C.使用催化剂后会改变△H1,但不会改变△H1+△H2 |
| D.反应②为总反应的决速步,催化剂的机理为降低反应②的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】通过CO变换可以获得更多的氢气,其反应方程式为:  ,当前CO变换过程有多种工艺,其中Cu催化CO变换几种可能的机理及各基元反应的活化能(Ea/eV)如图所示,下列说法正确的是
,当前CO变换过程有多种工艺,其中Cu催化CO变换几种可能的机理及各基元反应的活化能(Ea/eV)如图所示,下列说法正确的是

 ,当前CO变换过程有多种工艺,其中Cu催化CO变换几种可能的机理及各基元反应的活化能(Ea/eV)如图所示,下列说法正确的是
,当前CO变换过程有多种工艺,其中Cu催化CO变换几种可能的机理及各基元反应的活化能(Ea/eV)如图所示,下列说法正确的是
| A.从整个反应历程上看,线路(1)的反应机理在能量上最不利,不易进行 |
B.由图知H—H的键能是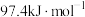 |
| C.上图各路线总反应的活化能及反应热均相同 |
D.路线(3)的历程中决定整个反应速率的步骤是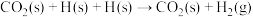 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是 ( )
| A.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量 |
| B.任何放热反应在常温条件下一定能发生反应 |
| C.形成生成物化学键释放的能量大于破坏反应物化学键所吸收的能量时,反应为吸热反应 |
| D.等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于敞口容器中的化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的是( )
| A.锌不能用来表示该反应的速率,其它反应物和生成物都能用来表示该反应的速率 |
B.反应过程中能量关系可用下图表示 |
| C.若将该反应设计成原电池,锌为负极 |
| D.若将其设计为原电池,当有32.5g锌溶解时,正极放出标况下11.2L气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学反应中的能量变化符合下图所示的是
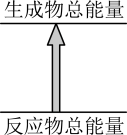

| A.甲烷燃烧 | B.碳酸钙高温分解 |
| C.钠与水反应 | D.酸碱中和 |
您最近一年使用:0次


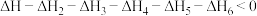
 比HBr的小
比HBr的小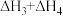 )比HI的大
)比HI的大