苯与卤素发生取代反应可细分为:
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。
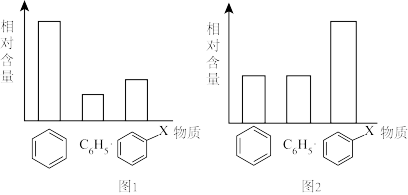
下列说法正确的是
①C6H6(苯)+∙X+X2→C6H5∙+X2+HX △H1
②C6H5∙+X2+HX→C6H5X+HX+∙X △H2
下图1、2表示反应中部分物质的含量(测量反应过程中多个时间点的各物质含量,去除开始时与结束前的极端值后取平均值),已知图1为使用催化剂前,图2为使用催化剂后,下表为相关△H的数据。

X | Cl | Br |
△H1(kJ∙mol-1) | 10 | 20 |
△H2(kJ∙mol-1) | -111 | -100 |
| A.可推知H-Cl键的键能比H-Br键的键能大10 kJ∙mol-1 |
| B.1mol苯与1mol氯气反应将会向环境释放101kJ热量 |
| C.使用催化剂后会改变△H1,但不会改变△H1+△H2 |
| D.反应②为总反应的决速步,催化剂的机理为降低反应②的活化能 |
2022·浙江·模拟预测 查看更多[5]
浙江省普通高校招生2022-2023学年高三上学期10月化学(选考)模拟试题(已下线)热点情景汇编-专题六 化学反应中的热能(已下线)素养卷03 化学反应与能量变化图象-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)浙江七彩阳光联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2022-11-10 11:32:35
|
相似题推荐
【推荐1】高温条件下C40H20生成C40H18的反应历程和相对能量变化如图所示:
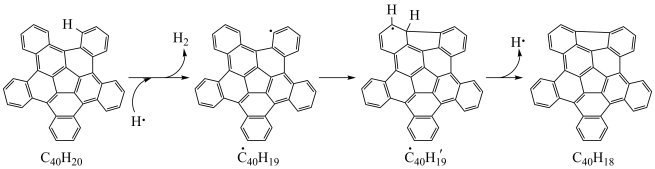
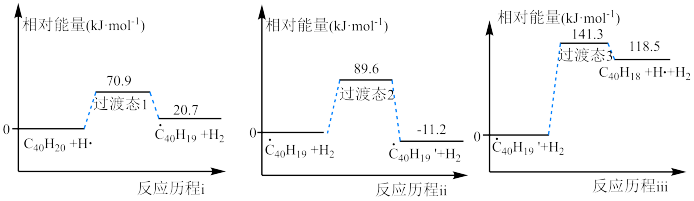
| A.三步反应历程中决定总反应速率的是反应历程ⅲ |
B.ⅰ、ⅱ、ⅲ三步的总反应为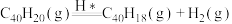  kJ⋅mol kJ⋅mol |
| C.根据图像可以判断过渡状态1、2、3的稳定性相对高低 |
| D. C40H18形成的过程中有极性键的断裂和形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
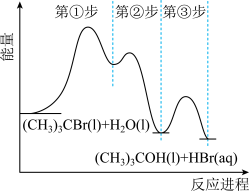
【推荐2】反应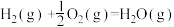 的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是

①c代表总反应放出的能量,为121kJ
②b代表新的化学键形成吸收的能量,为463kJ
③氢气中1molH-H键断裂时吸收热量为436kJ
④此反应为放热反应,所以无需加热就能进行
⑤NH4Cl晶体与Ba(OH)2·8H2O晶体混合搅拌与此反应的ΔH都<0
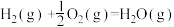 的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
的能量变化如图所示。已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出热量463kJ。以下说法错误的是
①c代表总反应放出的能量,为121kJ
②b代表新的化学键形成吸收的能量,为463kJ
③氢气中1molH-H键断裂时吸收热量为436kJ
④此反应为放热反应,所以无需加热就能进行
⑤NH4Cl晶体与Ba(OH)2·8H2O晶体混合搅拌与此反应的ΔH都<0
| A.①③④⑤ | B.②③④ | C.①②④⑤ | D.全部 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】最近,各国科学家联合成功研制的一种新型催化剂,可在常压下将二氧化碳与氢气的混合气体转化为甲烷。在容积为VL的容器中进行该转化,相关情况如图所示。下列有关说法不正确的是
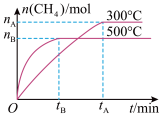

A.101KPa、120℃时,该反应的平衡常数表达式为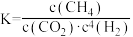 |
| B.断裂1molC=O键、2molH—H键所吸收的能量小于形成2molC—H键、2molO—H键所释放的能量 |
C.300℃时,从反应开始到达到平衡的这段时间,平均反应速率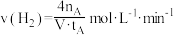 |
| D.其他条件不变,缩小容器容积,二氧化碳的平衡转化率增大,平衡常数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 与
与 重整生成
重整生成 和CO的过程中主要发生下列反应:
和CO的过程中主要发生下列反应:
CH4(g)+CO2(g)=2H2(g)+2CO(g) ∆H =+247.1kJ /mol;
H2(g)+CO2(g)=H2O(g)+CO(g) ∆H =+41.2kJ /mol
在恒压、反应物起始物质的量比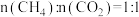 条件下,
条件下, 和
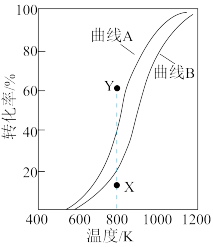
和 的平衡转化率随温度变化的曲线如图所示。下列说法不正确的是
的平衡转化率随温度变化的曲线如图所示。下列说法不正确的是
 与
与 重整生成
重整生成 和CO的过程中主要发生下列反应:
和CO的过程中主要发生下列反应:CH4(g)+CO2(g)=2H2(g)+2CO(g) ∆H =+247.1kJ /mol;
H2(g)+CO2(g)=H2O(g)+CO(g) ∆H =+41.2kJ /mol
在恒压、反应物起始物质的量比
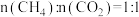 条件下,
条件下, 和
和 的平衡转化率随温度变化的曲线如图所示。下列说法不正确的是
的平衡转化率随温度变化的曲线如图所示。下列说法不正确的是
A.曲线A表示 的平衡转化率随温度的变化 的平衡转化率随温度的变化 |
| B.3CO2(g)+CH4(g)=2 H2O(g)+4CO(g) ∆H =+329.5kJ/mol |
C.升高温度、减小压强均有利于提高 的平衡转化率 的平衡转化率 |
D.恒压、800K、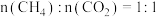 条件下,可通过改变 条件下,可通过改变 的量或使用高效催化剂等特定条件继续反应,使 的量或使用高效催化剂等特定条件继续反应,使 转化率从X点变为Y点 转化率从X点变为Y点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】恒温恒容条件下,对于反应
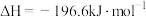 ,能量变化如图所示。下列说法中不正确的是
,能量变化如图所示。下列说法中不正确的是
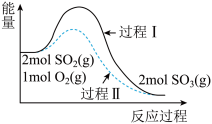

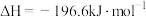 ,能量变化如图所示。下列说法中不正确的是
,能量变化如图所示。下列说法中不正确的是
A.由题意可知,反应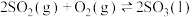 的 的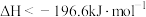 |
B.增大氧气浓度,平衡正向移动,平衡常数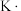 增大 增大 |
| C.与过程I相比,过程II加入了催化剂,增大了活化分子百分数 |
| D.若恒温恒压条件下充入惰性气体,反应速率会降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】水催化氧化机理如图所示。下列叙述错误的是
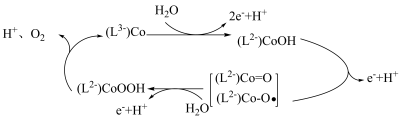
| A.钴位于元素周期表中的d区 |
| B.催化剂能降低反应的活化能,加快反应速率 |
| C.在转化过程中Co的化合价没有发生变化 |
D.该机理总反应式: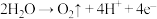 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用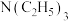 捕获
捕获 并在纳米金催化剂作用下较低温转化为甲酸,为实现“碳达峰、碳中和”提供了新路径,转化过程如图,下列说法错误的是
并在纳米金催化剂作用下较低温转化为甲酸,为实现“碳达峰、碳中和”提供了新路径,转化过程如图,下列说法错误的是
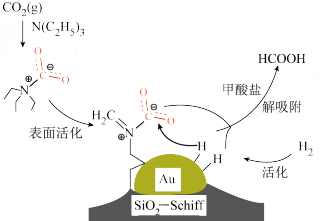
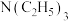 捕获
捕获 并在纳米金催化剂作用下较低温转化为甲酸,为实现“碳达峰、碳中和”提供了新路径,转化过程如图,下列说法错误的是
并在纳米金催化剂作用下较低温转化为甲酸,为实现“碳达峰、碳中和”提供了新路径,转化过程如图,下列说法错误的是
A.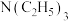 可与HCl反应生成盐 可与HCl反应生成盐 |
B. 加氢合成甲酸,符合绿色化学思想 加氢合成甲酸,符合绿色化学思想 |
C.1mol 完全转化为甲酸,转移电子数为4NA 完全转化为甲酸,转移电子数为4NA |
| D.纳米金催化剂降低了反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
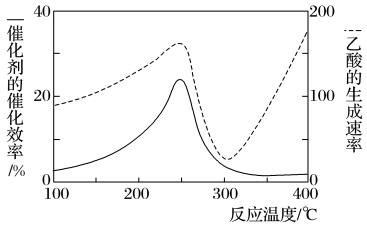
【推荐2】以二氧化钛表面覆盖Cu2Al2O4为催化剂,可将CO2和CH4直接转化成乙酸,如图为反应过程中催化剂的催化效率(实线)与乙酸的生成速率(虚线)随温度的变化情况。下列说法不正确的是

| A.该制备乙酸的反应中,原子利用率为100% |
| B.Cu2Al2O4写成氧化物的形式是Cu2O·Al2O3 |
| C.由图可知,工业上制备乙酸最适宜的温度应为250℃或者400℃ |
| D.250~300℃时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低 |
您最近一年使用:0次


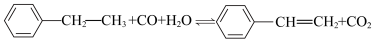

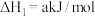

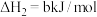
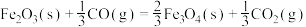
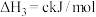
 的
的 (单位:kJ/mol)为
(单位:kJ/mol)为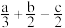
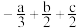
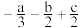
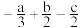


 不能自发进行,则该反应的
不能自发进行,则该反应的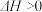
 、
、 、
、 的氧化性依次减弱
的氧化性依次减弱

