A、B、C、D、E是原子序数依次增大并分属四个周期的前20号主族元素。B、C相邻且C原子的最外层电子数是内层电子数的3倍,D、E能形成化合物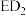 。
。
(1)B在元素周期表中的位置是___________ ,化合物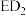 的电子式为
的电子式为___________ 。
(2)A与B、C形成的简单化合物的稳定性相对强弱为___________ (用化学式表示);化合物 中的化学键类型为
中的化学键类型为___________ 。
(3)科学研究发现化合物BC具有“扩张血管和增强免疫力、记忆力”的功能,故它成为当前生命科学研究中的“明星分子”。一定条件下该“明星分子”可转化为化合物B,C与另一种常见的红棕色气体,写出反应的化学方程式:___________ ,同温同体积条件下,该反应完全转化后,容器内反应前后的压强比为___________ 。
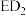 。
。(1)B在元素周期表中的位置是
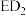 的电子式为
的电子式为(2)A与B、C形成的简单化合物的稳定性相对强弱为
 中的化学键类型为
中的化学键类型为(3)科学研究发现化合物BC具有“扩张血管和增强免疫力、记忆力”的功能,故它成为当前生命科学研究中的“明星分子”。一定条件下该“明星分子”可转化为化合物B,C与另一种常见的红棕色气体,写出反应的化学方程式:
更新时间:2022-05-04 21:19:29
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】有X、Y、Z、M、R、Q六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1)A元素与R在同一主族,A周期序数比R周期序数多4,则A元素的原子序数为_______
(2)根据表中数据推测,Y的原子半径的最小范围是_______
(3)Z、M、R的简单离子的半径由小到大的顺序为_______ (用离子符号表示)
(4)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是_______ (选填字母序号)
A.常温下Y的单质呈固态,R的单质呈气态
B.稳定性: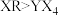
C.Y与R形成的化合物中Y呈正价
D.酸性
(5)写出Y的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式_______
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 |  、 、 |  |  、 、 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)A元素与R在同一主族,A周期序数比R周期序数多4,则A元素的原子序数为
(2)根据表中数据推测,Y的原子半径的最小范围是
(3)Z、M、R的简单离子的半径由小到大的顺序为
(4)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是
A.常温下Y的单质呈固态,R的单质呈气态
B.稳定性:
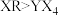
C.Y与R形成的化合物中Y呈正价
D.酸性

(5)写出Y的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下图为周期表的主族元素的一部分,L原子最外层电子数是次外层电子数的一半。
(1)写出M的元素符号:___________ 。
(2)写出R在元素周期表中的位置:___________ 。
(3)最高价氧化物对应水化物的碱性:R___________ (填“>”“<”或“=”,下同)W。
(4)气态氢化物的稳定性:Z___________ X。
(5)R、W、Z的简单离子的半径由大到小的排列顺序是___________ (用元素的离子符号表示)。
(6)下列说法不正确的是___________(填标号)。
| X | Z | ||||
| R | W | L | J | Q | |
| M |
(2)写出R在元素周期表中的位置:
(3)最高价氧化物对应水化物的碱性:R
(4)气态氢化物的稳定性:Z
(5)R、W、Z的简单离子的半径由大到小的排列顺序是
(6)下列说法不正确的是___________(填标号)。
| A.Q、M的最高价氧化物对应的水化物酸性:M<Q |
B.L元素的单质具有半导体的特性,与Z可形成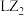 |
| C.W、Z形成的化合物既能与酸反应又能与碱反应 |
| D.M的单质的氧化性大于Q |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是部分短周期元素的常见化合价与原子序数的关系:
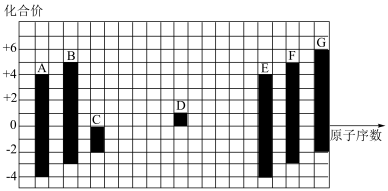
回答下列问题:
(1)E元素为__________ (填元素符号,下同);F元素为__________ 。
(2)C、D、G的离子半径由大到小的顺序是__________ (用元素符号表示)。
(3)最简单氢化物的热稳定性:B__________ (填“>”或“<”)C。
(4)C与D形成的具有强氧化性的化合物为__________ ,该化合物与 反应的化学方程式为
反应的化学方程式为________________________________________ ,其中氧化剂与还原剂的物质的量之比为__________ 。

回答下列问题:
(1)E元素为
(2)C、D、G的离子半径由大到小的顺序是
(3)最简单氢化物的热稳定性:B
(4)C与D形成的具有强氧化性的化合物为
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为元素周期表中前三周期的主族元素,它们的原子序数按A、B、C、D、E的顺序增大。A的最外层电子数是次外层电子数的2倍,C与E最外层电子数相等,E的最高价氧化物中含氧60%,D与C可形成D2C、D2C2两种离子化合物。填写下列空白:
(1)写出上述五种元素的元素符号:A___ ,B___ ,C___ ,D____ ,E___ 。
(2)写出D2C2的电子式_________ ,AC2的结构式___________ 。
(3)用电子式表示 AC2化合物的形成过程__________________ 。
(1)写出上述五种元素的元素符号:A
(2)写出D2C2的电子式
(3)用电子式表示 AC2化合物的形成过程
您最近一年使用:0次
【推荐2】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大,A元素的价层电子排布式为 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)D、C两种元素形成的化合物的电子式为___________ 。
(2)A、B、C三种元素的电负性由小到大的顺序为___________ (用元素符号表示)。
(3)C元素的电子排布图为___________ 。
(4)E元素位于元素周期表的第___________ 族,形成的离子中较稳定的离子的价层电子排布式是___________ 。
(5)F元素位于元素周期表的___________ 区,B元素原子核外占据最高能级的电子云轮廓图是___________ 形。
(6)G可能的性质有___________(填字母)。
 ;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子核外有7个能级且有4个未成对电子;F元素在元素周期表第11列;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)D、C两种元素形成的化合物的电子式为
(2)A、B、C三种元素的电负性由小到大的顺序为
(3)C元素的电子排布图为
(4)E元素位于元素周期表的第
(5)F元素位于元素周期表的
(6)G可能的性质有___________(填字母)。
| A.其最高价氧化物对应水化物是弱酸 | B.其第一电离能小于磷小于硒 |
| C.其原子半径大于锗 | D.氢化物的稳定性G大于A |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】已知 、
、 、
、 、
、 四种元素的核电荷数依次增大,
四种元素的核电荷数依次增大, 原子最外层电子数是次外层电子数的2倍;
原子最外层电子数是次外层电子数的2倍; 元素在地壳中含量最多;
元素在地壳中含量最多; 原子最外层电子数与
原子最外层电子数与 原子最外层电子数相等,且
原子最外层电子数相等,且 原子比
原子比 原子多一个电子层;
原子多一个电子层; 原子与
原子与 原子具有相同的电子层数,且
原子具有相同的电子层数,且 原子内层电子总数比最外层电子数多3。试回答下列问题:
原子内层电子总数比最外层电子数多3。试回答下列问题:
(1)写出四种元素的名称:
____________ ;
____________ ;
____________ ;
____________ 。
(2) 原子的结构示意图为
原子的结构示意图为________________________ 。
(3) 的阴离子的结构示意图为
的阴离子的结构示意图为________________________ 。
 、
、 、
、 、
、 四种元素的核电荷数依次增大,
四种元素的核电荷数依次增大, 原子最外层电子数是次外层电子数的2倍;
原子最外层电子数是次外层电子数的2倍; 元素在地壳中含量最多;
元素在地壳中含量最多; 原子最外层电子数与
原子最外层电子数与 原子最外层电子数相等,且
原子最外层电子数相等,且 原子比
原子比 原子多一个电子层;
原子多一个电子层; 原子与
原子与 原子具有相同的电子层数,且
原子具有相同的电子层数,且 原子内层电子总数比最外层电子数多3。试回答下列问题:
原子内层电子总数比最外层电子数多3。试回答下列问题:(1)写出四种元素的名称:




(2)
 原子的结构示意图为
原子的结构示意图为(3)
 的阴离子的结构示意图为
的阴离子的结构示意图为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。
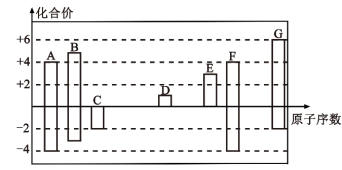
(1)G元素在周期表中的位置为___________ 。
(2)元素A与C形成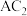 分子的电子式为
分子的电子式为____ ,B元素的单质的结构式为___________ 。
(3)A、B、F三种元素的原子半径由大到小的顺序是____ 。(填元素符号)
(4)D元素最高价氧化物的水化物所含的化学键有___________ (填化学键类型),D元素最高价氧化物的水化物与E元素的最高价氧化物的水化物反应的离子方程式是___________ 。
(5)元素C、G形成的简单气态氢化物中, 与
与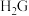 的稳定性较强的是
的稳定性较强的是___________ (填化学式)。
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷( )是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。
)是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。

(1)G元素在周期表中的位置为
(2)元素A与C形成
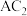 分子的电子式为
分子的电子式为(3)A、B、F三种元素的原子半径由大到小的顺序是
(4)D元素最高价氧化物的水化物所含的化学键有
(5)元素C、G形成的简单气态氢化物中,
 与
与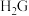 的稳定性较强的是
的稳定性较强的是(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷(
 )是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。
)是37号元素,相对原子质量是85,位于ⅠA族。关于铷的下列说法中不正确的是___________(填序号)。| A.与水反应比钠更剧烈 | B.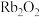 与水能剧烈反应并释放出 与水能剧烈反应并释放出 |
C.单质 具有很强的氧化性 具有很强的氧化性 | D.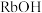 的碱性比同浓度的 的碱性比同浓度的 弱 弱 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】随着原子序数的递增,八种短周期元素(用字母x~h表示)的原子半径相对大小、最高正价或最低负价的变化如图所示。请回答下列问题:
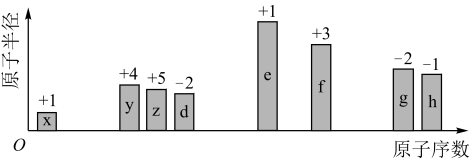
(1)x形成的阴离子的结构示意图为___________ 。
(2)如果1个z原子中含8个中子,则其原子符号为___________ 。
(3)f的最高价氧化物对应水化物和h的最高价氧化物对应的水化物相互反应的离子反应方程式___________ 。
(4)比较d、e常见离子的半径大小:___________ (填离子符号,用“>”连接)。
(5)用电子式表示h的氢化物形成过程___________ 。

(1)x形成的阴离子的结构示意图为
(2)如果1个z原子中含8个中子,则其原子符号为
(3)f的最高价氧化物对应水化物和h的最高价氧化物对应的水化物相互反应的离子反应方程式
(4)比较d、e常见离子的半径大小:
(5)用电子式表示h的氢化物形成过程
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】今有aX、bY、cZ三种元素。已知:①各原子序数a、b、c均小于20,且a+b+c=25; ②元素Y的原子价电子构型为ns2npn+2; ③X和Y在不同条件下可形成X2Y和X2Y2两种化合物,Y和Z在不同条件下可形成ZY和ZY2两种化合物; ④Z的硫化物的相对分子质量与Z氯化物的相对分子质量之比为38︰77。回答下列问题:
(1)X2Y2属于________ 化合物(填“离子”或“共价”),该化合物中化学键类型有:___________________ 。
(2)Z的硫化物的VSEPR模型为_________________ ,分子空间构型为______________ ;Z的氯化物的VSEPR模型和分子空间构型分别是_______________ 、_____________ , Z原子在硫化物、氯化物中分别以 ___________ 杂化轨道成键,根据原子轨道成键方式分,Z的硫化物分子中含有的键的种类及数目是 ________________ 、__________________ 。
(1)X2Y2属于
(2)Z的硫化物的VSEPR模型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。
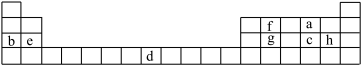
(1)表中字母h元素在周期表中位置___ 。
(2)写出b元素的最高价氧化物对应的水化物所含化学键类型___ 。
(3)下列事实能说明a元素的非金属性比c元素的非金属性强的有___ 。
A.a单质与c的氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mola单质比1molc单质得电子数目多
C.a和c两元素的简单氢化物受热分解,前者的分解温度高
(4)g与h两元素的单质反应生成1molg的最高价化合物。恢复至室温,放热687kJ。已知该化合物的熔、沸点分别为-69℃和58℃。写出该反应的热化学方程式___ 。
(5)常温下d遇浓硫酸形成致密氧化膜,若薄膜为具有磁性的该元素氧化物,写出该反应的化学方程式___ 。
(6)e与f形成的1mol化合物Q与水反应,生成2mol氢氧化物和1mol烃,该烃分子中碳氢质量比为9∶1,写出烃分子电子式___ 。

(1)表中字母h元素在周期表中位置
(2)写出b元素的最高价氧化物对应的水化物所含化学键类型
(3)下列事实能说明a元素的非金属性比c元素的非金属性强的有
A.a单质与c的氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1mola单质比1molc单质得电子数目多
C.a和c两元素的简单氢化物受热分解,前者的分解温度高
(4)g与h两元素的单质反应生成1molg的最高价化合物。恢复至室温,放热687kJ。已知该化合物的熔、沸点分别为-69℃和58℃。写出该反应的热化学方程式
(5)常温下d遇浓硫酸形成致密氧化膜,若薄膜为具有磁性的该元素氧化物,写出该反应的化学方程式
(6)e与f形成的1mol化合物Q与水反应,生成2mol氢氧化物和1mol烃,该烃分子中碳氢质量比为9∶1,写出烃分子电子式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】如图是元素周期表的一部分,请回答下列问题:
(1)g元素在元素周期表中位置为_______ 。
(2)f、h的最高价氧化物对应水化物相互反应的离子方程式为_______ (用元素符号作答,下同)。
(3)用电子式表示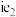 的形成过程
的形成过程_______ 。
(4)a、b、c、d形成的盐中含有的化学键类型为_______ 。
(5)用化学方程式说明d、g的简单氢化物的稳定性强弱的原因_____
| a | |||||||||||||||||
| b | c | d | e | ||||||||||||||
| f | g | ||||||||||||||||
| h | i | j | |||||||||||||||
(2)f、h的最高价氧化物对应水化物相互反应的离子方程式为
(3)用电子式表示
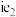 的形成过程
的形成过程(4)a、b、c、d形成的盐中含有的化学键类型为
(5)用化学方程式说明d、g的简单氢化物的稳定性强弱的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素①~⑩在周期表中的位置如表所示:
回答下列问题:
(1)最外层电子数为2的元素有_______ (填元素符号);⑨的简单离子结构示意图为_______ 。
(2)①与④两种元素形成相对分子质量为42的链状化合物的结构简式为_______ ;①、⑤、⑥三种元素形成的一种常见盐的化学式为_______ ,该盐中含有的化学键有_______ 。
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈_______ 色。⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为_______ 。
(4)用电子式表示⑧与⑩形成的化合物的形成过程_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)最外层电子数为2的元素有
(2)①与④两种元素形成相对分子质量为42的链状化合物的结构简式为
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈
(4)用电子式表示⑧与⑩形成的化合物的形成过程
您最近一年使用:0次



