溴、碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→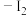 的
的 溶液
溶液
(1)上述实验流程中灼烧用到的仪器是_______ (从下列图中选择,写出名称,下同),萃取分液在_______ 中进行。

(2)“氧化”时加入 和
和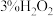 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______ 。
(3)检验氧化后的溶液中存在碘单质,可选用的试剂是_______ (填名称)溶液。
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
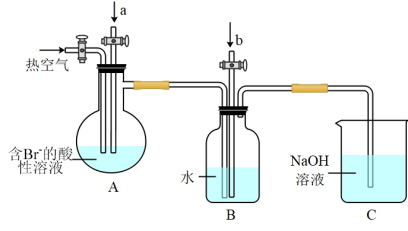
(4)A装置中通入a气体通常为_______ ,发生反应的离子方程式为_______ 。
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是_______ 。
(6)B装置的作用是收集并还原溴,则气体b为_______ 。
(7)C装置的作用是_______ 。
Ⅰ.实验室按如下实验流程提取海带中的碘。
海带→灼烧→溶解→过滤→氧化→萃取、分液→
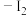 的
的 溶液
溶液(1)上述实验流程中灼烧用到的仪器是

(2)“氧化”时加入
 和
和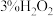 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)检验氧化后的溶液中存在碘单质,可选用的试剂是
Ⅱ.某化学兴趣小组模拟工业上以浓缩海水为原料提取溴的流程设计了如图所示装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。

(4)A装置中通入a气体通常为
(5)A装置中通入a气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
(6)B装置的作用是收集并还原溴,则气体b为
(7)C装置的作用是
更新时间:2022-05-07 08:58:30
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上以浓缩海水为原料提取溴的部分流程如下:
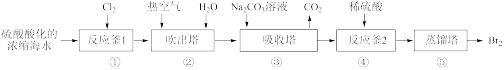
已知:吸收塔中的主要反应为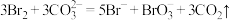 。
。
(1)实验室使用如图所示装置模拟上述流程的①~③。
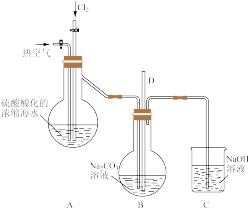
①实验室以浓盐酸和 为原料在加热条件下制取氯气的离子方程式:
为原料在加热条件下制取氯气的离子方程式:_______ 。
②A装置中先通入 一段时间后,再通入热空气。通入热空气的目的是
一段时间后,再通入热空气。通入热空气的目的是_______ 。
③烧瓶B中的长导管D起着平衡压强的作用,当烧瓶内气体压强过大时,可以观察到的现象是_______ 。
(2)向反应釜2中加入稀硫酸,反应釜中原溶液主要减少的离子有_______ 。
(3)蒸馏塔残留液中含有少量 ,可用臭氧氧化技术进行处理,但会产生易致癌的
,可用臭氧氧化技术进行处理,但会产生易致癌的 。取含
。取含 的水样,向其中投加一定量的
的水样,向其中投加一定量的 ,再经
,再经 氧化后,水中溴酸盐
氧化后,水中溴酸盐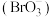 的含量如图所示。投加一定量的
的含量如图所示。投加一定量的 其目的是
其目的是_______ 。

(4)我国废水三级排放标准规定:废水中苯酚的含量不得超过 。实验室可用一定浓度的溴水测定某废水中苯酚的含量。
。实验室可用一定浓度的溴水测定某废水中苯酚的含量。
请完成相应的实验步骤:准确量取25.00mL待测废水于锥形瓶中,_______ ,将实验重复2次,进行数据处理。
(已知: 。实验中需使用的试剂:
。实验中需使用的试剂: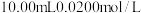 溴水(过量)、
溴水(过量)、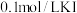 溶液、
溶液、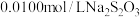 标准溶液、淀粉溶液)
标准溶液、淀粉溶液)

已知:吸收塔中的主要反应为
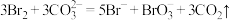 。
。(1)实验室使用如图所示装置模拟上述流程的①~③。

①实验室以浓盐酸和
 为原料在加热条件下制取氯气的离子方程式:
为原料在加热条件下制取氯气的离子方程式:②A装置中先通入
 一段时间后,再通入热空气。通入热空气的目的是
一段时间后,再通入热空气。通入热空气的目的是③烧瓶B中的长导管D起着平衡压强的作用,当烧瓶内气体压强过大时,可以观察到的现象是
(2)向反应釜2中加入稀硫酸,反应釜中原溶液主要减少的离子有
(3)蒸馏塔残留液中含有少量
 ,可用臭氧氧化技术进行处理,但会产生易致癌的
,可用臭氧氧化技术进行处理,但会产生易致癌的 。取含
。取含 的水样,向其中投加一定量的
的水样,向其中投加一定量的 ,再经
,再经 氧化后,水中溴酸盐
氧化后,水中溴酸盐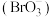 的含量如图所示。投加一定量的
的含量如图所示。投加一定量的 其目的是
其目的是
(4)我国废水三级排放标准规定:废水中苯酚的含量不得超过
 。实验室可用一定浓度的溴水测定某废水中苯酚的含量。
。实验室可用一定浓度的溴水测定某废水中苯酚的含量。请完成相应的实验步骤:准确量取25.00mL待测废水于锥形瓶中,
(已知:
 。实验中需使用的试剂:
。实验中需使用的试剂: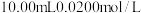 溴水(过量)、
溴水(过量)、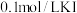 溶液、
溶液、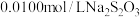 标准溶液、淀粉溶液)
标准溶液、淀粉溶液)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组在实验室以卤水(主要含溴物质为 )为原料制备液溴,工艺流程如图:
)为原料制备液溴,工艺流程如图:
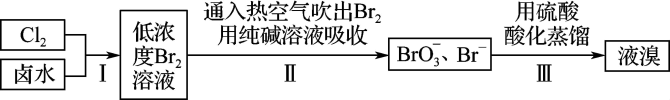
回答下列问题:
(1)反应I的离子方程式为___ ,制取氯气的装置如图甲,仪器a的名称为___ ,仪器b的作用是____ 。
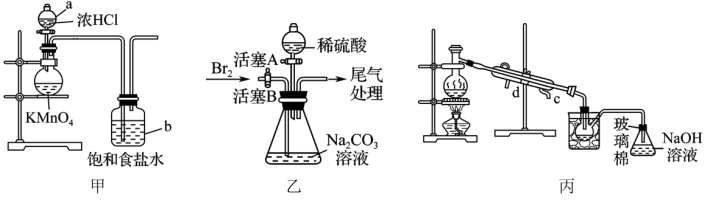
(2)反应II、反应III通过图乙装置实现,请写出反应Ⅱ的操作过程:_______ ,反应Ⅲ的有关化学反应的离子方程式为_______ 。
(3)通过图丙装置可得到液溴,写出该装置中缺少的仪器名称:_______ ,蒸馏烧瓶中加入小瓷片的目的是_______ ,冷凝水从_______ (填“c”或“d”)端进入。
 )为原料制备液溴,工艺流程如图:
)为原料制备液溴,工艺流程如图:
回答下列问题:
(1)反应I的离子方程式为

(2)反应II、反应III通过图乙装置实现,请写出反应Ⅱ的操作过程:
(3)通过图丙装置可得到液溴,写出该装置中缺少的仪器名称:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海水中蕴藏着丰富的资源。除从海水中可制得食盐外,还可以制取镁、钾、溴及其化工产品。从海水中制取金属镁、溴的化工流程图如下:
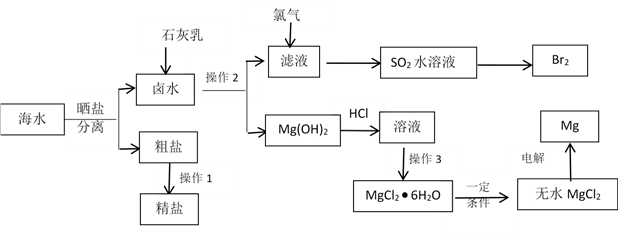
已知:MgO的熔点为2800℃,MgCl2的熔点为712℃。
回答下列问题:
(1)操作2的方法是_____________ ,操作3具体指_____________________ 。
(2)操作1粗盐精制主要是要除掉粗盐中的Ca2+、Mg2+、 离子,以下试剂合理的组合是
离子,以下试剂合理的组合是________
① 稀盐酸 ② NaOH ③ Na2CO3 ④ BaCl2
a.②③④① b.③②④① c.④②③① d.④③①②
(3)SO2水溶液可以起到富集溴的目的,该溶液吸收溴的离子反应方程式是____________ 。
(4)写出电解MgCl2制取Mg的化学方程式______________________ 。
(5)有同学认为:上述流程过于复杂,可直接加热Mg(OH)2得到MgO,再电解熔融的MgO制取金属镁,这样可简化实验步骤,体现实验的简约性原则。你同意该同学的想法吗?_______ (填“同意”或“不同意”),请说出你同意或不同意的理由____________________________ 。

已知:MgO的熔点为2800℃,MgCl2的熔点为712℃。
回答下列问题:
(1)操作2的方法是
(2)操作1粗盐精制主要是要除掉粗盐中的Ca2+、Mg2+、
 离子,以下试剂合理的组合是
离子,以下试剂合理的组合是① 稀盐酸 ② NaOH ③ Na2CO3 ④ BaCl2
a.②③④① b.③②④① c.④②③① d.④③①②
(3)SO2水溶液可以起到富集溴的目的,该溶液吸收溴的离子反应方程式是
(4)写出电解MgCl2制取Mg的化学方程式
(5)有同学认为:上述流程过于复杂,可直接加热Mg(OH)2得到MgO,再电解熔融的MgO制取金属镁,这样可简化实验步骤,体现实验的简约性原则。你同意该同学的想法吗?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。
I.海水的淡化多用蒸馏法,蒸馏法的优点是设备简单、操作简便、淡水质量好,但也有明显缺陷。
(1)蒸馏法进行海水淡化处理的主要缺陷是_______ ;
(2)某沿海地区拟采用蒸馏法兴建一座大型海水淡化工厂,为克服蒸馏法淡化海水的缺陷,请为该地区提出一条合理化建议:_________ ;
Ⅱ.空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如图:
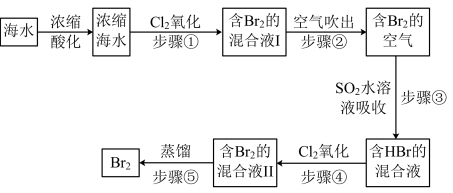
(3)步骤①中获得Br2的离子方程式为_________ ;
(4)步骤③中反应的化学方程式为__________ ;
(5)根据上述反应可判断SO2、 Cl2、 Br2三种物质氧化性由强到弱的顺序___________ ;
Ⅲ.海带灰中富含以I- 形式存在的碘元素。实验室提取I2的流程如图所示:
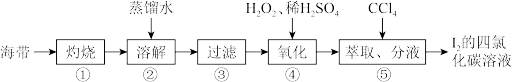
(6)步骤②需加热煮沸一会儿的目的是_______ ;
(7)步骤④中反应的离子方程式为_____ ;
(8)步骤⑤加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________ 色。萃取所用的主要仪器是________ 。
I.海水的淡化多用蒸馏法,蒸馏法的优点是设备简单、操作简便、淡水质量好,但也有明显缺陷。
(1)蒸馏法进行海水淡化处理的主要缺陷是
(2)某沿海地区拟采用蒸馏法兴建一座大型海水淡化工厂,为克服蒸馏法淡化海水的缺陷,请为该地区提出一条合理化建议:
Ⅱ.空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如图:

(3)步骤①中获得Br2的离子方程式为
(4)步骤③中反应的化学方程式为
(5)根据上述反应可判断SO2、 Cl2、 Br2三种物质氧化性由强到弱的顺序
Ⅲ.海带灰中富含以I- 形式存在的碘元素。实验室提取I2的流程如图所示:
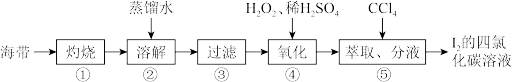
(6)步骤②需加热煮沸一会儿的目的是
(7)步骤④中反应的离子方程式为
(8)步骤⑤加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是___________ (填序号)。
A.食盐 B.淡水 C.烧碱 D.纯碱 E.溴
(2)大量的镁从海水中提取,一种工业制备无水氯化镁的工艺流程如下:
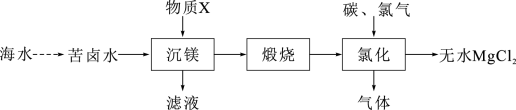
工业上常用“沉镁”物质X的是___________ ,“氯化”过程中的气态副产物常用作还原剂,“氯化”发生的化学方程式是___________ 。
(3)海带中含有碘元素。实验室提取碘的步骤如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是_______ 。海带灰中含有硫酸镁、碳酸钠等,在实验步骤___________ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式_______ 。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈___________ 色。
③请设计实验检验用CCl4提取碘后的水溶液中是否还含有碘单质___________ (包括实验步骤、现象及结论)。
(1)无需经过化学变化就能从海水中获得的物质是
A.食盐 B.淡水 C.烧碱 D.纯碱 E.溴
(2)大量的镁从海水中提取,一种工业制备无水氯化镁的工艺流程如下:

工业上常用“沉镁”物质X的是
(3)海带中含有碘元素。实验室提取碘的步骤如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
②写出步骤④反应的离子方程式
③请设计实验检验用CCl4提取碘后的水溶液中是否还含有碘单质
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用。
Ⅰ.人体碘的重要来源之一是食用加碘食盐(含KIO3)。为检测食盐中的KIO3,并测定加碘食盐样品的碘含量,某实验小组设计了如下实验:
①用天平准确称取w g食盐样品,加适量蒸馏水使其完全溶解。
②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全生成I2。
③以淀粉为指示剂,逐滴加入浓度为2.0×10-3mol·L-1的Na2S2O3溶液6.00 mL,恰好反应完全。(已知:I2+2S2O32-= 2I-+S4O62-)
(1)书写步骤②中反应的离子方程式:_______________________________ 。
(2)步骤③中判断反应恰好完全的现象是_____________________________ 。
(3)上述实验样品中碘元素 的含量是_________________ mg/g(以含w的代数式表达)。
Ⅱ.海带或海苔中含有丰富的碘元素,也是人体碘的一种来源。下图是实验室从海带
(含I-)中提取碘单质的流程图。
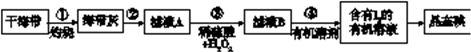
(1)步骤①中灼烧海带用到的实验仪器是__________ (填序号)。
a.坩埚b.试管c.蒸发皿d.烧杯
(2)步骤②的实验操作包括_____________ 。步骤④中分液所用的玻璃仪器是____ 、烧杯。
(3)步骤③中反应的离子方程式 是_______________________________________ 。
Ⅰ.人体碘的重要来源之一是食用加碘食盐(含KIO3)。为检测食盐中的KIO3,并测定加碘食盐样品的碘含量,某实验小组设计了如下实验:
①用天平准确称取w g食盐样品,加适量蒸馏水使其完全溶解。
②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全生成I2。
③以淀粉为指示剂,逐滴加入浓度为2.0×10-3mol·L-1的Na2S2O3溶液6.00 mL,恰好反应完全。(已知:I2+2S2O32-= 2I-+S4O62-)
(1)书写步骤②中反应的离子方程式:
(2)步骤③中判断反应恰好完全的现象是
(3)上述实验样品中
Ⅱ.海带或海苔中含有丰富的碘元素,也是人体碘的一种来源。下图是实验室从海带
(含I-)中提取碘单质的流程图。

(1)步骤①中灼烧海带用到的实验仪器是
a.坩埚b.试管c.蒸发皿d.烧杯
(2)步骤②的实验操作包括
(3)步骤③中反应的
您最近一年使用:0次



