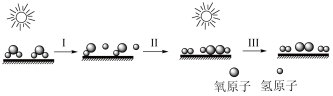
多相催化反应是反应物分子在催化剂表面通过吸附、解吸过程进行的反应。我国学者发现在T℃时,甲醇(CH3OH)在铜基催化剂上的反应机理如下(该反应为可逆反应)
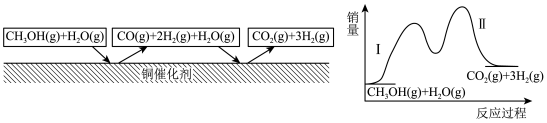
下列说法正确的是

下列说法正确的是
| A.铜基催化剂不参与反应 |
| B.CH3OH(g)与H2O(g)生成CO2(g)和H2(g)的反应为放热反应 |
| C.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂 |
| D.反应I的ΔH>0,反应II的ΔH<0 |
更新时间:2022-05-17 18:56:32
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某反应的能量变化如图所示,下列说法正确的是
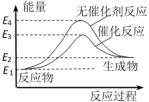

| A.反应物的总能量高于生成物的总能量 |
| B.反应的活化能E=E4-E3 |
| C.适当升高温度有利于提高该反应物的转化率 |
| D.使用催化剂能够降低该反应的反应热(ΔH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应NO2+CO=NO+CO2的能量变化如图所示,下列说法正确的是( )
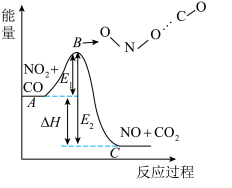

| A.正反应是吸热反应 |
| B.E1表示逆反应的活化能 |
| C.当NO2和CO系统的平均能量到达B处时,碰撞形成ONO…CO |
| D.A点表示NO2和CO系统的平均能量,此处两分子发生碰撞并发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.任何条件下的热效应都是焓变 |
| B.书写热化学方程式时若不标明温度和压强,则表示是在0℃、101 kPa条件下的反应热 |
| C.化学反应中的能量变化,是由化学反应中反应物中化学键断裂时吸收的能量与生成物中化学键形成时放出的能量不同所导致的 |
D.吸热反应的 H<0,放热反应的 H<0,放热反应的 H>0 H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确 的是
| A.任何酸碱之间发生中和反应生成1 mol H2O(l)时放出的热量都是57.3 kJ |
| B.H2的燃烧热指1molH2完全燃烧生成水所放出的热量 |
| C.中和热随酸碱反应物的用量的增加而增大 |
| D.反应热是指等温条件下,化学反应体系向环境释放的热量或从环境吸收的热量 |
您最近一年使用:0次
【推荐3】已知热化学方程式:H2(g)+2ICl(g) === 2HCl(g)+I2(g) ΔH=a kJ·mol-1。其反应过程如下:
①H2(g)+ICl(g) === HClI(g)+H(g)(慢)
②H(g)+ICl(g) === HCl(g)+I(g)(快)
③HClI(g) === HCl(g)+I(g)(快)
④I(g)+I(g) === I2(g)(快)
下列说法不正确的是( )
①H2(g)+ICl(g) === HClI(g)+H(g)(慢)
②H(g)+ICl(g) === HCl(g)+I(g)(快)
③HClI(g) === HCl(g)+I(g)(快)
④I(g)+I(g) === I2(g)(快)
下列说法不正确的是( )
| A.反应④的焓变小于0 |
| B.HClI是上述总反应的催化剂 |
| C.总反应的速率由反应①的速率决定 |
| D.总反应的正反应活化能Ea1与逆反应活化能Ea2之差为a kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应2NO(g)+2H2(g)=N2(g)+2H2O(g)中,每生成7 g N2放出166 kJ的热量,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n待测),该反应包含下列两步:①2NO+H2=N2+H2O2(慢),②H2O2+H2=2H2O(快)。T ℃时测得有关实验数据如表:
下列说法错误的是
| 序号 | c(NO)/(mol·L-1) | c(H2)/(mol·L-1) | 速率/(mol·L-1·min-1) |
| Ⅰ | 0.006 0 | 0.0010 | 1.8×10-4 |
| Ⅱ | 0.006 0 | 0.002 0 | 3.6×10-4 |
| Ⅲ | 0.001 0 | 0.006 0 | 3.0×10-5 |
| Ⅳ | 0.002 0 | 0.006 0 | 1.2×10-4 |
| A.整个反应速度由第①步反应决定 |
| B.该反应速率表达式:v=5000c2(NO)·c(H2) |
| C.正反应的活化能:①>② |
| D.该反应的热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g) ΔH=-332 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】工业上合成尿素的反应在进行时分为如下两步:
第一步: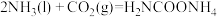 (氨基甲酸铵)
(氨基甲酸铵)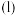

第二步: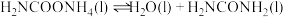

某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图Ⅰ所示。
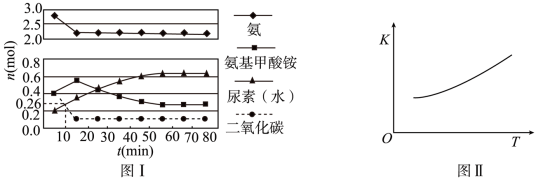
下列说法中正确的是
第一步:
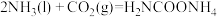 (氨基甲酸铵)
(氨基甲酸铵)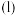

第二步:
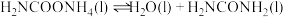

某实验小组模拟工业上合成尿素的条件,在一体积为0.5L密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如图Ⅰ所示。

下列说法中正确的是
| A.由图可知,第一步反应的活化能小于第二步反应 |
| B.当氨基甲酸铵的物质的量达到最大值时,合成尿素的反应达到化学平衡状态 |
C.0~10min中,用 表示的第一步反应的速率 表示的第一步反应的速率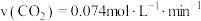 |
| D.已知第二步反应的化学平衡常数K随温度的变化如图Ⅱ所示。则其它条件不变时,温度升高,尿素的产率一定增大 |
您最近一年使用:0次