甲醇是重要的燃料,化学教材《选择性必修1》100页第5题介绍了甲醇( )酸性燃料电池,资料显示其结构如图所示。
)酸性燃料电池,资料显示其结构如图所示。

(1)A为燃料电池的_______ (填“正”或“负”)极, 在其表面发生
在其表面发生_______ 反应(填“氧化”或“还原”)。
(2)放电过程中,经过交换膜时, 的迁移方向是
的迁移方向是_______ (填“A→B”或“B→A”)。
(3)正极反应式_______ 。
(4)负极反应式为_______ 。
(5)在电池反应中,每生成1mol二氧化碳,理论上消耗标准状况下氧气的体积是_______ 。
(6)在25℃、101kPa下,1g液态甲醇燃烧生成 和液态水时放热22.5kJ,其热化学方程式为
和液态水时放热22.5kJ,其热化学方程式为_______ ;研究表明,甲醇用于火力发电的能量转化率_______ 于燃料电池(填“高”或“低”)。
(7)合成甲醇的反应为: △H。已知CO的结构式为
△H。已知CO的结构式为 ,甲醇的结构式为
,甲醇的结构式为 ,相关键能数据如下:
,相关键能数据如下:
由此计算△H=_______  。
。
 )酸性燃料电池,资料显示其结构如图所示。
)酸性燃料电池,资料显示其结构如图所示。
(1)A为燃料电池的
 在其表面发生
在其表面发生(2)放电过程中,经过交换膜时,
 的迁移方向是
的迁移方向是(3)正极反应式
(4)负极反应式为
(5)在电池反应中,每生成1mol二氧化碳,理论上消耗标准状况下氧气的体积是
(6)在25℃、101kPa下,1g液态甲醇燃烧生成
 和液态水时放热22.5kJ,其热化学方程式为
和液态水时放热22.5kJ,其热化学方程式为(7)合成甲醇的反应为:
 △H。已知CO的结构式为
△H。已知CO的结构式为 ,甲醇的结构式为
,甲醇的结构式为 ,相关键能数据如下:
,相关键能数据如下:| 化学键 | H-H | C-O |  | H-O | C-H |
 | 436 | 343 | 1076 | 465 | 413 |
 。
。
更新时间:2022-05-19 13:39:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的反应热(化学计量数相同)分别为ΔH1、ΔH2,ΔH1___ ΔH2(填“>”“<”或“=”,下同)。
(2)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___ ΔH2。
①4P(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
(3)将X分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈现如图所示状态。

①若X为金属氧化物,现象如图一所示,X可能是___ (填化学式)。
②若如图二所示,以下选项中与其能量变化相同的是___ 。
A.CO还原CuO的反应
B.CaCO3的分解反应
C.Al和Fe2O3的反应
(4)已知拆开1molH—H键、1molN—H键、1molN≡N键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___ 。
(5)已知:H2(g)+ O2(g)=H2O(1)ΔH1=-286kJ·mol-1
O2(g)=H2O(1)ΔH1=-286kJ·mol-1
H2(g)+O2(g)=H2O2(l)ΔH2=-188kJ·mol-1
过氧化氢分解反应2H2O2(1)=2H2O(l)+O2(g)的ΔH=___ kJ·mol-1。
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的反应热(化学计量数相同)分别为ΔH1、ΔH2,ΔH1
(2)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1
①4P(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
(3)将X分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈现如图所示状态。

①若X为金属氧化物,现象如图一所示,X可能是
②若如图二所示,以下选项中与其能量变化相同的是
A.CO还原CuO的反应
B.CaCO3的分解反应
C.Al和Fe2O3的反应
(4)已知拆开1molH—H键、1molN—H键、1molN≡N键需要的能量分别是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(5)已知:H2(g)+
 O2(g)=H2O(1)ΔH1=-286kJ·mol-1
O2(g)=H2O(1)ΔH1=-286kJ·mol-1H2(g)+O2(g)=H2O2(l)ΔH2=-188kJ·mol-1
过氧化氢分解反应2H2O2(1)=2H2O(l)+O2(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________ 。
(3)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g) H=+67.7kJ•mol-1;
H=+67.7kJ•mol-1;
N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1;
H=-534kJ•mol-1;
H2O(l)=H2O(g) H=+44.0kJ•mol-1;
H=+44.0kJ•mol-1;
则N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=___________ 。
请写出N2H4和NO2反应生成氮气和水蒸气的热化学方程式:___________ 。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(3)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知:N2(g)+2O2(g)=2NO2(g)
 H=+67.7kJ•mol-1;
H=+67.7kJ•mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g)
 H=-534kJ•mol-1;
H=-534kJ•mol-1;H2O(l)=H2O(g)
 H=+44.0kJ•mol-1;
H=+44.0kJ•mol-1;则N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=
请写出N2H4和NO2反应生成氮气和水蒸气的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ能量,根据如图中的能量图,回答下列问题:

(1)分别写出①②的数值:
①__________ ;②__________ 。
(2)生成H2(Xg)中的1 mol H—O键放出__________ kJ的能量。
(3)已知:H2O(l)二H2O(g)△H=+44 kJ • mol−1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:___________________________________ 。

(1)分别写出①②的数值:
①
(2)生成H2(Xg)中的1 mol H—O键放出
(3)已知:H2O(l)二H2O(g)△H=+44 kJ • mol−1,试写出氢气在氧气中完全燃烧生成液态水的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)“高分一号”卫星使用了大功率运载火箭,火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),其反应为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),该反应生成1molH2O(g)释放出160.4kJ热量。
①H2O2的电子式为______ 。
②若反应后,O-H键增加了16mol,则反应释放出的热量为______ kJ。
(2)镍氢蓄电池具有能量密度大、电压高、可多次反复充放电等特性,该电池放电时,正极反应式为2NiOOH+2H2O+2e-=2Ni(OH)2+2OH-,负极反应式为H2+2OH-+2e-=2H2O。
①该镍氢蓄电池放电时的电池总反应为____ 。
②该电池放电时,OH-向____ (填“正极”或“负极”)移动。
③假设该电池放电时有2.408×1024个电子从负极流向正极,则消耗的H2在标准状况下的体积为____ L。
(1)“高分一号”卫星使用了大功率运载火箭,火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),其反应为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g),该反应生成1molH2O(g)释放出160.4kJ热量。
①H2O2的电子式为
②若反应后,O-H键增加了16mol,则反应释放出的热量为
(2)镍氢蓄电池具有能量密度大、电压高、可多次反复充放电等特性,该电池放电时,正极反应式为2NiOOH+2H2O+2e-=2Ni(OH)2+2OH-,负极反应式为H2+2OH-+2e-=2H2O。
①该镍氢蓄电池放电时的电池总反应为
②该电池放电时,OH-向
③假设该电池放电时有2.408×1024个电子从负极流向正极,则消耗的H2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】控制适合的条件,将反应2Fe3++2I-⇌2Fe2++I2设计成如图所示的原电池。

请回答下列问题:
(1)①反应开始时,乙中石墨电极上发生__ (填“氧化”或“还原”)反应,电极反应式为___ 。甲中石墨电极上发生___ (填“氧化”或“还原”)反应,电极反应式为__ 。
②电流表读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作__ (填“正”或“负”)极,该电极的电极反应式为___ 。
(2)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为___ 。

请回答下列问题:
(1)①反应开始时,乙中石墨电极上发生
②电流表读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(2)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】汽车尾气中氮氧化合物、碳氧化合物的处理与利用是各国研究的热点。
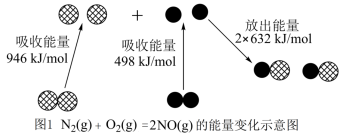
(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会____ (选填“吸收”或“放出”)____ kJ的能量。
(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g) 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
①反应进行到10s时,正反应速率____ 逆反应速率(选填“>”“<”或“=”),0~10s内用CO2表示的平均反应速率是____ mol/(L•s)。
②该条件下,NO的最大转化率为____ 。
③下列措施一定能增大该反应速率的是____ (填标号)。
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
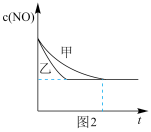
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂____ (选填“甲”或“乙”)的催化效果更好。
(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的____ 极(选填“正”或“负”),电极A的电极反应为____ 。

(1)NO生成过程的能量变化如图1所示。该条件下,1molN2和1molO2完全反应生成NO会

(2)CO与NO在催化剂作用下反应可实现汽车尾气净化:2CO(g)+2NO(g)
 2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。
2CO2(g)+N2(g)。某实验小组在200℃、5L恒容密闭容器中充入等物质的量的CO与NO模拟该过程,NO的物质的量随时间变化如表所示。| t/s | 0 | 10 | 20 | 30 | 40 | 50 |
| n(NO)/mol | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
①反应进行到10s时,正反应速率
②该条件下,NO的最大转化率为
③下列措施一定能增大该反应速率的是
A.及时分离出CO2 B.适当升高温度 C.适当压缩容器的容积 D.充入1molHe
④某同学在其它条件一定的情况下,分别用甲、乙两种催化剂完成该反应,绘出NO浓度随时间变化关系如图2所示,催化剂

(3)用电化学气敏传感器测定汽车尾气中CO含量,原理如图3所示,根据燃料电池的原理,推测电极B是该电池的

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.
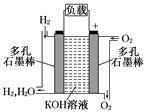
试回答下列问题:
(1)燃料电池的优点是________ ;电解质溶液中的OH -移向______ 极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________ 。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________ .
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为__________ 。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________ ;
(2)通过导线的电子数为__________ (用 N A表示).

试回答下列问题:
(1)燃料电池的优点是
(2)写出氢氧燃料电池工作时正极反应式:
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为
(2)通过导线的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】观察图A、B,回答下列问题:
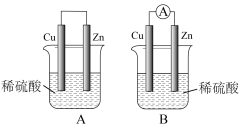
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡产生,再平行插入一块铜片,可观察到铜片_______ (填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来(见图A),组成一个原电池,正极的电极反应式为______ 。
(2)如果烧杯中最初装入的是2mol·L-1500mL的稀硫酸,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线流入铜电极),当在标准状况下收集到11.2L的氢气时,烧杯内溶液中溶质的物质的量浓度分别为(请指明溶质,溶液体积变化忽略不计)______ 、________ 。
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-=== +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是______ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子

(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡产生,再平行插入一块铜片,可观察到铜片
(2)如果烧杯中最初装入的是2mol·L-1500mL的稀硫酸,构成铜锌原电池(见图B,假设产生的气体没有损失,锌失去的电子完全沿导线流入铜电极),当在标准状况下收集到11.2L的氢气时,烧杯内溶液中溶质的物质的量浓度分别为(请指明溶质,溶液体积变化忽略不计)
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH--6e-===
 +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】图中p、q为电源两极,A为锌电极,B、C、 D为铂电极,接通电源,只有B、C、D上产生气泡。试回答:

(1)电极名称:p为 极,D为 极;
(2)两个电极上产生的气体相同的是 (填B、C、D)
(3)C极的电极反应式 ;
(4)烧杯中H+的移动方向: (填“A向B”或“B向A”)
(5)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月才充电一次。假定放电过程中,甲醇(CH3OH)完全氧化产生的CO2被充分吸收生成CO32-。 该电池的负极电极反应为 ; 用此新型电池做上图装置的电源,则当C极产生3mol气体时,电池需消耗 克甲醇蒸汽。

(1)电极名称:p为 极,D为 极;
(2)两个电极上产生的气体相同的是 (填B、C、D)
(3)C极的电极反应式 ;
(4)烧杯中H+的移动方向: (填“A向B”或“B向A”)
(5)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月才充电一次。假定放电过程中,甲醇(CH3OH)完全氧化产生的CO2被充分吸收生成CO32-。 该电池的负极电极反应为 ; 用此新型电池做上图装置的电源,则当C极产生3mol气体时,电池需消耗 克甲醇蒸汽。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学在物质制备、新材料和环境保护等方面具有独到的应用优势。
(1)高铁酸钠( )是一种新型水处理剂,强碱性条件下稳定存在。电解法制备
)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备 的工作原理如图所示,a是电源的
的工作原理如图所示,a是电源的___________ 极(填“正”或“负”)。阳极电极的电极反应式为___________ ,装置中可循环使用的物质的化学式是___________ 。

(2)燃煤烟气中的 可用如下装置进行处理。
可用如下装置进行处理。

M极发生的电极反应式为____________ ,一段时间后N极附近溶液
___________ (填“增大”、“减小”或“不变”);当外电路通过0.2 电子时,质子交换膜左侧溶液质量
电子时,质子交换膜左侧溶液质量___________ (填“增大”或“减小”)___________ g。
(1)高铁酸钠(
 )是一种新型水处理剂,强碱性条件下稳定存在。电解法制备
)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备 的工作原理如图所示,a是电源的
的工作原理如图所示,a是电源的
(2)燃煤烟气中的
 可用如下装置进行处理。
可用如下装置进行处理。
M极发生的电极反应式为

 电子时,质子交换膜左侧溶液质量
电子时,质子交换膜左侧溶液质量
您最近一年使用:0次
【推荐2】原电池反应一般是氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子,电子通过外电路输送到正极上,氧化剂在正极上得电子,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
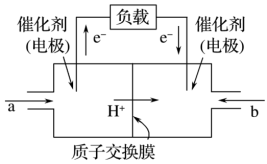
(1)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是_______ (填名称),其电极反应式为_______ ,b极电极反应式为_______
(2)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。
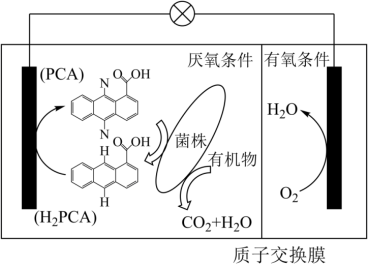
①该电池的电流方向:由_______ (填“左”或“右”,下同)侧电极经过负载流向_______ 侧电极。
②当1molO2参与电极反应时,从左侧穿过质子交换膜进入右侧的H+数目为_______ NA。
(1)甲醇燃料电池结构简单、能量转化率高,工作原理如图所示。加入的a是

(2)我国科学工作者从环境污染物中分离出一株假单胞菌,该菌株能够在分解有机物的同时产生电能,其原理如图所示。

①该电池的电流方向:由
②当1molO2参与电极反应时,从左侧穿过质子交换膜进入右侧的H+数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s),设计的原电池如图所示,其中盐桥内装琼脂-饱和KNO3溶液。请回答下列问题:
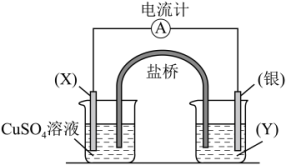
(1)电极X的材料是_______ ;(填化学式,下同)电解质溶液Y是 _______ 。
(2)Ag是_______ 极。填(“正”或“负”)
(3)写出两电极的电极反应式:银电极:_______ ;X电极:_______ 。
(4)外电路中的电子是从_______ 电极流向_______ 电极。(填电极材料名称)
(5)盐桥中向CuSO4溶液中迁移的离子是_______(填字母)。
(6)1 mol Ag生成时,转移电子的物质的量为_______ mol。

(1)电极X的材料是
(2)Ag是
(3)写出两电极的电极反应式:银电极:
(4)外电路中的电子是从
(5)盐桥中向CuSO4溶液中迁移的离子是_______(填字母)。
| A.K+ | B. | C.Ag+ | D. |
(6)1 mol Ag生成时,转移电子的物质的量为
您最近一年使用:0次



