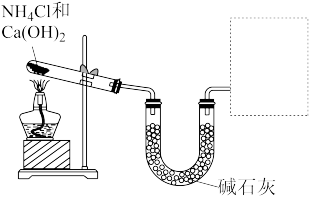
某银白色金属单质A在空气中加热燃烧时发出黄色火焰,得到淡黄色固体B,A露置在空气中足够长时间变为C,B和酸性气体D能生成C,A和B都能与水生成E,E和D也能生成C。回答下列问题。
(1)写出下列物质的化学式:C______ ,D______ ,E______ 。
(2)写出下列反应的化学方程式:
①A和水生成E:______ 。
②B和D生成C:______ 。
③Cl2与E的水溶液:______ 。
(1)写出下列物质的化学式:C
(2)写出下列反应的化学方程式:
①A和水生成E:
②B和D生成C:
③Cl2与E的水溶液:
11-12高一上·山东泰安·期中 查看更多[6]
(已下线)2011-2012学年山东省宁阳四中高一第一学期期中学分认定化学试卷(已下线)2013届广东省东莞市七中高三上学期第一次月考理综化学试卷(已下线)2013届河北保定唐县一中高三下第二次摸底考试化学试卷2016-2017学年山东省枣庄八中高一10月月考化学试卷福建省永安市第九中学2022-2023学年高一上学期期中考试化学试题甘肃省武威市凉州区2024届高三第三次诊断考试化学试题
更新时间:2016-12-09 04:18:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(一)下面是我们熟悉的物质:①O2 ②NaBr ③H2SO4 ④Na2CO3 ⑤NH4Cl ⑥NaHSO4 ⑦Ne ⑧Na2O2 ⑨NaOH ⑩CO2。
(1)这些物质中,只含有共价键的是____ ;只含有离子键的是____ ;不存在化学键的是____ (填物质序号)。
(2)属于共价化合物的是____ (填物质序号)。
(3)将Na2O2溶于水,破坏了Na2O2中的____ ,Na2O2的电子式为____ ;NaHSO4熔融状态下电离,破坏了____ 键,写出电离方程式____ 。
(4)CO2固体气化破坏了____ 。
(二)由H、N、O、Al组成的微粒中:微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(5)用化学式表示下列3种微粒:A____ ;C____ ;D____ 。
(6)写出过量的B通入E的溶液中反应的离子方程式____ 。
(7)用电子式表示B的形成过程____ 。
(1)这些物质中,只含有共价键的是
(2)属于共价化合物的是
(3)将Na2O2溶于水,破坏了Na2O2中的
(4)CO2固体气化破坏了
(二)由H、N、O、Al组成的微粒中:微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(5)用化学式表示下列3种微粒:A
(6)写出过量的B通入E的溶液中反应的离子方程式
(7)用电子式表示B的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)④、⑥、⑦的离子半径由大到小的顺序为___________ 。
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式___________ 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为________ 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式___________ 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。
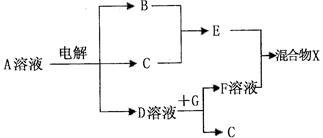
①写出D溶液与G反应的化学方程式_________________________________ 。
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为________ mol。
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有_______________ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ||||||
| 3 | ⑤ | ③ | ⑥ | ⑦ | ||||
(1)④、⑥、⑦的离子半径由大到小的顺序为
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求填写下列方程式
(1)NaOH溶液和氯气反应的化学方程式:___________ ;
(2)过氧化钠和二氧化碳反应的化学方程式:___________ ;
(3)过氧化钠和水反应的化学方程式:___________ ;
(4)写出 在加热条件下的化学方程式:
在加热条件下的化学方程式:___________ ;
(5)钠与水(加入酚酞)反应的化学方程式:___________ ;并写出该实验出现的五个现象___________ 。
(1)NaOH溶液和氯气反应的化学方程式:
(2)过氧化钠和二氧化碳反应的化学方程式:
(3)过氧化钠和水反应的化学方程式:
(4)写出
 在加热条件下的化学方程式:
在加热条件下的化学方程式:(5)钠与水(加入酚酞)反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据化学知识和基本原理回答下列问题。
(1)根据组成和性质分类, 应属于
应属于_______ 氧化物;金属Al溶于氢氧化钠溶液的离子反应方程式为_______ 。
(2)15.6g 固体中所含阴离子的数目为
固体中所含阴离子的数目为_______ ,标准状况下4.48L  中所含电子数目为
中所含电子数目为_______ ,与其含有相同H原子数目的HC1气体的物质的量为_______ mol。
(3)将0.4mol HCl气体溶于水配成200mL溶液,则所得盐酸溶液中溶质的物质的量浓度为_______ mol/L,从该溶液中取出25.00mL,加水稀释至500mL,则稀释后盐酸溶液中溶质的物质的量浓度为_______ mol/L。
(4)100mL某 和
和 的混合溶液中,已知
的混合溶液中,已知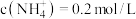 ,
, ,则该溶液中所含
,则该溶液中所含 的物质的量浓度为
的物质的量浓度为_______ mol/L。
(1)根据组成和性质分类,
 应属于
应属于(2)15.6g
 固体中所含阴离子的数目为
固体中所含阴离子的数目为 中所含电子数目为
中所含电子数目为(3)将0.4mol HCl气体溶于水配成200mL溶液,则所得盐酸溶液中溶质的物质的量浓度为
(4)100mL某
 和
和 的混合溶液中,已知
的混合溶液中,已知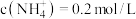 ,
, ,则该溶液中所含
,则该溶液中所含 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】金属及其化合物在人类生产、生活中发挥着重要的作用。
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是________ (填化学式,下同);适宜做耐火材料的是__________ 。
(2)向盛有硫酸铝溶液的试管中滴加氨水,反应的离子方程式为_________________________________ ,得到的胶状沉淀物在医疗上治疗胃酸过多,利用的原理用离子方程式表示为_________________ 。
(3)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ (填序号)。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是
(2)向盛有硫酸铝溶液的试管中滴加氨水,反应的离子方程式为
(3)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】浩瀚的大海具有丰富的化学资源可以开发和利用,回答下列相关问题:
(1)纯碱是人类最早制取和使用的化学物质之一,其属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。我国化学家侯德榜发明了联合制碱法,制取方法是向饱和食盐水先通入足量NH3,再通入过量CO2,得到_______ (填化学式)晶体,过滤,再由该晶体制得纯碱的实验操作方法为_______ 。
(2)目前很多自来水厂使用ClO2来消毒、杀菌。
工业制取ClO2的反应:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O,该反应的氧化产物为_______ ,若制得33.75gClO2,转移电子的数目为_______ 。
(3)金属钠可用于生产汽车安全气囊中的气体发生剂NaN3.某汽车安全气囊中含NaN3.Fe2O3和NaHCO3等物质。
①当汽车发生较严重的碰撞时,NaN3受热分解为Na和N2,其化学方程式为_______ 。
②气囊中产生的NaN3立即与Fe2O3反应生成Na2O与另一种单质,该反应属于四种基本反应类型 中的_______ 反应。
③NaHCO3是冷却剂,分解时会吸收产气过程释放的热量。该反应的化学方程式为_______ 。
(1)纯碱是人类最早制取和使用的化学物质之一,其属于
(2)目前很多自来水厂使用ClO2来消毒、杀菌。
工业制取ClO2的反应:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O,该反应的氧化产物为
(3)金属钠可用于生产汽车安全气囊中的气体发生剂NaN3.某汽车安全气囊中含NaN3.Fe2O3和NaHCO3等物质。
①当汽车发生较严重的碰撞时,NaN3受热分解为Na和N2,其化学方程式为
②气囊中产生的NaN3立即与Fe2O3反应生成Na2O与另一种单质,该反应属于
③NaHCO3是冷却剂,分解时会吸收产气过程释放的热量。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如图1所示(部分产物已略去):
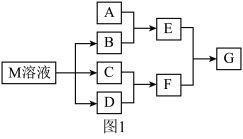
(1)写出B的电子式________ 。
(2)若A是一种非金属单质,且可用于制造半导体材料,写出A和B水溶液反应的离子方程式__________________________ 。
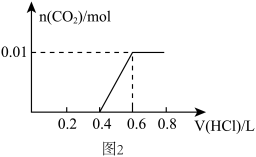
(3)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,生成的CO2物质的量与所用盐酸体积如图2所示,则A与B溶液反应后溶液中所有溶质的化学式为_____________ ;c(HCl)=________ mol/L。
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是______________________________________ 。
(5)若A是一种可用于做氮肥的化合物, A和B反应可生成气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,写出E与D反应的化学方程式为___________________ 。
(6)若A是一种溶液,可能含有H+、NH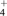 、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图3所示,由此可知,该溶液中肯定含有的离子是
、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图3所示,由此可知,该溶液中肯定含有的离子是_____________________ ,它们的物质的量浓度之比为______________ 。

(1)写出B的电子式
(2)若A是一种非金属单质,且可用于制造半导体材料,写出A和B水溶液反应的离子方程式
(3)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,生成的CO2物质的量与所用盐酸体积如图2所示,则A与B溶液反应后溶液中所有溶质的化学式为

(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是
(5)若A是一种可用于做氮肥的化合物, A和B反应可生成气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,写出E与D反应的化学方程式为
(6)若A是一种溶液,可能含有H+、NH
 、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图3所示,由此可知,该溶液中肯定含有的离子是
、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图3所示,由此可知,该溶液中肯定含有的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列各空:
(1)物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2和NaOH溶液 ⑥Fe和HNO3溶液 ⑦Fe和H2SO4溶液 ⑧Na和O2
a 由于温度不同而发生不同氧化还原反应的是_____________ 。
b由于浓度不同而发生不同氧化还原反应的是_______________ 。
c氧化还原反应不受浓度、温度影响的是_____________ 。
(2)用适当的方法除杂(括号内为杂质)
(1)物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2和NaOH溶液 ⑥Fe和HNO3溶液 ⑦Fe和H2SO4溶液 ⑧Na和O2
a 由于温度不同而发生不同氧化还原反应的是
b由于浓度不同而发生不同氧化还原反应的是
c氧化还原反应不受浓度、温度影响的是
(2)用适当的方法除杂(括号内为杂质)
| 物质 | 所加试剂或方法 |
| Na2CO3(NaHCO3)固体粉末 | |
| Na2CO3(NaHCO3)溶液 | |
| NaHCO3(Na2CO3)溶液 |
您最近一年使用:0次