科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可计算某些特殊反应的热效应。
(1)已知:①P4(s,白磷)+5O2(g)=P4O10(s) △H1=-2983.2kJ/mol;
②P(s,红磷)+ O2(g)=
O2(g)=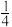 P4O10(s) △H2=-738.5kJ/mol。
P4O10(s) △H2=-738.5kJ/mol。
则白磷转化为红磷的热化学方程式____ ,相同的状况下,白磷的稳定性比红磷____ (填“高”或“低”)。
(2)红磷P(s)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
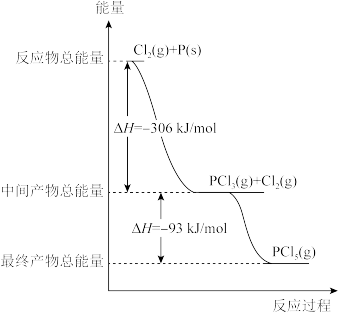
①PCl5分解生成PCl3和Cl2的热化学方程式____ 。
②P和Cl2分两步反应生成1molPCl5的△H3=____ 。
(1)已知:①P4(s,白磷)+5O2(g)=P4O10(s) △H1=-2983.2kJ/mol;
②P(s,红磷)+
 O2(g)=
O2(g)=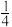 P4O10(s) △H2=-738.5kJ/mol。
P4O10(s) △H2=-738.5kJ/mol。则白磷转化为红磷的热化学方程式
(2)红磷P(s)和Cl2发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

①PCl5分解生成PCl3和Cl2的热化学方程式
②P和Cl2分两步反应生成1molPCl5的△H3=
更新时间:2022-05-31 16:25:23
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(I) (1)下列过程中不一定放出能量的是_______ 。
A.形成化学键 B.燃料燃烧 C.化合反应 D.炸药爆炸 E.酸碱中和
(2)已知A和B是同种元素形成的两种单质,A转化为B时需吸收能量,则A和B相比,较稳定的是_______ (填“A”或“B”)。
(3)某化学反应中,反应物的总能量为E1,生成物的总能量为E2,且E1<E2,则该反应是_______ (填“放热”或“吸热”)反应。
(4)已知H2和O2反应放热,且破坏1molH - H键、1molO=O键、1molO- H键需吸收的能量分别为Q1kJ、Q2kJ、 Q3kJ。下列关系正确的是_______ 。
A. Q1+Q2>Q3 B. Q1+Q2> 2Q3 C.2Q1+Q2<4Q3 D.2Q1+Q2 <2Q3
(II)在体积为2 L密闭容器中加入反应物A、B,发生如下反应:A+2B=3C,经2min后,A的浓度从开始时的1.0 mol/L降到0.8 mol/L。已知反应开始时B的浓度是1.2 mol/L。则:2min末 B的浓度_______ 、C的物质的量_______ ,2min内,用A物质的浓度变化来表示该反应的反应速率,即v(A) =_______ 。
A.形成化学键 B.燃料燃烧 C.化合反应 D.炸药爆炸 E.酸碱中和
(2)已知A和B是同种元素形成的两种单质,A转化为B时需吸收能量,则A和B相比,较稳定的是
(3)某化学反应中,反应物的总能量为E1,生成物的总能量为E2,且E1<E2,则该反应是
(4)已知H2和O2反应放热,且破坏1molH - H键、1molO=O键、1molO- H键需吸收的能量分别为Q1kJ、Q2kJ、 Q3kJ。下列关系正确的是
A. Q1+Q2>Q3 B. Q1+Q2> 2Q3 C.2Q1+Q2<4Q3 D.2Q1+Q2 <2Q3
(II)在体积为2 L密闭容器中加入反应物A、B,发生如下反应:A+2B=3C,经2min后,A的浓度从开始时的1.0 mol/L降到0.8 mol/L。已知反应开始时B的浓度是1.2 mol/L。则:2min末 B的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)汽车尾气是城市污染的一种,在汽车尾气装置中加入适当的催化剂可以实现汽车尾气的无害治理。如图是NO和CO反应生成CO2和N2过程中的能量变化示意图,说明这个反应是___________ (填“吸热”或“放热”)反应,NO和CO的总能量___________ (填“大于”“小于”或“等于”)CO2和N2的总能量。
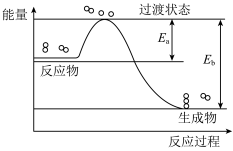
(2)金刚石和石墨互为同素异形体。已知在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9kJ的热量。
①该反应___________ (填“是”或“不是”)吸热反应。
②石墨和金刚石相比,___________ 能量高,___________ 更稳定。
③推测石墨与金刚石各1mol在相同条件下燃烧,___________ 放出的热量多。
(1)汽车尾气是城市污染的一种,在汽车尾气装置中加入适当的催化剂可以实现汽车尾气的无害治理。如图是NO和CO反应生成CO2和N2过程中的能量变化示意图,说明这个反应是

(2)金刚石和石墨互为同素异形体。已知在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9kJ的热量。
①该反应
②石墨和金刚石相比,
③推测石墨与金刚石各1mol在相同条件下燃烧,
您最近一年使用:0次
【推荐3】含碳的化合物之间很容易发生转化。请回答下列问题:
(1)有机物 M 在有光的时候很容易转化成 N,其过程如下:
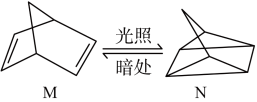
M 到 N 过程中,光能转化为__________ 能;其中较稳定的物质是_____________ (用 M、N 回答)。
(2)已知(l)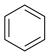 的燃烧热为3267.5kJ·mol-1,
的燃烧热为3267.5kJ·mol-1,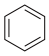 (l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a
(l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a__________ -3267.5(填“>”、“<”或“=”)。
(3)在标准状态即压力为 100kPa,一定温度下,由元素最稳定的单质生成生成 1mol 纯化合物时的反应热称为该化合物的标准摩尔生成焓(△H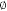 )。已知 100kPa,一定温度下:
)。已知 100kPa,一定温度下:
Fe2 O 3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+490.0 kJ·mol-1
CO(g)+1/2O2(g)=CO2 (g) △H=-280.0kJ·mol-1
C(石墨)+O 2 ( g)=CO2 (g) △H=-390.5kJ·mol-1
则 Fe2O3的标准摩尔生成焓△H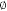 =
=______________ 。
(1)有机物 M 在有光的时候很容易转化成 N,其过程如下:

M 到 N 过程中,光能转化为
(2)已知(l)
 的燃烧热为3267.5kJ·mol-1,
的燃烧热为3267.5kJ·mol-1, (l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a
(l)+6O2(g)═6CO2(g)+3H2(g)△H=akJ·mol-1,则 a(3)在标准状态即压力为 100kPa,一定温度下,由元素最稳定的单质生成生成 1mol 纯化合物时的反应热称为该化合物的标准摩尔生成焓(△H
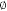 )。已知 100kPa,一定温度下:
)。已知 100kPa,一定温度下:Fe2 O 3(s)+3C(石墨)=2Fe(s)+3CO(g) △H=+490.0 kJ·mol-1
CO(g)+1/2O2(g)=CO2 (g) △H=-280.0kJ·mol-1
C(石墨)+O 2 ( g)=CO2 (g) △H=-390.5kJ·mol-1
则 Fe2O3的标准摩尔生成焓△H
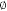 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分。
回答下列问题
(1)Z元素在周期表中的位置为__________ 。
(2)表中元素原子半径最大的是(填元素符号)__________ 。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________ ;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式__________ 。
(5)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为__________ 。Q与水反应的化学方程式为__________ 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种气体组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________ 。
| 碳 | 氮 | Y | |
| X | 硫 | Z |
回答下列问题
(1)Z元素在周期表中的位置为
(2)表中元素原子半径最大的是(填元素符号)
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式
(5)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种气体组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应的过程既是物质的转化过程,也是化学能与其他形式的能量转化的过程。研究化学反应中的能量变化与研究物质变化具有同样的重要意义。
Ⅰ.汽车尾气中的主要污染物是NOx(包括NO、NO2等氮氧化物)和CO。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图甲所示,则图甲中三种分子中最稳定的是_______ (填化学式)。 CO2(g)+N2(g) △H=Q kJ/mol。有关能量变化过程如图乙所示。
CO2(g)+N2(g) △H=Q kJ/mol。有关能量变化过程如图乙所示。_______ (填“放热”或“吸热”)反应。
(3)在反应体系中加入Pt2O*作为该反应的催化剂,则△H_______ Q kJ/mol (填“>”“<”或“=”)。
Ⅱ.完成下列热化学方程式
(4)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下3.2g SiH4自燃放出热量142.72kJ。SiH4自燃的热化学方程式为_______ 。
(5)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(6)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100g CaCO3沉淀,则表示乙醇燃烧热的热化学方程式为_______ 。
(7)目前我国城市居民所用燃料一般为煤气与石油液化气两种。煤气的主要成分为一氧化碳与氢气,煤气主要是在高温下由煤炭与水蒸气反应制得的;石油液化气的主要成分是C3H8.请回答下列问题:
已知:C3H8(g)+ O2(g)=3CO(g)+4H2(g) △H= -72.7 kJ/mol
O2(g)=3CO(g)+4H2(g) △H= -72.7 kJ/mol
CO(g)+ O2(g)=CO2(g) △H=-283.0 kJ/mol,
O2(g)=CO2(g) △H=-283.0 kJ/mol,
H2(g)+ O2(g)=H2O(l) △H=-285.8k/mol
O2(g)=H2O(l) △H=-285.8k/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=_______ kJ/mol。
Ⅰ.汽车尾气中的主要污染物是NOx(包括NO、NO2等氮氧化物)和CO。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图甲所示,则图甲中三种分子中最稳定的是
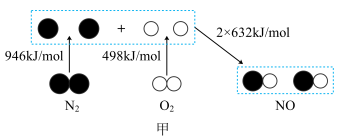
 CO2(g)+N2(g) △H=Q kJ/mol。有关能量变化过程如图乙所示。
CO2(g)+N2(g) △H=Q kJ/mol。有关能量变化过程如图乙所示。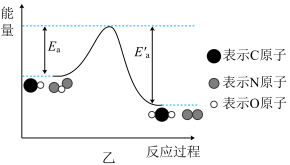
(3)在反应体系中加入Pt2O*作为该反应的催化剂,则△H
Ⅱ.完成下列热化学方程式
(4)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下3.2g SiH4自燃放出热量142.72kJ。SiH4自燃的热化学方程式为
(5)已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(6)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100g CaCO3沉淀,则表示乙醇燃烧热的热化学方程式为
(7)目前我国城市居民所用燃料一般为煤气与石油液化气两种。煤气的主要成分为一氧化碳与氢气,煤气主要是在高温下由煤炭与水蒸气反应制得的;石油液化气的主要成分是C3H8.请回答下列问题:
已知:C3H8(g)+
 O2(g)=3CO(g)+4H2(g) △H= -72.7 kJ/mol
O2(g)=3CO(g)+4H2(g) △H= -72.7 kJ/molCO(g)+
 O2(g)=CO2(g) △H=-283.0 kJ/mol,
O2(g)=CO2(g) △H=-283.0 kJ/mol,H2(g)+
 O2(g)=H2O(l) △H=-285.8k/mol
O2(g)=H2O(l) △H=-285.8k/molC3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
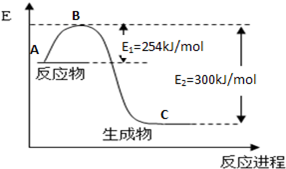
(1)上图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:_______ 。
(2)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g) 2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a
2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a_______ (填“增大”“减小”或“不变”)。
(3)用NH3催化还原NOx可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ/mol①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ/mol②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=_______ kJ·mol-1(用含a、b的式子表示)。
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=—25 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=—47 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:_______ 。

(1)上图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:
(2)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)
 2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a
2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a(3)用NH3催化还原NOx可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ/mol①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ/mol②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=—25 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=—47 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1 mol气态水过程中的能量变化图。
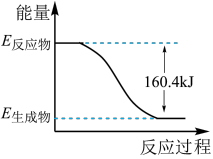
(1)该反应属于________ (填“吸热”或“放热”)反应。
(2)写出该火箭推进器中相关反应的热化学方程式:______ 。
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为_______ mol。

(1)该反应属于
(2)写出该火箭推进器中相关反应的热化学方程式:
(3)若该火箭推进器中有36g H2O生成,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为285.8 kJ·mol1、283.0 kJ·mol1和726.5kJ·mol1。请回答下列问题:
①写出表示H2燃烧热的热化学反应方程式__________________________ 。
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________________ 。
(2)以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)= CO(g)+3H2(g) ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)= CH3OH(g) ΔH=-129.0 kJ/mol
①将1.0 mol CH4和2.0 mol H2O(g)通入容积为10 L的反应容器,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。在100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为___________ 。100 ℃时反应Ⅰ的平衡常数为_______ 。在温度和容积不变的情况下,再向平衡体系中充入1.0 mol CH4和2.0 mol H2O(g),达到平衡时CO转化率_________ 。(填“增大”“不变”或“减小”)

②工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)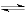 CO(g)+2H2(g),此反应高温下能自发进行的原因是:
CO(g)+2H2(g),此反应高温下能自发进行的原因是:________________ 。
(1)已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为285.8 kJ·mol1、283.0 kJ·mol1和726.5kJ·mol1。请回答下列问题:
①写出表示H2燃烧热的热化学反应方程式
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(2)以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)= CO(g)+3H2(g) ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)= CH3OH(g) ΔH=-129.0 kJ/mol
①将1.0 mol CH4和2.0 mol H2O(g)通入容积为10 L的反应容器,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。在100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为

②工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)
 CO(g)+2H2(g),此反应高温下能自发进行的原因是:
CO(g)+2H2(g),此反应高温下能自发进行的原因是:
您最近一年使用:0次

 O2 (g)
O2 (g) SO3(g),ΔH=-98kJ·mol-1,钒催化剂参与反应的能量变化如图(a)所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:
SO3(g),ΔH=-98kJ·mol-1,钒催化剂参与反应的能量变化如图(a)所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:


