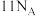二氯异氰尿酸钠是中国疾控中心研发的“−18℃低温消毒剂”的主要成分之一,其合成方法如图。下列有关说法错误的是

| A.上述流程所涉及物质中,离子晶体和分子晶体均有3种 |
| B.二氯异氰尿酸钠、次氯酸钠、75%的酒精均可用于杀菌消毒,它们的消毒原理相同 |
| C.二氯异氯尿酸钠所含元素中电负性最大的是O,第一电离能最小的是Na |
| D.二氯异氰尿酸钠中各原子最外层均满足8电子稳定结构 |
更新时间:2022-05-15 23:57:34
|
相似题推荐
【推荐1】以下说法中错误的是
| A.在①N、P、As和②Na、P、Cl中,元素的电负性随原子序数增大而递增的是② |
| B.同一原子中,2p、3p、4p能级的轨道依次增多 |
C.某元素原子的部分逐级电离能 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 分别为738、1451、7733、10540、13630,该元素可能在第三周期第ⅡA族 |
| D.在共价键F-I、F-Cl和C-C,极性最强的是F-I |
您最近一年使用:0次
【推荐2】下列说法不正确的是
| A.S−H键键能比Se−H键键能大,所以H2S比H2Se稳定 |
| B.某元素气态基态原子的逐级电离能(kJ·mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X2+ |
| C.白磷为正四面体分子,白磷分子中键角(P−P−P)是60° |
| D.乙炔(HC≡CH)分子易发生加成反应,分子中的π键键能小,易断裂,以此推断,N2分子中π键也容易断裂而发生化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图所示的化合物是一种重要的化工原料,X、Y、Z、W、E是原子序数依次增大的短周期主族元素,其中Z、E同族,基态Y原子的核外有3个未成对电子。下列说法正确的是
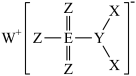
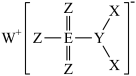
A.原子半径: | B.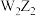 中只含有离子键 中只含有离子键 |
| C.Z、W、E组成化合物的水溶液一定显中性 | D.电负性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于物质结构或性质及解释都正确的是
| 物质结构或性质 | 解释 | |
| A | 键角: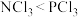 | N的电负性比P大,孤电子对对成键电子对的斥力比较大 |
| B | 稳定性:HF>HCl | HF分子间可以形成氢键,HCl没有氢键 |
| C | 配位键的稳定性: |  中O电负性更大,因而形成的配位键更稳定 中O电负性更大,因而形成的配位键更稳定 |
| D | 电子云半径:2s<4s | 4s电子能量高,在离核更远的区域出现的概率大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

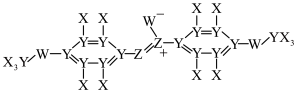

 键数为
键数为