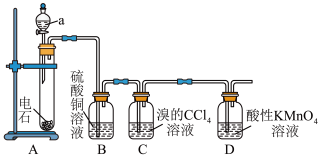
如图为实验室制取乙炔及其性质检验的装置图。(电石中含CaS等杂质)
回答下列问题:
(1)仪器a的名称为_______ ;该仪器中盛放的试剂为_______ 。
(2)装置A中主要反应的化学方程式为_______ 。
(3)装置B的作用是_______ 。
(4)C中反应物之间按物质的量之比1∶1反应,其化学方程式为_______ 。
(5)D中观察到的现象是_______ 。

回答下列问题:
(1)仪器a的名称为
(2)装置A中主要反应的化学方程式为
(3)装置B的作用是
(4)C中反应物之间按物质的量之比1∶1反应,其化学方程式为
(5)D中观察到的现象是
更新时间:2022-06-23 23:30:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】聚乙烯醇(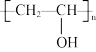 )是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
)是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
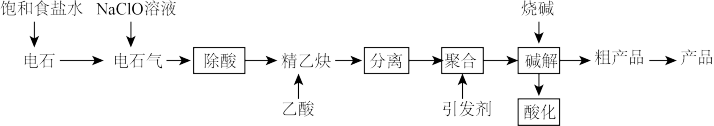
已知:①电石气中通常含有H2S、PH3等杂质②电石气通入次氯酸钠溶液后反应后,溶液仍澄清③乙炔较易与羧酸反应生成酯
回答下列问题:
(1)制取电石气时用饱和食盐水代替水的目的是____ ,电石气通入NaClO溶液发生的主要反应的离子方程式为____ (写一个即可)。
(2)分离过程中采取的主要操作名称为____ 。
(3)碱解时发生反应的化学方程式为____ ,流程图中可循环利用的物质为____ 。
(4)电石常用CaO与碳素材料在1800~2200℃的高温下制备,甲烷在高温下(1300~1500℃和氧不足的条件下燃烧时所放出的热量可使甲烷发生反应生成乙炔。与电石制乙炔相比,该方法的优点是___ (写一条即可),若标准状况下22.4m3甲烷可得到聚乙烯醇产品13.2kg,则甲烷的转化率为___ 。
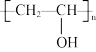 )是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
)是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
已知:①电石气中通常含有H2S、PH3等杂质②电石气通入次氯酸钠溶液后反应后,溶液仍澄清③乙炔较易与羧酸反应生成酯
回答下列问题:
(1)制取电石气时用饱和食盐水代替水的目的是
(2)分离过程中采取的主要操作名称为
(3)碱解时发生反应的化学方程式为
(4)电石常用CaO与碳素材料在1800~2200℃的高温下制备,甲烷在高温下(1300~1500℃和氧不足的条件下燃烧时所放出的热量可使甲烷发生反应生成乙炔。与电石制乙炔相比,该方法的优点是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是以乙炔(结构简式为 )为主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡胶的转化关系图。
)为主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡胶的转化关系图。
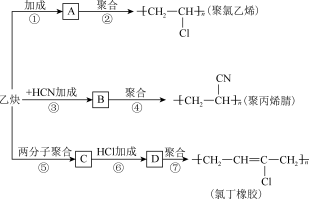
(1)写出A、B、C、D四种物质的结构简式:
A:________ ,B:________ ,C:________ ,D:________ 。
(2)写出有关反应的化学方程式:
②:____________ ;
③:_____________ ;
⑤:___________ ;
⑦:_________ 。
 )为主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡胶的转化关系图。
)为主要原料合成聚氯乙烯、聚丙烯腈和氯丁橡胶的转化关系图。
(1)写出A、B、C、D四种物质的结构简式:
A:
(2)写出有关反应的化学方程式:
②:
③:
⑤:
⑦:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定电石样品中CaC2的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。
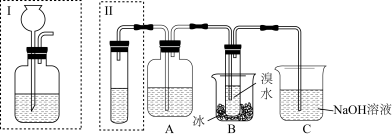
(1)A瓶中的液体可以从酸性KMnO4溶液和CuSO4溶液中选择,应该选择_______ ,它的作用是_______ 。
(2)写出实验室制取乙炔的化学方程式_______ 。
(3)装置C中NaOH作用是_______ ;
(4)装置B中的现象是_______ , B装置中发生的反应方程式_______ 。

(1)A瓶中的液体可以从酸性KMnO4溶液和CuSO4溶液中选择,应该选择
(2)写出实验室制取乙炔的化学方程式
(3)装置C中NaOH作用是
(4)装置B中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】草酸及其盐在生产生活中有重要用途。某兴趣小组计划制备草酸并研究其性质。
I.草酸的制备
将一定量的催化剂加入100mL质量分数为50%的硝酸中,待溶解后,倒入三颈烧瓶,组装好的实验装置如图所示,缓慢均匀地通入用电石与水反应产生的乙炔气体,反应结束后,将反应后的产品及母液倒出,冷却结晶、过滤,干燥得 。
。
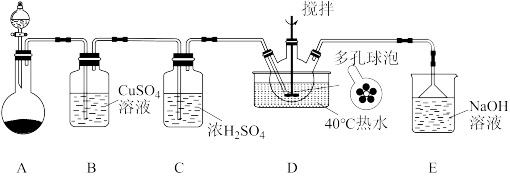
(1)装置A中选择的试剂组合最合理的是_______ (填标号);装置C除干燥外还有的作用是_______ 。
a.水、粉末状电石 b.饱和食盐水、粉末状电石
c.水、块状电石 d.饱和食盐水、块状电石
(2)实验中草酸的产量与起始硝酸的质量分数的变化关系如图所示,A点后草酸的产量下降的原因是_______ 。
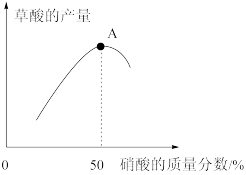
II.草酸纯度的测定
称取2.500g草酸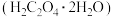 样品,配成100mL溶液。准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,用
样品,配成100mL溶液。准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,用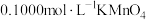 标准溶液进行滴定。
标准溶液进行滴定。
(3)下列仪器中,在配制该溶液时一定需要的是_______ (填对应仪器名称)。
A.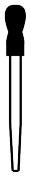 B.
B. C.
C.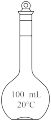 D.
D.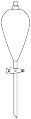 E.
E.
(4)在滴定过程中发现,刚滴下少量 标准溶液时,溶液紫红色并没有马上褪去,将锥形瓶摇动一段时间后,紫红色才慢慢消失,再继续滴加时,紫红色又很快褪去,出现该现象的可能原因是
标准溶液时,溶液紫红色并没有马上褪去,将锥形瓶摇动一段时间后,紫红色才慢慢消失,再继续滴加时,紫红色又很快褪去,出现该现象的可能原因是_______ ;写出滴定过程中发生反应的离子方程式:_______ 。
(5)记录的实验数据如表所示,则此草酸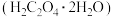 样品的纯度为
样品的纯度为_______ %。
I.草酸的制备
将一定量的催化剂加入100mL质量分数为50%的硝酸中,待溶解后,倒入三颈烧瓶,组装好的实验装置如图所示,缓慢均匀地通入用电石与水反应产生的乙炔气体,反应结束后,将反应后的产品及母液倒出,冷却结晶、过滤,干燥得
 。
。
(1)装置A中选择的试剂组合最合理的是
a.水、粉末状电石 b.饱和食盐水、粉末状电石
c.水、块状电石 d.饱和食盐水、块状电石
(2)实验中草酸的产量与起始硝酸的质量分数的变化关系如图所示,A点后草酸的产量下降的原因是

II.草酸纯度的测定
称取2.500g草酸
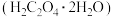 样品,配成100mL溶液。准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,用
样品,配成100mL溶液。准确量取25.00mL所配溶液于锥形瓶中,加少量硫酸酸化,用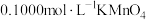 标准溶液进行滴定。
标准溶液进行滴定。(3)下列仪器中,在配制该溶液时一定需要的是
A.
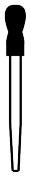 B.
B. C.
C.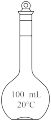 D.
D.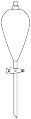 E.
E.
(4)在滴定过程中发现,刚滴下少量
 标准溶液时,溶液紫红色并没有马上褪去,将锥形瓶摇动一段时间后,紫红色才慢慢消失,再继续滴加时,紫红色又很快褪去,出现该现象的可能原因是
标准溶液时,溶液紫红色并没有马上褪去,将锥形瓶摇动一段时间后,紫红色才慢慢消失,再继续滴加时,紫红色又很快褪去,出现该现象的可能原因是(5)记录的实验数据如表所示,则此草酸
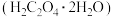 样品的纯度为
样品的纯度为| 序号 | 1 | 2 | 3 |
| 滴定前的的刻度/mL | 0.20 | 0.80 | 1.03 |
| 滴定后的的刻度/mL | 18.69 | 19.31 | 20.24 |
您最近一年使用:0次
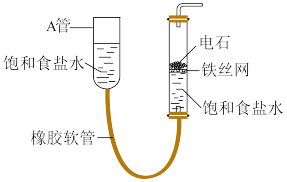
【推荐2】实验室用以下改进装置快速制备乙炔气体:
(1)电石的主要成分的电子式为_______ ,与饱和食盐水发生反应的化学方程式为_______ 。
(2)若要使反应停止,应_______ (“向上”或“向下”)移动A管。
(3)因电石中含有某些杂质,制备的乙炔气体中往往混有少量的PH3和H2S,除去乙炔中的这两种杂质气体,应使混合气体通过盛有足量_______ (填试剂名称)的洗气瓶。
(4)纯净的乙炔通入含少量 的
的 溶液中观察到的现象是
溶液中观察到的现象是_______ ,该过程发生的主要反应的化学方程式为_______ ;此反应的有机产物_______ (填“能”或“不能”)发生加聚反应。
(1)电石的主要成分的电子式为
(2)若要使反应停止,应
(3)因电石中含有某些杂质,制备的乙炔气体中往往混有少量的PH3和H2S,除去乙炔中的这两种杂质气体,应使混合气体通过盛有足量
(4)纯净的乙炔通入含少量
 的
的 溶液中观察到的现象是
溶液中观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】乙炔是有机合成中重要的工业原料。某同学利用如图所示装置以电石(含有少量 、
、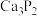 )为原料制取乙炔并验证乙炔的化学性质。
)为原料制取乙炔并验证乙炔的化学性质。 ,当溶液变成无色时,得到品红亚硫酸溶液。品红亚硫酸溶液遇到醛基,又会由无色变成红色。
,当溶液变成无色时,得到品红亚硫酸溶液。品红亚硫酸溶液遇到醛基,又会由无色变成红色。
请回答下列问题:
(1)仪器甲的名称为___________ ,实验室制取乙炔的化学方程式为____________ 。
(2)本实验的关键是控制产生乙炔的速率。为了控制反应速率,通常用____________ (填试剂名称)替代纯水,并逐滴加入从而得到平稳的乙炔气流。
(3)装置B中盛装的是___________ (填试剂名称),其作用是___________________ 。
(4)打开 ,当乙炔气流稳定时,微热装置C,使液体的温度控制在
,当乙炔气流稳定时,微热装置C,使液体的温度控制在 ,乙炔通过催化剂溶液后,开始有些浑浊,然后逐渐变澄清。该过程中发生的主要反应的反应类型为
,乙炔通过催化剂溶液后,开始有些浑浊,然后逐渐变澄清。该过程中发生的主要反应的反应类型为__________ ,当看到________________ 现象时,说明装置C中有乙醛生成。
 、
、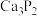 )为原料制取乙炔并验证乙炔的化学性质。
)为原料制取乙炔并验证乙炔的化学性质。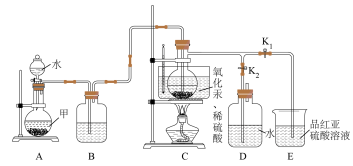
 ,当溶液变成无色时,得到品红亚硫酸溶液。品红亚硫酸溶液遇到醛基,又会由无色变成红色。
,当溶液变成无色时,得到品红亚硫酸溶液。品红亚硫酸溶液遇到醛基,又会由无色变成红色。请回答下列问题:
(1)仪器甲的名称为
(2)本实验的关键是控制产生乙炔的速率。为了控制反应速率,通常用
(3)装置B中盛装的是
(4)打开
 ,当乙炔气流稳定时,微热装置C,使液体的温度控制在
,当乙炔气流稳定时,微热装置C,使液体的温度控制在 ,乙炔通过催化剂溶液后,开始有些浑浊,然后逐渐变澄清。该过程中发生的主要反应的反应类型为
,乙炔通过催化剂溶液后,开始有些浑浊,然后逐渐变澄清。该过程中发生的主要反应的反应类型为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
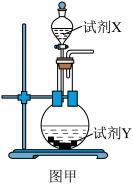
【推荐1】氯化亚铜难溶于水,能溶于氨水生成络合物。在气体分析中用于一氧化碳和乙炔的测定。某化学兴趣小组设计实验制备并探究氯化亚铜与乙炔的反应(装置如下,部分夹持装置省略)。
查阅资料:
① 与乙炔气体反应得到暗红色
与乙炔气体反应得到暗红色 沉淀。
沉淀。
② 也可与
也可与 发生反应。
发生反应。
I.制备氯化亚铜:小组同学拟用二氧化硫和硫酸铜、氯化钠溶液反应制备氯化亚铜。
(1)图甲中盛放试剂X的仪器名称是___________ ,若试剂Y为亚硫酸钠,则试剂X为___________ 。
(2)检验二氧化硫气体的操作是___________ 。
Ⅱ.探究氯化亚铜与乙炔的反应:小组同学利用电石(主要成分 ,杂质为
,杂质为 )与
)与 反应制
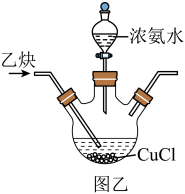
反应制 ,并将提纯后的乙炔通入图乙装置,验证乙炔与氯化亚铜的反应。
,并将提纯后的乙炔通入图乙装置,验证乙炔与氯化亚铜的反应。
(3)小组同学将电石与水反应产生的气体通入溴水,溴水___________ (填现象),___________ (填“能”或“不能”)证明反应生成了乙炔,理由是___________ 。
(4)提纯乙炔的试剂通常选用___________ (填化学式)溶液。
(5)向三颈烧瓶中逐滴滴加氨水,白色固体逐渐溶解为 ,判断氨水过量的方法是
,判断氨水过量的方法是___________ 。停止滴加氨水,通入净化后的乙炔,烧瓶底部有暗红色沉淀析出,写出生成沉淀的离子方程式:___________ 。

查阅资料:
①
 与乙炔气体反应得到暗红色
与乙炔气体反应得到暗红色 沉淀。
沉淀。②
 也可与
也可与 发生反应。
发生反应。I.制备氯化亚铜:小组同学拟用二氧化硫和硫酸铜、氯化钠溶液反应制备氯化亚铜。
(1)图甲中盛放试剂X的仪器名称是
(2)检验二氧化硫气体的操作是
Ⅱ.探究氯化亚铜与乙炔的反应:小组同学利用电石(主要成分
 ,杂质为
,杂质为 )与
)与 反应制
反应制 ,并将提纯后的乙炔通入图乙装置,验证乙炔与氯化亚铜的反应。
,并将提纯后的乙炔通入图乙装置,验证乙炔与氯化亚铜的反应。
(3)小组同学将电石与水反应产生的气体通入溴水,溴水
(4)提纯乙炔的试剂通常选用
(5)向三颈烧瓶中逐滴滴加氨水,白色固体逐渐溶解为
 ,判断氨水过量的方法是
,判断氨水过量的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用乙醇制取乙烯,用电石(主要成分为CaC2,含少量CaS)制取乙炔。
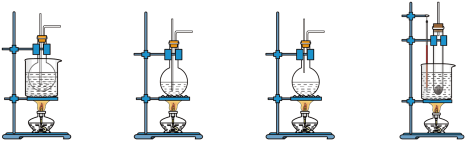
(1)实验室制取乙烯的化学方程式为_____________________________ ,可用于制取乙烯的发生装置是_______ 。(选填编号)
(2)制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是________ 。
a 吸水性 b 脱水性 c 强氧化性 d 酸性
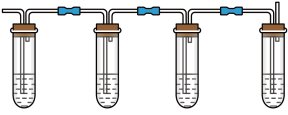
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
①_______________ ,②_______________ ,③_______________ ,④______________ 。
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
(3)实验室制备乙炔的化学反应方程式为_________________________________ 。实验室制乙炔时为避免电石和水反应过于激烈,除用分液漏斗控制滴速外,通常还可用_________ 代替水。为除去乙炔中混有的少量硫化氢杂质,可将气体通过___________ (选填编号)。
a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
(1)实验室制取乙烯的化学方程式为

a b c d
(2)制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是
a 吸水性 b 脱水性 c 强氧化性 d 酸性

① ② ③ ④
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
①
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
(3)实验室制备乙炔的化学反应方程式为
a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
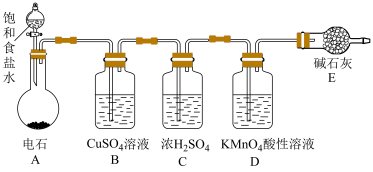
【推荐3】为测定乙炔的相对分子质量,某小组利用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。________ 。
(2)装置A中发生反应的化学方程式是________ 。
(3)B中的 溶液作用是
溶液作用是________ 。
(4)小组查阅资料得出:乙炔能与硫酸酸化的 反应生成
反应生成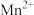 和
和 ,该反应的离子方程式是
,该反应的离子方程式是________ 。
(5)实验前D中含有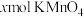 的酸性溶液,实验时向D中通入一定量的乙炔直至
的酸性溶液,实验时向D中通入一定量的乙炔直至 酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重
酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重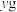 ,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):
,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):________ 。
(6)另一活动小组的同学认为上述实验装置存在不足,则改进的措施是________ 。
(2)装置A中发生反应的化学方程式是
(3)B中的
 溶液作用是
溶液作用是(4)小组查阅资料得出:乙炔能与硫酸酸化的
 反应生成
反应生成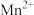 和
和 ,该反应的离子方程式是
,该反应的离子方程式是(5)实验前D中含有
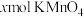 的酸性溶液,实验时向D中通入一定量的乙炔直至
的酸性溶液,实验时向D中通入一定量的乙炔直至 酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重
酸性溶液恰好完全褪色,实验完毕后装置D及E的总质量共增重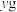 ,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):
,通过计算求出所测乙炔的相对分子质量(用含字母x、y的代数式表示):(6)另一活动小组的同学认为上述实验装置存在不足,则改进的措施是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】锰酸钾是一种用途广泛的强氧化剂。某课外小组利用碱性高锰酸钾溶液在65℃下反应制备锰酸钾,拟用如图所示的装置(夹持装置略)制备:
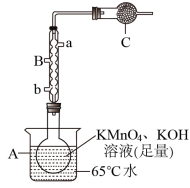
查阅资料:①MnO 溶液呈绿色;②锰酸钾在酸性溶液(即使是碳酸等弱酸性溶液)中能完全转化为高锰酸钾和二氧化锰。回答下列问题:
溶液呈绿色;②锰酸钾在酸性溶液(即使是碳酸等弱酸性溶液)中能完全转化为高锰酸钾和二氧化锰。回答下列问题:
(1)仪器B的名称是_______ ,冷凝水进口是_______ 。(填“a”或“b”)
(2)仪器C中盛放的药品是_______ 。
(3)反应结束时,A中烧瓶中出现的现象是_______ ,其反应的化学方程式是_______ ;若温度过高,产品中会含有_______ (填化学式)杂质。
(4)本实验获得产品时还要经过一系列操作,其中洗涤产品的蒸馏水需要预处理,预处理的简单方法是_______ 。

查阅资料:①MnO
 溶液呈绿色;②锰酸钾在酸性溶液(即使是碳酸等弱酸性溶液)中能完全转化为高锰酸钾和二氧化锰。回答下列问题:
溶液呈绿色;②锰酸钾在酸性溶液(即使是碳酸等弱酸性溶液)中能完全转化为高锰酸钾和二氧化锰。回答下列问题:(1)仪器B的名称是
(2)仪器C中盛放的药品是
(3)反应结束时,A中烧瓶中出现的现象是
(4)本实验获得产品时还要经过一系列操作,其中洗涤产品的蒸馏水需要预处理,预处理的简单方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】精对苯二甲酸(PTA)是生产聚酯纤维的重要化工原料。生产过程产生的氧化残渣主要含有苯甲酸、对苯二甲酸、钴锰催化剂等。采用以下工艺流程可实现PTA残渣中有效成分苯甲酸和Co2+、Mn2+的回收与纯化,达到废物再利用的目的。
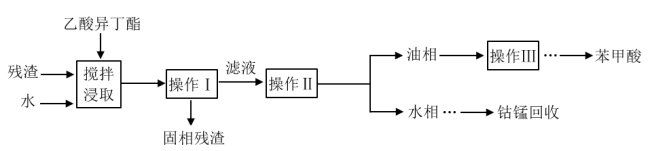
(1)操作I的方法是______ ;实验室进行操作Ⅱ主要用的玻璃仪器有_________ 。
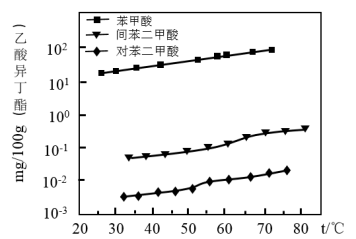
(2)判定乙酸异丁酯可用于浸取并有效回收苯甲酸的理由是_________ 。
(3)从上表所列实验数据可知苯甲酸在乙酸异丁酯中的溶解过程是_________ (填“放热”或“吸热”)过程。
(4)操作Ⅲ为蒸馏,蒸出的溶剂可返回_________ 工序循环使用。
(5)钴锰回收时常采用Na,S沉淀法将钴沉淀为CoS,若油水分离后的溶液经蒸发浓缩后,Co2+和Mn2+的浓度均为0.1mol∙L-1,计算说明当Co2+完全沉淀时产生的固体中不含MnS,支持这个结论的数学关系式是_________ 。[已知:Ksp(CoS)=2×10-25,Ksp(MnS)=2×10-13,完全沉淀指溶液中离子浓度小于10-5mol∙L-1]
(6)得到的CoS通过硫酸化焙烧转变为水溶性的CoSO4,其化学方程式为_________ 。


| 序号 | 浸取温度/℃ | 进料质量比溶剂:水:干残渣 | 苯甲酸浸取率/% |
| 1 | 30 | 4∶1∶1 | 87.48 |
| 2 | 40 | 4∶1∶1 | 90.33 |
| 3 | 50 | 4∶1∶1 | 90.81 |
(1)操作I的方法是
(2)判定乙酸异丁酯可用于浸取并有效回收苯甲酸的理由是
(3)从上表所列实验数据可知苯甲酸在乙酸异丁酯中的溶解过程是
(4)操作Ⅲ为蒸馏,蒸出的溶剂可返回
(5)钴锰回收时常采用Na,S沉淀法将钴沉淀为CoS,若油水分离后的溶液经蒸发浓缩后,Co2+和Mn2+的浓度均为0.1mol∙L-1,计算说明当Co2+完全沉淀时产生的固体中不含MnS,支持这个结论的数学关系式是
(6)得到的CoS通过硫酸化焙烧转变为水溶性的CoSO4,其化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】兴趣小组用下列装置制取气体,请回答下列问题:
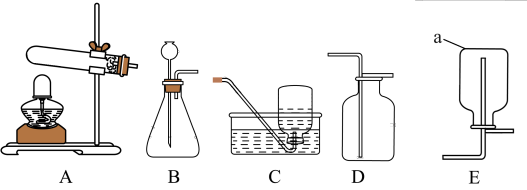
(1)写出仪器a的名称:___________ 。
(2)实验室制取二氧化碳气体,应选择的发生装置是___________ (填字母),发生反应的化学方程式为___________ 。
(3)可以用装置D收集氧气,其原因是___________ 。
(4)用装置A制取氧气,反应方程式为___________ 。

(1)写出仪器a的名称:
(2)实验室制取二氧化碳气体,应选择的发生装置是
(3)可以用装置D收集氧气,其原因是
(4)用装置A制取氧气,反应方程式为
您最近一年使用:0次



