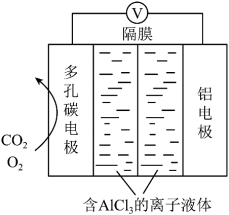
(1)电池的总反应式为
(2)电池的正极反应式:2CO2+2e-=C2O
 (草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:
(草酸根),正极反应过程中,O2是催化剂,催化过程可表示为:①6O2+6e-=6O

②……
写出反应②的离子方程式:
相似题推荐
 固体 ⑩熔融的Na2O,根据所学知识回答下列问题:
固体 ⑩熔融的Na2O,根据所学知识回答下列问题:(1)上述物质在所处的状态下,可以导电的有
(2)②在水溶液中电离方程式为:
(3)④电离方程式为
(4)已知H3PO3是二元酸,写出其与足量NaOH反应的化学方程式
(5)下列各项与胶体性质有关的有
a.卤水点豆腐 b.明矾净水 c.油水分离 d.血液透析 e.酸碱中和 f.三角洲形成 g.制备氢氧化铁沉淀 h.臭氧消毒
Ⅱ.写出下列反应的离子方程式
(6)NH4Fe(SO4)2与足量NaOH溶液反应:
(7)澄清石灰水与少量小苏打溶液反应:
 、Mg2+、Fe3+、Al3+、SO
、Mg2+、Fe3+、Al3+、SO 、HCO
、HCO 等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。
等离子,当向溶液中加入一定浓度NaOH溶液时,生成沉淀的物质的量随加入NaOH溶液的体积关系如图所示。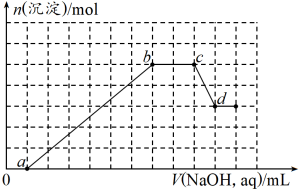
请回答下列问题:
(1)该无色溶液中一定不存在的离子有
(2)ab段生成的沉淀的化学式为
(3)bc段表明溶液中有
(4)cd段沉淀减少的离子方程式为
(5)原溶液中一定含有的离子的物质的量之比为
 ):n(Mg2+)=1:1:1]
):n(Mg2+)=1:1:1]

(1)下列说法正确的是
a.火山口常有硫单质可能的原因是2H2S+SO2=3S+2H2O
b.转化过程中硫元素既发生氧化反应又发生还原反应
c.含硫矿物中硫元素均为-2价
(2)写出SO2形成酸雨的化学方程式:
(3)工业生产也会产生大量二氧化硫进入大气,污染环境,有多种方法可用于SO2的脱除。
①氨法脱硫。该方法是一种高效低耗能的湿法脱硫方式,利用氨水吸收废气中的SO2,并在富氧条件下转化为硫酸铵,该过程中被氧化的元素是
②用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是
③酸性条件下,用MnO2进行脱硫处理的原理如下图所示。

i.上述过程中可以循环使用的是
ii.脱硫最终产物的化学式是
(1)煤液化是
(2)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:
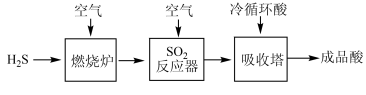
①SO2反应器中的化学方程式是
②生产过程中的尾气需要测定SO2的含量符合标准才能排放。已知有V L(已换算成标准状况)尾气,通入足量H2O2吸收再加足量BaCl2溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到b g沉淀。H2O2吸收SO2的化学方程式是
(3)H2S还可用于回收单质硫。含有H2S和空气的尾气按一定流速通入酸性FeCl3溶液,可实现空气脱硫,得到单质硫。FeCl3溶液吸收H2S过程中,溶液中的n(Fe3+)、被吸收的n(H2S) 随时间t的变化如图:
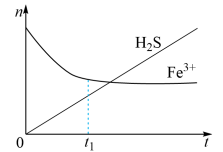
① 由图中信息可知,0 ~ t1时,一定发生的反应是
②t1以后,溶液中n (Fe3+ ) 保持基本不变,原因是
【推荐3】中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。

已知:Fe2+与铁氰化钾(K3[Fe(CN)6])溶液生成蓝色沉淀。
(1)铁器在具有O2、
(2)铁器表面氧化层的成分有多种,性质如下:
成分 | Fe3O4 | FeO(OH) | FeOCl |
性质 | 致密 | 疏松 | 疏松 |
现通过以下实验检验铁器表面氧化层中铁元素的价态:
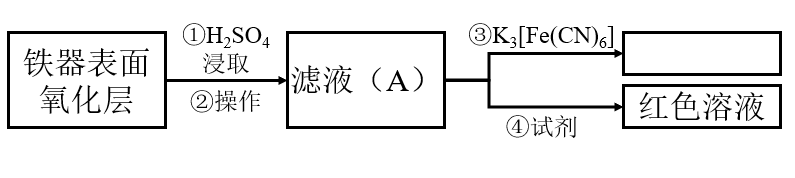
①步骤②的操作是
②步骤④的试剂是
(3)铁器的锈蚀经过了一系列复杂的化学变化,请完成以下反应:
①Fe(OH)2被空气氧化为Fe3O4的化学方程式是
②在有氧条件下,Fe3O4在含Cl-溶液中会转化为FeOCl,将相关反应的离子方程式补充完整:
4Fe3O4+O2+ ___________+
___________+ H2O=
H2O= FeOCl+
FeOCl+ ___________。
___________。
(4)化学修复可以使FeOCl最终转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤至无Cl-。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOCl
②Na2SO3的作用是
③检验FeOCl转化完全的操作和现象是
(1)利用反应
 构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。
构成电池的方法,既能实现有效消除氮氧化物的排放,又能提供电能,装置如图所示。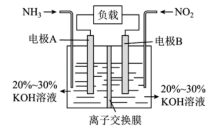
①A电极的电极反应式为
②下列关于该电池的说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电池工作一段时间,溶液的
 不变
不变D.当有
 被处理时,转移电子物质的量为
被处理时,转移电子物质的量为
(2)以含
 废气为原料,用电化学方法制取硫酸。装置如图。
废气为原料,用电化学方法制取硫酸。装置如图。
写出负极电极反应式
(2)我国首创以铝空气海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是
(3)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO
 -4e-=4CO2,正极反应式为
-4e-=4CO2,正极反应式为【推荐3】氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图(Ⅰ)所示。
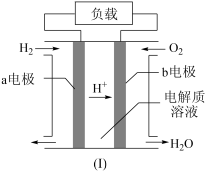
(1)若该电池中的电解质溶液是稀硫酸溶液,则 a 电极上发生反应的电极反应式为
(2)b 电极是该电池的
(3)当转移 0.2mol 电子时,需要消耗标况下的氢气体积是
(4)如图 (Ⅱ)所示,是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:

①当电极 a 为 Fe,电极 b 为 Cu,电解质溶液为浓 HNO3溶液时,一段时间后,形成稳定电流的原电池的总反应的离子方程式为
②燃料电池的工作原理是将燃料和氧化剂(如 O2)反应所产生的化学能转化为电能。现设计一燃料电池,以电极 a 为正 极,电极 b 为负极,CH4为燃料,采用 NaOH 溶液为电解液,则 CH4通入的电极反应式为
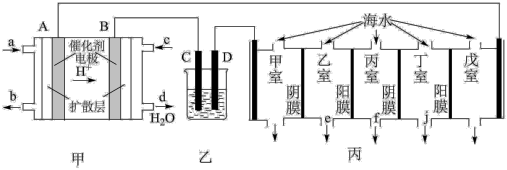
(1)甲装置中c口通入的气体是
(2)乙装置用来模拟精炼和电镀。
①若用于粗铜的精炼,装置中电极C是
②若用于电镀金属银,则电镀液宜使用
(3)电渗析法是海水淡化的常用方法,某地海水中主要离子的含量如表,现利用“电渗析法”进行淡化,技术原理如图丙所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。
| 离子 | Na+ | K+ | Ca2+ | Mg2+ | Cl- |  |  |
| 含量/mg•L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |
②产生淡水的出水口为
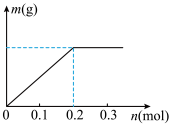
(4)若乙装置中C,D都是惰性电极,溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol的混合溶液,通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是
 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸。则正极的反应式是(2)一种熔融碳酸盐燃料电池原理示意如图所示:

电池工作时,外电路上电流的方向应从电极
(3)将两铂片插入KOH溶液中作为电极,在两极区分别通入甲醇(CH3OH)和氧气构成燃料电池,则通入甲醇的电极是原电池的
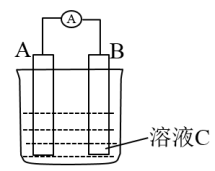
(1)甲同学认为,所有的氧化还原反应都可以设计成原电池,你是否同意
(2)乙同学依据氧化还原反应:2Ag+ +Cu=Cu2+ + 2Ag设计的原电池如图所示:
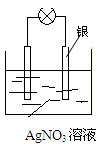
①负极的材料是
②外电路中的电子是从
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是
④请指出该原电池装置的一个缺点:

 、
、 、
、 三种无色溶液,只用一种试剂可把它们鉴别出来:
三种无色溶液,只用一种试剂可把它们鉴别出来:


