NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第____ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的____ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是___ (填“H”或“O”)。
(4)Na的最高价氧化物的化学式为____ 。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
(4)Na的最高价氧化物的化学式为
更新时间:2022-09-13 20:06:02
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】联合国将2019年定为“国际化学元素周期表年”,2018年中国化学会制作了新版周期表,包含118种元素。回答下列问题:
(1)碳元素在周期表中的位置是______ 。
(2)将硅的元素符号填写在上述周期表相应的空格中_______ 。
(3)在上述周期表中,用实线画出 周期表的上方边界 ________ 。
(4)从原子结构角度解释碳化硅中碳元素显负价的原因______ 。
(5)第118号元素为Og(中文名“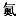 ”,ào),下列说法
”,ào),下列说法不正确 的是______ 。
a.Og是第七周期0族元素 b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强 d.中子数为179的Og核素符号是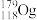
(6)已知X与Y是位于相邻周期的同主族元素。某温度下,X、Y的单质与H2化合生成气态氢化物的平衡常数分别为KX =9.7×1012、KY =5.6×107。Y是______ (填元素符号),判断理由是______ 。
| X | |||||||||||||||||
(2)将硅的元素符号填写在上述周期表相应的空格中
(3)在上述周期表中,用
(4)从原子结构角度解释碳化硅中碳元素显负价的原因
(5)第118号元素为Og(中文名“
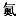 ”,ào),下列说法
”,ào),下列说法a.Og是第七周期0族元素 b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强 d.中子数为179的Og核素符号是
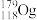
(6)已知X与Y是位于相邻周期的同主族元素。某温度下,X、Y的单质与H2化合生成气态氢化物的平衡常数分别为KX =9.7×1012、KY =5.6×107。Y是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】新疆也要建造磁悬浮列车了。在磁悬浮列车制造过程中将使用大量含钇(Y)元素的超导材料。钇(Y)元素在元素周期表中的信息如图所示:_______ 个质子,左图中89.91表示的是_______ ;
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据_______ 个电子层;
(3)钇元素形成氧化物的化学式是_______ 。
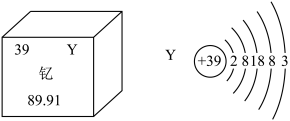
(2)电子离核越远能量越高,越容易在反应中失去,Y的核外电子其占据
(3)钇元素形成氧化物的化学式是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】比较物质的性质(用化学式和“>”、“<”表示)
(1)Na、Mg的单质与水反应的剧烈程度:___________
(2)Si、P的单质与氢气化合的难易程度:___________
(3)O、S元素的气态氢化物的稳定性:___________
(4)P、Cl元素的气态氢化物的稳定性:___________
(5)Be、Mg元素的最高价氧化物对应水化物的碱性:___________
(6)S、Cl元素的最高价氧化物对应水化物的酸性:___________
(7)N、P元素的最高价氧化物对应水化物的酸性:___________
(1)Na、Mg的单质与水反应的剧烈程度:
(2)Si、P的单质与氢气化合的难易程度:
(3)O、S元素的气态氢化物的稳定性:
(4)P、Cl元素的气态氢化物的稳定性:
(5)Be、Mg元素的最高价氧化物对应水化物的碱性:
(6)S、Cl元素的最高价氧化物对应水化物的酸性:
(7)N、P元素的最高价氧化物对应水化物的酸性:
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第________ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
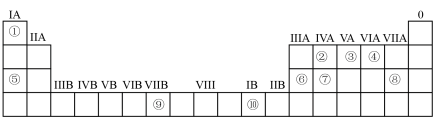
【推荐1】下表为元素周期表的一部分,请参照元素①—⑩在表中的位置,回答下列问题:___________ (用元素符号表示)。
(2)④、⑤、⑥的原子半径由大到小的顺序为___________ (用元素符号表示);
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________ (用化学式表示)。
(4)①、④、⑤、⑧中的某些 元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________ 。
(5)第一电离能 :
: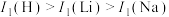 ,原因是
,原因是___________ 。
(6)基态⑧原子占据的最高能级的电子云轮廓图的形状是___________ 形;基态⑨原子的价层电子排布的轨道表示式为___________ ;元素⑩属于___________ 区(填“s”、“d”、“ds”或“p”)。
(7)由④元素形成的常见物质有很多,例如: 、
、 、
、 等,基态④原子的核外电子排布式是
等,基态④原子的核外电子排布式是___________ ,对 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测: 分子中
分子中___________ (填字母序号),确定其结构一定不是甲。
a. 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角
(2)④、⑤、⑥的原子半径由大到小的顺序为
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(4)①、④、⑤、⑧中的
(5)第一电离能
 :
: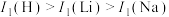 ,原因是
,原因是(6)基态⑧原子占据的最高能级的电子云轮廓图的形状是
(7)由④元素形成的常见物质有很多,例如:
 、
、 、
、 等,基态④原子的核外电子排布式是
等,基态④原子的核外电子排布式是 分子结构的研究,曾有以下推测:
分子结构的研究,曾有以下推测: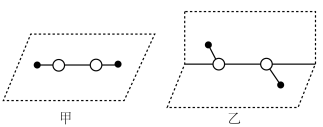
 分子中
分子中a.
 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
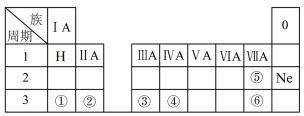
(1)元素⑤的符号是___________ 。
(2)③的最高价氧化物对应的水化物的化学式为___________ (填化学式)。
(3)④和⑥两种元素原子半径的大小关系:④___________ ⑥(填“>”或“<”)。
(4)①和②两种元素金属性强弱关系:①___________ ②(填“>”或“<”)。
(5)⑥的氢化物的电子式为___________ 。
(6)①的最高价氧化物对应的水化物与单质③的反应方程式:___________ 。

(1)元素⑤的符号是
(2)③的最高价氧化物对应的水化物的化学式为
(3)④和⑥两种元素原子半径的大小关系:④
(4)①和②两种元素金属性强弱关系:①
(5)⑥的氢化物的电子式为
(6)①的最高价氧化物对应的水化物与单质③的反应方程式:
您最近一年使用:0次




