请根据所学知识,回答下列问题:
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
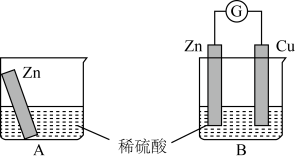
(1)B中Zn板是___________ 极,正极发生的电极反应是___________
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
(3)在B中,当导线中有1 mol电子通过时,理论上的两极变化是___________。
(4)若将反应2Fe3++Cu=Cu2++2Fe2+设计成原电池,写出正极电极反应式___________ ;
(5)写出碱性氢氧燃料电池正极电极反应式___________
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式___________
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:___________
某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
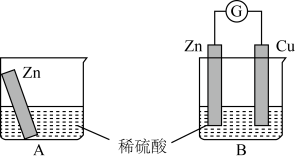
(1)B中Zn板是
(2)该小组同学反思原电池的原理,其中观点正确的是___________;
| A.原电池反应的过程中一定有电子转移 |
| B.电极一定不能参加反应 |
| C.原电池装置中的电子流向:负极→外线路→正极→电解质→负极 |
| D.氧化反应和还原反应可以拆开在两极发生 |
| A.锌片溶解32.5 g | B.锌片增重32.5 g |
| C.铜片上析出2 g H2 | D.铜片上析出1 mol H2 |
(5)写出碱性氢氧燃料电池正极电极反应式
(6)写出酸性乙醇(C2H5OH)燃料电池负极电极反应式
(7)写出铜片和铝片插入浓硝酸溶液中的正极反应为:
更新时间:2022-08-18 17:25:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)今有氢氧燃料电池,则正极通入的气体是________ ,负极通入的气体是________ ,电解质溶液为稀硫酸时,电极反应式为:正极____________ ;负极___________ ,电池的总反应式为__________ ;
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极___________ 。
(2)如把H2改为甲烷、KOH作导电物质,则电极反应式为:负极
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:
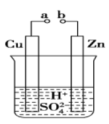
(1)a和b用导线连接,Zn极为原电池__________ 极(填“正”或“负”),Cu极发生__________ (填“氧化”或“还原”),溶液中SO42-移向_________ (填“Cu”或“Zn”)极
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.4mol电子,则理论上Zn片应溶解__________ g
(3)有同学想把Ba(OH)2·8H2O晶体与NH4NO3晶体的反应设计成原电池,你认为是否可行?__________ (填“是”或“否”),理由是 __________ 。

(1)a和b用导线连接,Zn极为原电池
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.4mol电子,则理论上Zn片应溶解
(3)有同学想把Ba(OH)2·8H2O晶体与NH4NO3晶体的反应设计成原电池,你认为是否可行?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电池在我们的生活中有着重要的应用,请回答下列问题:
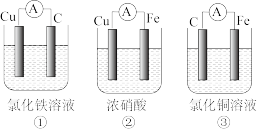
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ (填序号)。若构建原电池时两个电极的质量相等,当导线中通过0.1mol电子时,两个电极的质量差为_______ 。
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
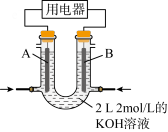
实验测得OH-向B电极定向移动,则_______ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_______ 。当消耗甲烷的体积为33.6L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为_______ 。
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移向_______ (填“电极a”或“电极b”),负极发生的电极反应式为_______ 。

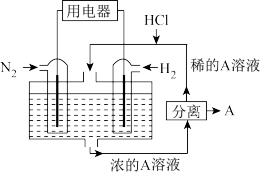
(4)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。电池正极的电极反应式是_______ 。
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH-向B电极定向移动,则
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移向

(4)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。电池正极的电极反应式是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学电源在生产生活中有着广泛的应用,同学们常常通过设计实验和查阅资料的方式学习化学电源的相关知识。
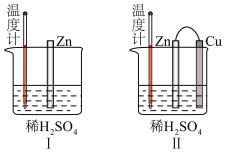
(1)甲同学为了解反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。____ Ⅱ(>、<或=),温度计的示数Ⅰ___ II(>、<或=)。
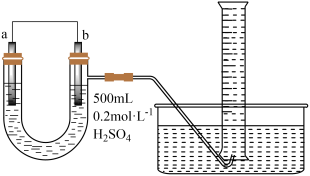
(2)乙同学用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为________ ,当量筒中收集到 336mL(标准状况下)气体时,通过导线的电子的物质的量为_______ 。
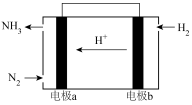
(3)丙同学了解到科学家正在研究利用原电池原理常温常压下合成氨,在该装置如图,电极 a 为____ 极(填“正”或“负”)。_____ ,电解质溶液为_____ ,负极的电极反应式为_____ 。
(1)甲同学为了解反应中的能量转化,设计了一组对比实验(实验装置如图Ⅰ和图Ⅱ)。
(2)乙同学用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为

(3)丙同学了解到科学家正在研究利用原电池原理常温常压下合成氨,在该装置如图,电极 a 为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一种新型的燃料电池可用于制取乙醛(CH3CHO),总反应式为 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
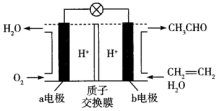
(1)该装置的能量转化形式为_______ 。
(2)a电极为燃料电池的_______ 极,该电极的电极反应式为_______ 。
(3)电池工作时,H+由_______ (填“a电极”或“b电极”,下同)移向_______ 。
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气_______ mL。
 ,电池的主要构成要素如图所示,请回答下列问题:
,电池的主要构成要素如图所示,请回答下列问题:
(1)该装置的能量转化形式为
(2)a电极为燃料电池的
(3)电池工作时,H+由
(4)生成3.3g乙醛时,需要消耗标准状况下的氧气
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】写出下列电极方程式书写:
(1)酸性电解质的条件下氢氧燃料电池负极的电极方程式________ ;正极的电极方程式____ ;
(2)氢氧化钾做电解质条件下写出甲醇(CH3OH)的燃料电池的负极的电极方程式____________________ ;正极的电极方程式____________ ;
(3)写出碱性锌锰原电池的负极的电极方程式_____________ ;正极的电极方程式_________ ;
(4)写出铅蓄电池放电的负极的电极反应方程式__________________ ;
(1)酸性电解质的条件下氢氧燃料电池负极的电极方程式
(2)氢氧化钾做电解质条件下写出甲醇(CH3OH)的燃料电池的负极的电极方程式
(3)写出碱性锌锰原电池的负极的电极方程式
(4)写出铅蓄电池放电的负极的电极反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)写出铝热法炼铁的化学方程式_________________________________ ;
(2)氢氧燃烧电池是一种高效低污染的新型电池,主要用于航天领域。它的电极材料一般为活化电极,具有很强的催化活性,如铂电极、活性炭电极等。电解质溶液一般为40%的KOH溶液。请写出电极反应式:
负极:______________________________
正极:______________________________
(3)在中国古代的《淮南万毕术》里,就有湿法炼铜:"曾青得铁则化为铜"的记载。曾青又名空青、白青、石胆、胆矾等,其实都是天然的硫酸铜。请根据“湿法炼铜”的反应设计一个原电池装置,在下边方框中画出原电池的装置图,标出正、负极和电解质溶液。

_____________________________________ 。
(2)氢氧燃烧电池是一种高效低污染的新型电池,主要用于航天领域。它的电极材料一般为活化电极,具有很强的催化活性,如铂电极、活性炭电极等。电解质溶液一般为40%的KOH溶液。请写出电极反应式:
负极:
正极:
(3)在中国古代的《淮南万毕术》里,就有湿法炼铜:"曾青得铁则化为铜"的记载。曾青又名空青、白青、石胆、胆矾等,其实都是天然的硫酸铜。请根据“湿法炼铜”的反应设计一个原电池装置,在下边方框中画出原电池的装置图,标出正、负极和电解质溶液。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(一)铅蓄电池是典型的二次电池,电池总反应式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________ 。当外电路通过1 mol电子时,理论上负极板的质量增加______ g。
(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为________________ ;
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为____________ 。
 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)利用8NH3+6NO2=7N2+12H2O可以消除氮氧化物的污染,若设计成原电池,使用2mol·L-1的KOH溶液为电解质溶液。该电池正极的电极反应式为_______ ,放电一段时间后,负极附近溶液pH将_______ (填“增大”、“减小”或“不变”)。
(2)一种熔融碳酸盐燃料电池原理示意如图所示
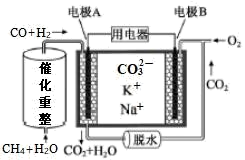
①写出催化重整的化学方程式_______ 。
②电池工作时, 向
向_______ (填A或B)极移动,电极A上H2参与的电极反应为:_______ 。
③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为_______ L。
(2)一种熔融碳酸盐燃料电池原理示意如图所示

①写出催化重整的化学方程式
②电池工作时,
 向
向③用电器中每转移2mol电子,理论上电极B处消耗的气体体积(标准状况下)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铝作为一种应用广泛的金属,在电化学领域发挥着举足轻重的作用。回答下列问题:
(1)某同学根据氧化还原反应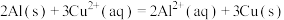 设计加图所示的原电池:
设计加图所示的原电池:
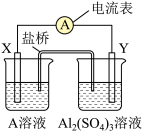
A溶液溶质的化学式为_______ ;电极Y材料的化学式为_______ ;盐桥中的阴离子向_______ (填化学式)溶液中移动。
(2)新型电池中的铝电池类型较多。
①Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为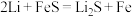 ,充电时锂电极连接电源的
,充电时锂电极连接电源的_______ 极,充电时阳极的电极反应式为_______ 。
②Al-AgO(氧化高银)电池可用作水下动力电源。该电池反应的化学方程式为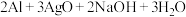
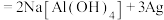 ,当电极上折出2.16 g Ag时,铝电极质量减少
,当电极上折出2.16 g Ag时,铝电极质量减少_______ g。
(1)某同学根据氧化还原反应
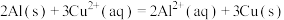 设计加图所示的原电池:
设计加图所示的原电池:
A溶液溶质的化学式为
(2)新型电池中的铝电池类型较多。
①Li-Al/FeS是一种二次电池,可用于车载电源,其电池总反应为
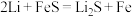 ,充电时锂电极连接电源的
,充电时锂电极连接电源的②Al-AgO(氧化高银)电池可用作水下动力电源。该电池反应的化学方程式为
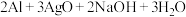
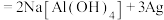 ,当电极上折出2.16 g Ag时,铝电极质量减少
,当电极上折出2.16 g Ag时,铝电极质量减少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)图1是高铁电池的模拟实验装置,放电时电池反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH
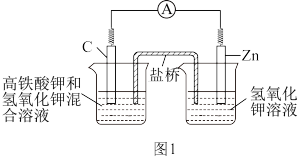

①该电池放电时正极的电极反应式为_________ 。
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向______ 移动(填“左”或“右”)。
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________________ 。
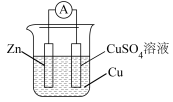
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为_______ 。
(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2 −4e−═4CO2
−4e−═4CO2
正极反应式____________ ;总电池反应_______________ 。


①该电池放电时正极的电极反应式为
②盐桥中含有饱和KCl溶液,此盐桥中氯离子向
③如图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)某同学在研究如图所示的原电池装置时,测得Zn电极质量减轻6.5 g,Cu电极质量增加4.8 g。通过导线的电子数与反应转移电子总数的比值定义为电池的能量转换效率,则该实验中电池的能量转换效率为

(3)熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
负极反应式:2CO+2
 −4e−═4CO2
−4e−═4CO2正极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】认真观察图中装置,回答下列问题:
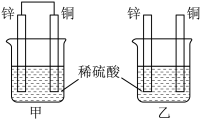
(1)下列说法中正确的是_________ (填序号)。
a.甲中铜片质量减少 b.乙中锌片质量减少
c.乙中铜片上没有明显变化 d.甲装置为原电池,乙装置为电解池
(2)同等条件下,两烧杯中产生气泡的速率:甲______ (填“>”“<”或“=”)乙。
(3)甲烧杯中锌电极为_______ (正极或负极),写出铜极的反应电极方程式_______ 。
(4)当甲中产生2.24 L(标准状况)气体时,理论上通过导线的电子数目为_______ mol。

(1)下列说法中正确的是
a.甲中铜片质量减少 b.乙中锌片质量减少
c.乙中铜片上没有明显变化 d.甲装置为原电池,乙装置为电解池
(2)同等条件下,两烧杯中产生气泡的速率:甲
(3)甲烧杯中锌电极为
(4)当甲中产生2.24 L(标准状况)气体时,理论上通过导线的电子数目为
您最近一年使用:0次



