石灰氮( )是一种氮肥,与土壤中的
)是一种氮肥,与土壤中的 反应生成氰胺(
反应生成氰胺( ),氰胺可进一步转化为尿素
),氰胺可进一步转化为尿素 。下列有关说法正确的是
。下列有关说法正确的是
 )是一种氮肥,与土壤中的
)是一种氮肥,与土壤中的 反应生成氰胺(
反应生成氰胺( ),氰胺可进一步转化为尿素
),氰胺可进一步转化为尿素 。下列有关说法正确的是
。下列有关说法正确的是A. 的电子式为 的电子式为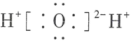 |
B.1个 分子中含3个 分子中含3个 键 键 |
C. 分子中 分子中 键与 键与 键的个数之比为 键的个数之比为 |
D.已知 中含有 中含有 键,1个 键,1个 分子中含有2个 分子中含有2个 键 键 |
21-22高二·全国·课时练习 查看更多[1]
更新时间:2022-08-29 06:23:31
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列可以成为形成物质世界多样性的原因有( )
①元素种类;②同位素;③化学键成键方式;④同分异构现象(化合物具有相同分子式,但结构不同);⑤同素异形现象
①元素种类;②同位素;③化学键成键方式;④同分异构现象(化合物具有相同分子式,但结构不同);⑤同素异形现象
| A.仅①②③ | B.仅②④⑤ | C.仅①③ | D.①②③④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】关于晶体和晶胞的说法正确的是( )
| A.同一个物质可以是晶体也可以是非晶体 |
| B.进行X-射线干涉实验可以识别物质是否是晶体 |
| C.晶体的各向异性和对称性是矛盾的 |
| D.水晶是晶体,所以水是晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,这四种元素的最外层电子数之和为22。下列说法不正确 的是
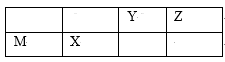

| A.Z与M可形成化合物MZ4 |
| B.简单离子半径:Y>Z |
| C.Z的非金属性比Y强,所以Z的氢化物沸点比Y高 |
| D.MY2与MZ4的化学键类型相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列变化中,既有共价键和离子键断裂,又有共价键和离子键形成的是( )
| A.2Na2O2+2CO2=2Na2CO3+O2 |
| B.2K+2H2O=2KOH+H2↑ |
| C.Cl2+H2O=HCl+HClO |
| D.Na2SO4+BaCl2=BaSO4↓+2NaCl |
您最近一年使用:0次
【推荐1】下列叙述正确的是
| A.直线形分子可能是非极性分子 |
| B.四原子分子不可能是正四面体形 |
| C.一种元素只能形成一种类型的晶体 |
| D.两种元素形成的化合物肯定含有极性键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法中错误的是
| A.根据对角线规则,B和Si的性质具有相似性 |
| B.元素电负性越大的原子,吸引电子的能力越强 |
| C.气体单质分子中,一定没有π键 |
| D.金属焰色反应原理是发生了电子跃迁 |
您最近一年使用:0次
【推荐1】下列模型分别表示 、
、 、
、 的结构,下列说法不正确的是
的结构,下列说法不正确的是

 、
、 、
、 的结构,下列说法不正确的是
的结构,下列说法不正确的是
A.1 mol  分子中有3 mol σ键和2 mol π键 分子中有3 mol σ键和2 mol π键 |
B.32 g  分子中含有1 mol σ键 分子中含有1 mol σ键 |
C. 是由非极性键构成的非极性分子 是由非极性键构成的非极性分子 |
| D.三种物质构成的晶体均为分子晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
①lmol CH 中含11NA个电子
中含11NA个电子
②1mol -OH中含10NA个电子
③lmol C10H22分子中共价键总数为31NA
④0.4mol以任意比例混合的乙炔和乙醛气体在氧气中充分燃烧时,消耗氧分子数为NA
⑤1 L 1 mol/L苯酚钠溶液中含有C6H5O-的个数为NA
⑥28g乙烯和环丙烷组成的混合气体中含有3NA个氢原子
①lmol CH
 中含11NA个电子
中含11NA个电子②1mol -OH中含10NA个电子
③lmol C10H22分子中共价键总数为31NA
④0.4mol以任意比例混合的乙炔和乙醛气体在氧气中充分燃烧时,消耗氧分子数为NA
⑤1 L 1 mol/L苯酚钠溶液中含有C6H5O-的个数为NA
⑥28g乙烯和环丙烷组成的混合气体中含有3NA个氢原子
| A.①④ | B.②⑥ | C.③④ | D.②⑤ |
您最近一年使用:0次

 和
和 是两种不同的元素
是两种不同的元素 和
和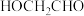 互为同系物
互为同系物 在元素周期表中处于同一主族
在元素周期表中处于同一主族 的数目小于0.2NA
的数目小于0.2NA

