研究金属腐蚀和防腐的原理很有现实意义。
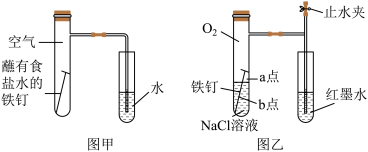
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如下表,根据数据判断腐蚀的速率随时间逐渐____ (填“加快”、“不变”、“减慢”),你认为影响因素为____ 。
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
根据以上实验探究,试判断_______ (填“a”或“b”)为负极,该点腐蚀更严重。
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式_______ 。

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱的上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。
| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,请完成表格空白:
| 实验操作 | 实验现象 | 实验结论 |
| 向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
| 然后再滴加2~3滴K3[Fe(CN)6]溶液 | b点周围出现蓝色沉淀 | b点电极反应为② |
根据以上实验探究,试判断
(4)金属阳极钝化是一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,试写出该阳极电极反应式
更新时间:2022-08-29 15:11:08
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
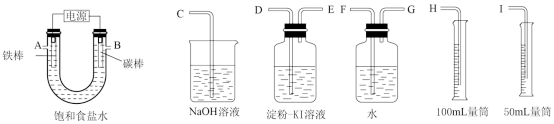
(1)试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接___________ ,B接___________ 。
(2)能说明氯气具有氧化性的实验现象是___________ 。
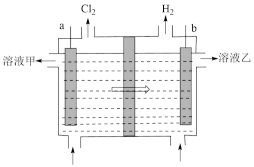
(3)工业上采用离子交换膜法电解饱和食盐水,如右图所示,该离子交换膜是___________ (填“阳离子”或“阴离子”)交换膜,溶液乙是___________

(1)试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接
(2)能说明氯气具有氧化性的实验现象是

(3)工业上采用离子交换膜法电解饱和食盐水,如右图所示,该离子交换膜是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】如图所示:甲、乙为相互串联的两电解池。试回答:

(1)乙池中Fe极电极反应式为___________ ,若在乙池中滴入少量酚酞试液,开始电解一段时间,铁极附近呈_________ 色。
(2)甲池若为用电解原理精炼铜(假设粗铜的组成是均匀的,且比其活泼和不活泼的成分均存在)的装置,则A电极名称为_____ 极,电极反应式为____________ ,电解质溶液可以是______ ;通电一段时间后,A极增重12.8g,则甲池溶液原溶质的浓度______ (填“增大”、“减小”、“不变”或“无法确定”),乙池C(石墨)极放出气体在标准状况下的体积为________ ,若此时,乙池剩余溶液为25℃,体积为400 mL,则溶液的pH=_______ 。

(1)乙池中Fe极电极反应式为
(2)甲池若为用电解原理精炼铜(假设粗铜的组成是均匀的,且比其活泼和不活泼的成分均存在)的装置,则A电极名称为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】CO2既是温室气体,也是重要的化工原料。以CO2为原料可合成多种物质。
(1)利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为:
①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol−1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol−1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol−1
反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H=____ 。
(2)在一定温度下,向2L固定容积的密闭容器中通入2 mol CO2和6 mol H2发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。

①前10 min内的平均反应速率υ(H2)=____ mol∕(L·min)。
②能说明该反应已达平衡状态的是____ 。
A.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
B.混合气体的平均摩尔质量保持不变
C.CH3OH的体积分数在混合气体中保持不变
D.混合气体的密度不随时间变化
③下列措施能使n(CH3OH) ∕n(CO2) 增大的是____ 。
A.升高温度 B.恒温恒容充入He(g)
C.使用高效催化剂 D.恒温恒容下,再充入1mol CO2、3mol H2
④该温度下的平衡常数K=____ (L∕mol)2。
(3)用100mL 0.25 mol∕L Na2CO3溶液吸收标准状况下336mL的CO2气体(溶液体积变化忽略不计),所得溶液中:c(HCO3−)+c(CO32−)+c(H2CO3)=____ mol∕L(填数字)。
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。

① b电极的名称是____ 。
② 请写出电解时生成乙烯的电极反应式____ 。
(1)利用CO2和CH4重整可制合成气(主要成分CO、H2),重整过程中部分反应的热化学方程式为:
①CH4(g) = C(s) + 2H2(g) △H = +75.0 kJ·mol−1
②CO2(g) + H2(g) = CO(g) + H2O(g) △H = +41.0 kJ·mol−1
③CO(g) + H2(g) = C(s) + H2O(g) △H = -131.0 kJ·mol−1
反应CO2(g) + CH4(g) = 2CO(g) + 2H2(g)的△H=
(2)在一定温度下,向2L固定容积的密闭容器中通入2 mol CO2和6 mol H2发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
CH3OH(g)+H2O(g) △H<0。测得CO2和CH3OH(g)浓度随时间变化如下图所示。
①前10 min内的平均反应速率υ(H2)=
②能说明该反应已达平衡状态的是
A.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
B.混合气体的平均摩尔质量保持不变
C.CH3OH的体积分数在混合气体中保持不变
D.混合气体的密度不随时间变化
③下列措施能使n(CH3OH) ∕n(CO2) 增大的是
A.升高温度 B.恒温恒容充入He(g)
C.使用高效催化剂 D.恒温恒容下,再充入1mol CO2、3mol H2
④该温度下的平衡常数K=
(3)用100mL 0.25 mol∕L Na2CO3溶液吸收标准状况下336mL的CO2气体(溶液体积变化忽略不计),所得溶液中:c(HCO3−)+c(CO32−)+c(H2CO3)=
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。

① b电极的名称是
② 请写出电解时生成乙烯的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.中和反应反应热的测定。
测定50mL 0.50mol/L盐酸和50mL 0.55mol/L NaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是_______ 。
(2)若两种溶液的密度均为 ,反应后生成溶液的比热容
,反应后生成溶液的比热容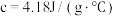 ,反应过程中测得体系温度升高3℃,则该反应放出
,反应过程中测得体系温度升高3℃,则该反应放出_______ kJ热量。
Ⅱ.温度对化学平衡的影响。
(3)在 生成
生成 的反应中,存在如下平衡:
的反应中,存在如下平衡:
 。取两个封装有
。取两个封装有 和
和 混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在
混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在_______ (填“热水”或“冷水”)中的颜色更深,产生这一现象的原因是_______ 。
ⅢI.简易原电池反应。
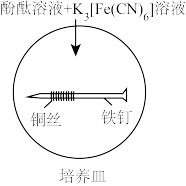
(4)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液和 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生_______ 色的_______ (填化学式)沉淀;铜丝周围的现象是_______ ,发生的电极反应式为_______ 。
Ⅰ.中和反应反应热的测定。
测定50mL 0.50mol/L盐酸和50mL 0.55mol/L NaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是
(2)若两种溶液的密度均为
 ,反应后生成溶液的比热容
,反应后生成溶液的比热容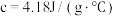 ,反应过程中测得体系温度升高3℃,则该反应放出
,反应过程中测得体系温度升高3℃,则该反应放出Ⅱ.温度对化学平衡的影响。
(3)在
 生成
生成 的反应中,存在如下平衡:
的反应中,存在如下平衡:
 。取两个封装有
。取两个封装有 和
和 混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在
混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在ⅢI.简易原电池反应。
(4)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
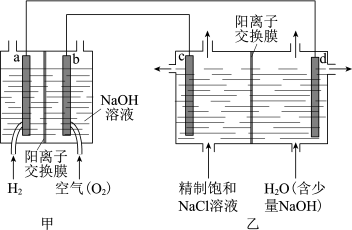

①乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_______ ;反应一段时间后,d极产生 气体时,乙装置中转移电子
气体时,乙装置中转移电子_______  。
。
②下列说法正确的是_______ (填字母序号)。
A.甲装置可实现化学能向电能的转化
B.甲装置中 透过阳离子交换膜向a极移动
透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀.炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈.请写出铁锅生锈过程的正极反应式:_______ 。
②图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的_______ 极。
(3)蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是: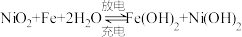 。
。
①若此蓄电池放电时,该电池某一电极发生还原反应的物质是_______ (填序号)。
A.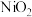 B.
B. C.
C. D.
D.
②该电池放电时,正极附近溶液的pH_______ (填增大、减小、不变)。
③充电时该电池阴极的电极反应式_______ 。
(1)我国利用氯碱厂生产的
 作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。

①乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为 气体时,乙装置中转移电子
气体时,乙装置中转移电子 。
。②下列说法正确的是
A.甲装置可实现化学能向电能的转化
B.甲装置中
 透过阳离子交换膜向a极移动
透过阳离子交换膜向a极移动C.乙装置中c极一侧流出的是浓盐水
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀.炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈.请写出铁锅生锈过程的正极反应式:
②图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的
(3)蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是:
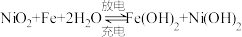 。
。①若此蓄电池放电时,该电池某一电极发生还原反应的物质是
A.
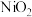 B.
B. C.
C. D.
D.
②该电池放电时,正极附近溶液的pH
③充电时该电池阴极的电极反应式
您最近一年使用:0次
【推荐3】化学实验有助于理解化学知识,提升科学素养。
I.某探究小组用以下右图装置做如下实验。
(1)实验1:同时加入试剂,反应开始阶段可观察到U形管中液面_____ (填编号,下同),反应结束静置一段时间,最终U形管中液面_______ 。
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后观察到U形管中液面左低右高, b管溶液中出现红褐色浑浊物,请解释出现上述现象的原因:________________________________________________ 。
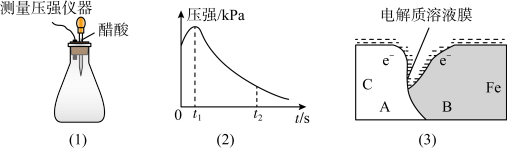
II.某研究小组为探究弱酸性条件下铁的电化学腐蚀类型,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图(1)所示)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(3)请填满表中空格,以完成实验设计:
(4)实验①测得容器中的压强随时间的变化如图(2)所示。该小组得出0~t1时压强增大的主要原因是:___________________________________ 。t2时,容器中压强明显变小的原因是______________ 。请在图(3)中用箭头标出发生该腐蚀时A和B之间的电子移动方向______________ 。
I.某探究小组用以下右图装置做如下实验。
| 实验编号 | a中试剂 | b中试剂 | 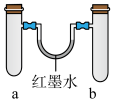 |
| 1 | 0.1克Na、3 mL水 | 0.1克Na、3 mL乙醇 | |
| 2 | 3 mL水 | 3 mL饱和FeSO4溶液 |
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后观察到U形管中液面左低右高, b管溶液中出现红褐色浑浊物,请解释出现上述现象的原因:
II.某研究小组为探究弱酸性条件下铁的电化学腐蚀类型,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图(1)所示)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(3)请填满表中空格,以完成实验设计:
| 编号 | 实验目的 | 炭粉/g | 铁粉/g | 醋酸浓度/mol/L |
| ① | 作参照实验 | 0.5 | 2.0 | 1.0 |
| ② | 探究醋酸浓度对实验的影响 | 0.5 | 0.1 | |
| ③ | 0.2 | 2.0 | 1.0 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】镍的全球消费量仅次于铜、铝、铅、锌,居有色金属第五位,常用于各种高光泽装饰漆和塑料生产,也用作催化剂,制取原理: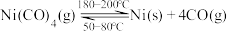 ,实验室用如图所示装置制取Ni(CO)4。
,实验室用如图所示装置制取Ni(CO)4。

已知:①
②Ni(CO)4熔点 25℃,沸点43℃,60℃以上与空气混合易爆炸
25℃,沸点43℃,60℃以上与空气混合易爆炸
③Fe(CO)5熔点 20℃,沸点103℃。回答下列问题:
20℃,沸点103℃。回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置C用于合成Ni(CO)4(夹持装置略),最适宜选用的装置为___________ (填标号)。
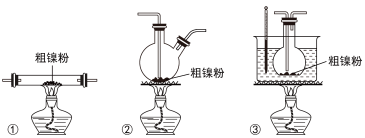
(3)在加热C装置之前,必须先观察___________ 装置(填字母)中___________ (填实验现象),目的是为了防止___________ 。
(4)利用“封管实验”原理可获得高纯镍。如图所示的石英玻璃封管中充有CO气体,则高纯镍粉在封管的___________ 温度区域端生成(填“323K”或“473K”)。

(5)实验中加入11.50gHCOOH,C装质量减轻2.95g(设杂志不参加反应),E装置中盛有PdCl2溶液100mL,则PdCl2溶液的物质的量浓度至少为___________  。
。
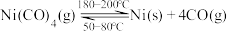 ,实验室用如图所示装置制取Ni(CO)4。
,实验室用如图所示装置制取Ni(CO)4。
已知:①

②Ni(CO)4熔点
 25℃,沸点43℃,60℃以上与空气混合易爆炸
25℃,沸点43℃,60℃以上与空气混合易爆炸③Fe(CO)5熔点
 20℃,沸点103℃。回答下列问题:
20℃,沸点103℃。回答下列问题:(1)装置A中发生反应的化学方程式为
(2)装置C用于合成Ni(CO)4(夹持装置略),最适宜选用的装置为

(3)在加热C装置之前,必须先观察
(4)利用“封管实验”原理可获得高纯镍。如图所示的石英玻璃封管中充有CO气体,则高纯镍粉在封管的

(5)实验中加入11.50gHCOOH,C装质量减轻2.95g(设杂志不参加反应),E装置中盛有PdCl2溶液100mL,则PdCl2溶液的物质的量浓度至少为
 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】无色而有刺激性气味的甲酸,是最简单的羧酸液体,熔点8.6℃,沸点100.8℃。化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其反应方程式为:HCOOH CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。
CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。
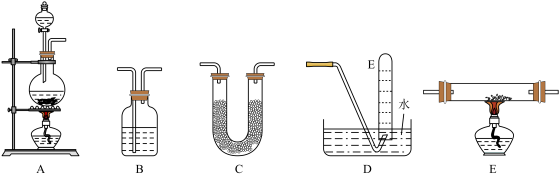
(1)请从图中选用所需的仪器(仪器可重复使用)组成一套验证甲酸(HCOOH)和浓硫酸加热生成产物的实验装置。现提供以下药品:甲酸、浓硫酸、无水硫酸铜、氧化铜粉末、澄清石灰水。将所用仪器的序号按连接顺序由上至下依次填入下表(可以不填满),并写出该仪器中应加试剂的名称或化学式(划横线部分不需要填写)。___
证明有一氧化碳生成的现象是___ 。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2⋅4H2O]晶体。查阅资料可知四水甲酸铜晶体为浅蓝色晶体,可溶于水,难溶于醇。
相关的化学方程式是:2CuSO4+4NaHCO3=Cu(OH)2⋅CuCO3↓+3CO2↑+2Na2SO4+H2O;Cu(OH)2⋅CuCO3+4HCOOH+5H2O=2Cu(HCOO)2⋅4H2O+CO2↑
实验步骤如下:
Ⅰ.碱式碳酸铜的制备:
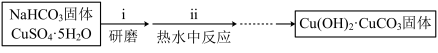
①步骤ⅰ是将一定量CuSO4⋅5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是___ 。
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到___ (填写实验现象),说明温度过高。
Ⅱ.甲酸铜的制备:将Cu(OH)2⋅CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的 时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
③制取甲酸铜时需要趁热过滤的原因是___ 。
④用无水乙醇洗涤晶体的目的是___
 CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。
CO↑+H2O,制备时先加热浓硫酸至80℃-90℃,控制温度,再逐滴滴入甲酸。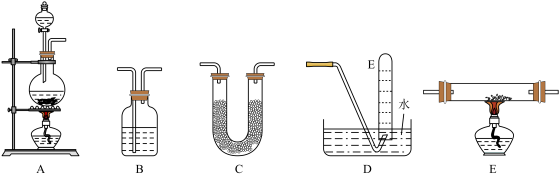
(1)请从图中选用所需的仪器(仪器可重复使用)组成一套验证甲酸(HCOOH)和浓硫酸加热生成产物的实验装置。现提供以下药品:甲酸、浓硫酸、无水硫酸铜、氧化铜粉末、澄清石灰水。将所用仪器的序号按连接顺序由上至下依次填入下表(可以不填满),并写出该仪器中应加试剂的名称或化学式(划横线部分不需要填写)。
| 选用的仪器 | 加入的试剂 |
| A | 甲酸、浓硫酸 |
| D | -- |
证明有一氧化碳生成的现象是
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸制得四水甲酸铜[Cu(HCOO)2⋅4H2O]晶体。查阅资料可知四水甲酸铜晶体为浅蓝色晶体,可溶于水,难溶于醇。
相关的化学方程式是:2CuSO4+4NaHCO3=Cu(OH)2⋅CuCO3↓+3CO2↑+2Na2SO4+H2O;Cu(OH)2⋅CuCO3+4HCOOH+5H2O=2Cu(HCOO)2⋅4H2O+CO2↑
实验步骤如下:
Ⅰ.碱式碳酸铜的制备:

①步骤ⅰ是将一定量CuSO4⋅5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是
②步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃-80℃,如果看到
Ⅱ.甲酸铜的制备:将Cu(OH)2⋅CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的
 时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。
时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2-3次,晾干,得到产品。③制取甲酸铜时需要趁热过滤的原因是
④用无水乙醇洗涤晶体的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酰硫酸(NOSO4H)是一种浅黄色或蓝紫色液体,遇水分解,溶于浓硫酸不分解,主要用于燃料、医药领域的重氮化反应中取代亚硝酸钠。亚硝酰硫酸能有效降低硫酸使用量,增加反应的流动性,不产生无机盐,从而可以降低成本,提高产品质量,使燃料成品色泽鲜艳、固色能力强,并减少污水。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。
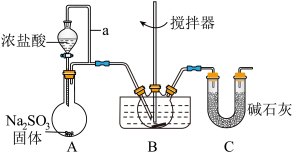
(1)导管a的作用是_________ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,故可将三颈烧瓶置于_________ 中。
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是_________ 。
③该实验装置存在导致NOSO4H产量降低的缺陷,请提出改进方案_________ 。
④利用装置A制备SO2,下列试剂最适合的是________ 。
A.Na2SO3固体和20%硝酸
B.Na2SO3固体和20%硫酸
C.Na2SO3固体和70%硫酸
D.Na2SO3固体和98%硫酸
⑤已知亚硝酸不稳定,易分解,发生反应2HNO2=NO2↑+NO↑+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式____________ 。
(3)测定亚硝酰硫酸NOSO4H的纯度。准确称取1.380g产品放入250mL的碘量瓶中,加入60.00mL 0.1000mol·L‾1 KMnO4标准溶液和10mL 25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500 mol·L‾1的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。亚硝酰硫酸的纯度为_______________ 。

(1)导管a的作用是
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,故可将三颈烧瓶置于
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
③该实验装置存在导致NOSO4H产量降低的缺陷,请提出改进方案
④利用装置A制备SO2,下列试剂最适合的是
A.Na2SO3固体和20%硝酸
B.Na2SO3固体和20%硫酸
C.Na2SO3固体和70%硫酸
D.Na2SO3固体和98%硫酸
⑤已知亚硝酸不稳定,易分解,发生反应2HNO2=NO2↑+NO↑+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式
(3)测定亚硝酰硫酸NOSO4H的纯度。准确称取1.380g产品放入250mL的碘量瓶中,加入60.00mL 0.1000mol·L‾1 KMnO4标准溶液和10mL 25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500 mol·L‾1的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。亚硝酰硫酸的纯度为
您最近一年使用:0次



