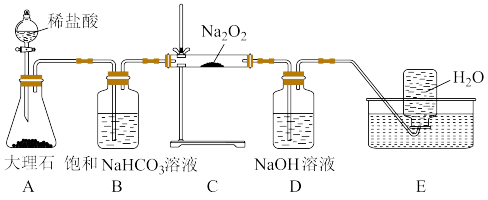
镍的全球消费量仅次于铜、铝、铅、锌,居有色金属第五位,常用于各种高光泽装饰漆和塑料生产,也用作催化剂,制取原理: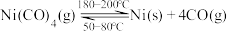 ,实验室用如图所示装置制取Ni(CO)4。
,实验室用如图所示装置制取Ni(CO)4。

已知:①
②Ni(CO)4熔点 25℃,沸点43℃,60℃以上与空气混合易爆炸
25℃,沸点43℃,60℃以上与空气混合易爆炸
③Fe(CO)5熔点 20℃,沸点103℃。回答下列问题:
20℃,沸点103℃。回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置C用于合成Ni(CO)4(夹持装置略),最适宜选用的装置为___________ (填标号)。
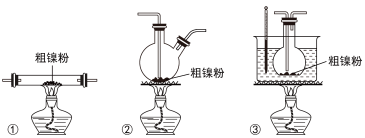
(3)在加热C装置之前,必须先观察___________ 装置(填字母)中___________ (填实验现象),目的是为了防止___________ 。
(4)利用“封管实验”原理可获得高纯镍。如图所示的石英玻璃封管中充有CO气体,则高纯镍粉在封管的___________ 温度区域端生成(填“323K”或“473K”)。

(5)实验中加入11.50gHCOOH,C装质量减轻2.95g(设杂志不参加反应),E装置中盛有PdCl2溶液100mL,则PdCl2溶液的物质的量浓度至少为___________  。
。
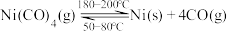 ,实验室用如图所示装置制取Ni(CO)4。
,实验室用如图所示装置制取Ni(CO)4。
已知:①

②Ni(CO)4熔点
 25℃,沸点43℃,60℃以上与空气混合易爆炸
25℃,沸点43℃,60℃以上与空气混合易爆炸③Fe(CO)5熔点
 20℃,沸点103℃。回答下列问题:
20℃,沸点103℃。回答下列问题:(1)装置A中发生反应的化学方程式为
(2)装置C用于合成Ni(CO)4(夹持装置略),最适宜选用的装置为

(3)在加热C装置之前,必须先观察
(4)利用“封管实验”原理可获得高纯镍。如图所示的石英玻璃封管中充有CO气体,则高纯镍粉在封管的

(5)实验中加入11.50gHCOOH,C装质量减轻2.95g(设杂志不参加反应),E装置中盛有PdCl2溶液100mL,则PdCl2溶液的物质的量浓度至少为
 。
。
更新时间:2022-02-15 19:53:16
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】铈(Ce)是人类发现的第二种稀土元素,常用作还原剂、催化剂、特殊光学材料添加剂等。铈的常见价态是+3和+4,请回答下列问题:
(1)大气污染物NO可被含Ce4+的溶液吸收,生成 、
、 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是_______ 。
(2)用电解的方法可将上述吸收液中的 转化为稳定的无毒气体,同时再生Ce4+,电解装置如图所示。
转化为稳定的无毒气体,同时再生Ce4+,电解装置如图所示。

①无毒气体从电解槽的c口逸出,则A极为电源的_______ 极(填“正”或“负”)。
② 转化为稳定的无毒气体的电极反应式是
转化为稳定的无毒气体的电极反应式是_______ 。
(3)铈元素在自然界中主要以氟碳铈(CeFCO3)矿的形式存在。工业上利用氟碳铈矿提取CeO2的一种工艺流程如下:

①“焙烧”过程中发生的主要反应的氧化剂和还原剂的物质的量之比为_______ 。
②已知硼酸H3BO3与足量NaOH反应的产物是Na[B(OH)4],则硼酸在溶液的电离方程式为_______ 。
③已知“转化”过程没有电子转移,则“转化”过程的化学方程式为_______ 。
④常温下,“沉铈”过程中Ce3+恰好沉淀完全[c(Ce3+)为1.0×10-5mol·L-1],此时测得溶液的pH=5,则溶液中c( )=
)=_______ mol·L-1。(已知常温下Ka1(H2CO3)=5.0×10-7,Ka2(H2CO3)=5.0×10-11,Ksp[Ce2(CO3)3]=1.0×10-28)
(1)大气污染物NO可被含Ce4+的溶液吸收,生成
 、
、 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是(2)用电解的方法可将上述吸收液中的
 转化为稳定的无毒气体,同时再生Ce4+,电解装置如图所示。
转化为稳定的无毒气体,同时再生Ce4+,电解装置如图所示。
①无毒气体从电解槽的c口逸出,则A极为电源的
②
 转化为稳定的无毒气体的电极反应式是
转化为稳定的无毒气体的电极反应式是(3)铈元素在自然界中主要以氟碳铈(CeFCO3)矿的形式存在。工业上利用氟碳铈矿提取CeO2的一种工艺流程如下:

①“焙烧”过程中发生的主要反应的氧化剂和还原剂的物质的量之比为
②已知硼酸H3BO3与足量NaOH反应的产物是Na[B(OH)4],则硼酸在溶液的电离方程式为
③已知“转化”过程没有电子转移,则“转化”过程的化学方程式为
④常温下,“沉铈”过程中Ce3+恰好沉淀完全[c(Ce3+)为1.0×10-5mol·L-1],此时测得溶液的pH=5,则溶液中c(
 )=
)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸( )是一种常用的除锈剂、还原剂和滴定剂。某小组以电石(主要成分是
)是一种常用的除锈剂、还原剂和滴定剂。某小组以电石(主要成分是 ,含少量CaS、
,含少量CaS、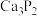 杂质)为原料制备草酸并探究草酸的性质、测定粗草酸产品的纯度。
杂质)为原料制备草酸并探究草酸的性质、测定粗草酸产品的纯度。 、
、 ,
, 。
。
请回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置A中,实际操作中常用饱和食盐水代替水,其原因是___________ 。
(3)装置B的作用是吸收装置A中产生的杂质 、
、 ,经测定,装置B中吸收
,经测定,装置B中吸收 过程生成了沉淀
过程生成了沉淀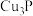 和两种最高价含氧酸,写出
和两种最高价含氧酸,写出 发生反应的离子方程式:
发生反应的离子方程式:___________ 。
(4)实验测得装置C中产生NO、 的物质的量之比为1∶1,则装置C中反应的化学方程式为
的物质的量之比为1∶1,则装置C中反应的化学方程式为___________ (忽略 ,
, 的转化)。
的转化)。
(5)实验结束后,采用结晶法从装置C中分离出草酸,将草酸加入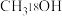 和浓硫酸中,加热后产生有香味的油状物质,有香味的物质是
和浓硫酸中,加热后产生有香味的油状物质,有香味的物质是___________ (填结构简式)。
(6)称取w g草酸粗产品配制成250 mL溶液,准确量取25.00mL所配溶液于锥形瓶中,加入足量稀硫酸,用c mol⋅L
 标准溶液滴定至终点,消耗滴定液V mL。该粗产品的纯度为
标准溶液滴定至终点,消耗滴定液V mL。该粗产品的纯度为___________ %(假设杂质不参加反应,用含w、c、V的代数式表示)。
 )是一种常用的除锈剂、还原剂和滴定剂。某小组以电石(主要成分是
)是一种常用的除锈剂、还原剂和滴定剂。某小组以电石(主要成分是 ,含少量CaS、
,含少量CaS、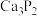 杂质)为原料制备草酸并探究草酸的性质、测定粗草酸产品的纯度。
杂质)为原料制备草酸并探究草酸的性质、测定粗草酸产品的纯度。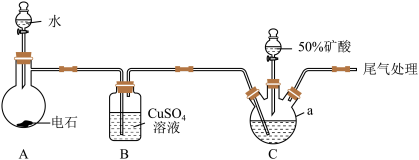
 、
、 ,
, 。
。请回答下列问题:
(1)仪器a的名称是
(2)装置A中,实际操作中常用饱和食盐水代替水,其原因是
(3)装置B的作用是吸收装置A中产生的杂质
 、
、 ,经测定,装置B中吸收
,经测定,装置B中吸收 过程生成了沉淀
过程生成了沉淀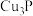 和两种最高价含氧酸,写出
和两种最高价含氧酸,写出 发生反应的离子方程式:
发生反应的离子方程式:(4)实验测得装置C中产生NO、
 的物质的量之比为1∶1,则装置C中反应的化学方程式为
的物质的量之比为1∶1,则装置C中反应的化学方程式为 ,
, 的转化)。
的转化)。(5)实验结束后,采用结晶法从装置C中分离出草酸,将草酸加入
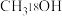 和浓硫酸中,加热后产生有香味的油状物质,有香味的物质是
和浓硫酸中,加热后产生有香味的油状物质,有香味的物质是(6)称取w g草酸粗产品配制成250 mL溶液,准确量取25.00mL所配溶液于锥形瓶中,加入足量稀硫酸,用c mol⋅L

 标准溶液滴定至终点,消耗滴定液V mL。该粗产品的纯度为
标准溶液滴定至终点,消耗滴定液V mL。该粗产品的纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】电镀废水中常含有剧毒的NaCN,可用两段氧化法处理:
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素Na、N、O中,简单离子半径最小的是___ (填离子符号),氢原子最外层电子的轨道表示式是___ 。
(2)NaCN中所含有的化学键类型是___ ,N2的电子式为___ 。
(3)已知NaOCN中N元素为-3价,配平第二段过程的化学方程式并标出电子转移的方向和数目___ 。
(4)综合两段反应,处理含有0.01molNaCN的废水,至少需NacClO___ mol。
(5)请用一个方程式证明氮元素的非金属性大于碳元素___ 。
①第一段:NaCN+NaClO→NaOCN+NaCl
②第二段:NaOCN+NaClO→Na2CO3+CO2↑+NaCl+N2↑(未配平)
完成下列填空:
(1)上述反应涉及的元素Na、N、O中,简单离子半径最小的是
(2)NaCN中所含有的化学键类型是
(3)已知NaOCN中N元素为-3价,配平第二段过程的化学方程式并标出电子转移的方向和数目
(4)综合两段反应,处理含有0.01molNaCN的废水,至少需NacClO
(5)请用一个方程式证明氮元素的非金属性大于碳元素
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组在实验室探究氨的有关性质,设计了下图所示实验,A处是气体发生装置,A中所用的实验药品从下列物质中选取。
①碳酸钠 ②碳酸氢钠 ③碳酸氢铵 ④氯化铵 ⑤熟石灰 ⑥氢氧化钠

按上图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯,部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)若A中制取气体时只用了一种药品,则该药品是____ (填物质序号)
(2)B装置的作用为____
(3)D中铜片发生反应的离子方程式为____ ,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的____ (填下列各项序号)
A.Na2CO3 B.AgNO3 C.H2SO4 D.FeSO4
(4)图E中持续通入氧气的作用为____ 。
(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进,谈谈你的意见:____ 。
①碳酸钠 ②碳酸氢钠 ③碳酸氢铵 ④氯化铵 ⑤熟石灰 ⑥氢氧化钠

按上图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯,部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)若A中制取气体时只用了一种药品,则该药品是
(2)B装置的作用为
(3)D中铜片发生反应的离子方程式为
A.Na2CO3 B.AgNO3 C.H2SO4 D.FeSO4
(4)图E中持续通入氧气的作用为
(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进,谈谈你的意见:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室利用如图装置制取氧气,回答下列问题:

(1)仪器①的名称是_______ 。
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式为_______ 。
(3)若用B装置干燥氧气,则B中盛放的试剂为_______ (填试剂名称),若将B装置中装满水收集氧气,则气体应从导管_______ (填“a”或“b”)端通入。
(4)若直接用30%的过氧化氢溶液制取氧气,反应速率太快。为获得平稳的氧气流,图中C~F四个发生装置能达到最佳效果的是_______ (填字母)。

(1)仪器①的名称是
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气的化学方程式为
(3)若用B装置干燥氧气,则B中盛放的试剂为
(4)若直接用30%的过氧化氢溶液制取氧气,反应速率太快。为获得平稳的氧气流,图中C~F四个发生装置能达到最佳效果的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】三甲基镓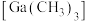 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金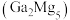 、碘甲烷
、碘甲烷 等为原料制备
等为原料制备 ,实验主要装置和步骤如下:
,实验主要装置和步骤如下:

向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚(用 表示),加热(55℃)并搅拌
表示),加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加三正辛胺(用
中逐滴滴加三正辛胺(用 表示),室温下搅拌
表示),室温下搅拌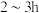 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得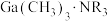 。将
。将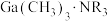 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。
已知:①常温下, 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。
②相关物质的沸点信息如下表:
回答下列问题:
(1)仪器a的名称是________ ;制备 时,需在真空中加热的原因是
时,需在真空中加热的原因是_________ 。
(2)三颈烧瓶中除生成 外,还有
外,还有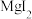 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为___________ 。
(3)用真空泉不断抽出 蒸气,有利于
蒸气,有利于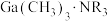 生成的理由是
生成的理由是___________ (用平衡移动原理解释);与直接分解 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是___________ 。
(4)测定 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入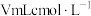 盐酸,至不再产生气泡
盐酸,至不再产生气泡 ,加入2滴甲基橙,用
,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为___________ (用含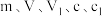 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果___________ (填“偏高”“偏低”或“无影响”)。
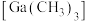 是一种重要的半导体材料前驱体。实验室以镓镁合金
是一种重要的半导体材料前驱体。实验室以镓镁合金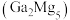 、碘甲烷
、碘甲烷 等为原料制备
等为原料制备 ,实验主要装置和步骤如下:
,实验主要装置和步骤如下:
向三颈烧瓶中加入镓镁合金、碘甲烷和乙醚(用
 表示),加热(55℃)并搅拌
表示),加热(55℃)并搅拌 。蒸出低沸点有机物后减压蒸馏,收集
。蒸出低沸点有机物后减压蒸馏,收集 。向
。向 中逐滴滴加三正辛胺(用
中逐滴滴加三正辛胺(用 表示),室温下搅拌
表示),室温下搅拌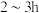 ,并用真空泵不断抽出
,并用真空泵不断抽出 蒸气,制得
蒸气,制得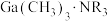 。将
。将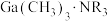 置于真空中加热,蒸出
置于真空中加热,蒸出 。
。已知:①常温下,
 为无色透明的液体,易水解,在空气中易自燃。
为无色透明的液体,易水解,在空气中易自燃。②相关物质的沸点信息如下表:
| 物质 |  |  |  |  |
| 沸点/℃ | 55.8 | 40.3 | 34.5 | 365.8 |
(1)仪器a的名称是
 时,需在真空中加热的原因是
时,需在真空中加热的原因是(2)三颈烧瓶中除生成
 外,还有
外,还有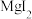 和
和 生成,该反应的化学方程式为
生成,该反应的化学方程式为(3)用真空泉不断抽出
 蒸气,有利于
蒸气,有利于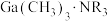 生成的理由是
生成的理由是 制备
制备 相比,采用“
相比,采用“ 配体交换”工艺制备的产品纯度更高的原因是
配体交换”工艺制备的产品纯度更高的原因是(4)测定
 产品的纯度。取
产品的纯度。取 样品于锥形瓶中,加入
样品于锥形瓶中,加入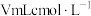 盐酸,至不再产生气泡
盐酸,至不再产生气泡 ,加入2滴甲基橙,用
,加入2滴甲基橙,用 溶液滴定剩余盐酸,消耗
溶液滴定剩余盐酸,消耗 溶液的体积为
溶液的体积为 ,则
,则 的质量分数为
的质量分数为 的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
的代数式表示);若滴定达终点时发现滴定管尖嘴内有气泡生成,则测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为常用玻璃仪器组成的六种实验装置,均可根据不同的实验需要在其中加入不同的液体或固体试剂。请用适宜装置的序号完成下列填空:

(1)能用于干燥CO2气流的装置是_________ 。
(2)用于除去Cl2,中HCl杂质的最佳装置是_________ 。
(3)用于尾气吸收并能防止液体倒吸到反应装置中的是_________ 。
(4)接在气体制备的连续实验装置中间,用于控制气流平稳的装置是_________ 。
(5)利用装置A收集CO2气体,应从____ 口进气。A中装满水,用排水法测量生成H2的体积,应从____ 口进气。

(1)能用于干燥CO2气流的装置是
(2)用于除去Cl2,中HCl杂质的最佳装置是
(3)用于尾气吸收并能防止液体倒吸到反应装置中的是
(4)接在气体制备的连续实验装置中间,用于控制气流平稳的装置是
(5)利用装置A收集CO2气体,应从
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯酸锶 为白色结晶粉末,可溶于水,微溶于酒精。它主要用于制造红色焰火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
为白色结晶粉末,可溶于水,微溶于酒精。它主要用于制造红色焰火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:

(1)仪器a的名称是___________ 。
(2)A中发生反应的离子方程式为___________ ,该反应中 作
作___________ 剂。
(3)装置B中所装的试剂为___________ ,其作用是___________ 。
(4)装置C中搅拌的目的是___________ ;装置C制备氯酸锶的反应为 ,若反应消耗
,若反应消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为___________ mol。
(5)装置D的作用是___________ 。
 为白色结晶粉末,可溶于水,微溶于酒精。它主要用于制造红色焰火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
为白色结晶粉末,可溶于水,微溶于酒精。它主要用于制造红色焰火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
(1)仪器a的名称是
(2)A中发生反应的离子方程式为
 作
作(3)装置B中所装的试剂为
(4)装置C中搅拌的目的是
 ,若反应消耗
,若反应消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为(5)装置D的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氨基甲酸铵(NH2COONH4)是一种易分解、易水解的白色固体、难溶于CCl4。实验室可将干燥二氧化碳和氨气通入CCl4中进行制备,反应原理为2NH3(g)+CO2(g)=NH2COONH4(s) △H<0,回答下列问题:
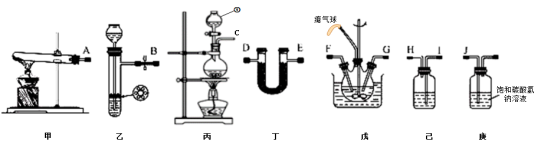
(1)仪器①的名称为_____ ,装置己中盛放的试剂为_____ 。
(2)简述检验装置乙气密性的操作_____ 。
(3)氨气的发生装置可以选择上图中的_____ ,制取氨气的化学方程式为_____ 。
(4)预制备产品,选择上图中必要的装置,其连接顺序为:发生装置→_____ →FG←_____ ←KJ←_____ (按气流方向,用大写字母表示)。
(5)为了提高氨基甲酸铵的产率.对三颈瓶采取的控温方法是_____ ,反应结束后,从反应后的混合物中分离出产品的实验操作是_____ ,戊中气球的作用是_____ 。
(6)氨基甲酸铵容易变质生成碳酸氢铵,现取长期存放的样品19.550g,用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,通过系列操作得纯净碳酸钙25.000g,则该样品的纯度为_____ %。(计算结果保留三位有效数字;有关物质的相对式量:氨基甲酸铵78、碳酸氢铵79、碳酸钙100) 。

(1)仪器①的名称为
(2)简述检验装置乙气密性的操作
(3)氨气的发生装置可以选择上图中的
(4)预制备产品,选择上图中必要的装置,其连接顺序为:发生装置→
(5)为了提高氨基甲酸铵的产率.对三颈瓶采取的控温方法是
(6)氨基甲酸铵容易变质生成碳酸氢铵,现取长期存放的样品19.550g,用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,通过系列操作得纯净碳酸钙25.000g,则该样品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某校化学小组学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体。(图中夹持及尾气处理装置均已略去)
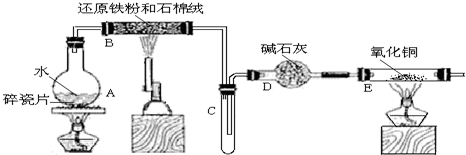
(1)装置B中发生反应的化学方程式是______ 。
(2)装置E中的现象是______ 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:______ 。
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如图所示:
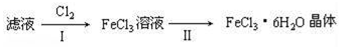
①步骤I中通入Cl2的作用是________ 。
②简述检验滤液中Fe3+的操作方法_______ 。
③步骤Ⅱ从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:_______ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:
(4)该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如图所示:
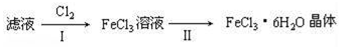
①步骤I中通入Cl2的作用是
②简述检验滤液中Fe3+的操作方法
③步骤Ⅱ从FeCl3稀溶液中得到FeCl3•6H2O晶体的主要操作包括:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】金属 对
对 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状
有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状 转化成多孔型雷尼
转化成多孔型雷尼 后,其倠化活性显著提高。
后,其倠化活性显著提高。
已知:①雷尼 暴露在空气中可自然,在制备和使用时,需用水或有机溶剂保持表面“湿润”。
暴露在空气中可自然,在制备和使用时,需用水或有机溶剂保持表面“湿润”。
②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼 并探究其催化氢化性能的实验如下:
并探究其催化氢化性能的实验如下:
步骤1:雷尼 的制备
的制备

步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置用于储存和监测反应过程。

回答下列问题:
(1)仪器M的名称是___________ ;
(2)操作(a)中,反应的离子方程式是___________ ;
(3)操作(d)中,判断雷尼 被水洗净的方法是
被水洗净的方法是___________ ;
(4)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是___________;
(5)反应前应向装置II中通入 一段时间,目的是
一段时间,目的是___________ ;
(6)向集气管中充入 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置II供气,此时孔路位置需调节为
时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置II供气,此时孔路位置需调节为___________ ;

(7)判断氢化反应完全的现象是___________ 。
 对
对 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状
有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状 转化成多孔型雷尼
转化成多孔型雷尼 后,其倠化活性显著提高。
后,其倠化活性显著提高。已知:①雷尼
 暴露在空气中可自然,在制备和使用时,需用水或有机溶剂保持表面“湿润”。
暴露在空气中可自然,在制备和使用时,需用水或有机溶剂保持表面“湿润”。②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼
 并探究其催化氢化性能的实验如下:
并探究其催化氢化性能的实验如下:步骤1:雷尼
 的制备
的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置用于储存和监测反应过程。

回答下列问题:
(1)仪器M的名称是
(2)操作(a)中,反应的离子方程式是
(3)操作(d)中,判断雷尼
 被水洗净的方法是
被水洗净的方法是(4)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是___________;
| A.丙酮 | B.四氯化碳 | C.乙醇 | D.正己烷 |
 一段时间,目的是
一段时间,目的是(6)向集气管中充入
 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置II供气,此时孔路位置需调节为
时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置II供气,此时孔路位置需调节为
(7)判断氢化反应完全的现象是
您最近一年使用:0次