请按要求回答下列问题。
(1)写出下列物质在水溶液中的电离方程式
①HClO:_______ ;
②H2SO3:_______ ;
③NaHCO3:_______ ;
④Cu(OH)2:_______ 。
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(3)在25 ℃、101 kPa时,H2在O2中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为_______ 。
(4)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+260 kJ·mol-1①
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②
则CH4与O2反应生成CO和H2的热化学方程式为_______ 。
(1)写出下列物质在水溶液中的电离方程式
①HClO:
②H2SO3:
③NaHCO3:
④Cu(OH)2:
(2)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为
(3)在25 ℃、101 kPa时,H2在O2中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为
(4)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+260 kJ·mol-1①
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1②
则CH4与O2反应生成CO和H2的热化学方程式为
更新时间:2022-09-15 18:37:26
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)家用液化气的主要成分之一是丁烷,当58g丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为2900kJ,试写出表示丁烷燃烧热的热化学方程式:__________________ ;
(2)稀盐酸和NaOH稀溶液反应生成1mol水放热57.3KJ, 该反应的热化学方程式为_______________________________________________ 。
(2)稀盐酸和NaOH稀溶液反应生成1mol水放热57.3KJ, 该反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Ⅰ.已知下列热化学方程式:①H2(g)+ O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,
②H2(g)+ O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
③C(s)+ O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为___________ ;(填序号)
(2)燃烧1gH2生成气态水,放出的热量为___________ 。
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量___________ (填“大于”“等于”或“小于”)57.3kJ,原因是___________ 。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热∆H ___________ 0。
 O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,②H2(g)+
 O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,③C(s)+
 O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为
(2)燃烧1gH2生成气态水,放出的热量为
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】 在高温下分解产生的
在高温下分解产生的 可作为硫酸工业中
可作为硫酸工业中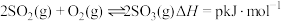 的催化剂,其催化原理如图所示。
的催化剂,其催化原理如图所示。
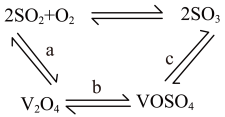
过程a和过程b的热化学方程式分别为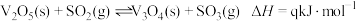 、
、 。请写出过程c的热化学方程式:
。请写出过程c的热化学方程式:___________ 。
 在高温下分解产生的
在高温下分解产生的 可作为硫酸工业中
可作为硫酸工业中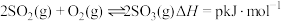 的催化剂,其催化原理如图所示。
的催化剂,其催化原理如图所示。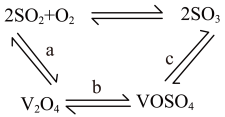
过程a和过程b的热化学方程式分别为
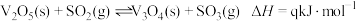 、
、 。请写出过程c的热化学方程式:
。请写出过程c的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题。
(1)常温下,0.1molCl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为_______ 。
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
①2O2(g)+N2(g)=N2O4(1) △H1
②N2(g)+2H2(g)=N2H4(1) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=_______ ,联氨和N2O4可作为火箭推进剂的主要原因为_______ 。
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是_______ (至少答出两点)。
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(1)常温下,0.1molCl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
①2O2(g)+N2(g)=N2O4(1) △H1
②N2(g)+2H2(g)=N2H4(1) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】煤燃烧后的主要产物是CO、CO2。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
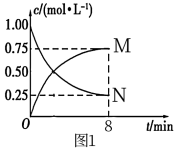

①图1中N表示的是______ (填化学式);0~8min内,以氢气表示的平均反应速率v(H2)=_______ mol • L-1 • min-1。
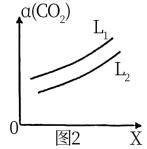
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是____________ (填“温度”或“压强”),L1________ (填“>”或“<”)L2。
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g) 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K_____________ 。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。


①图1中N表示的是
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g)
 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表中的数据是破坏 物质中的化学键所消耗的能量
物质中的化学键所消耗的能量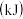 :
:
根据上述数据回答下列问题:
(1)下列氢化物中,最稳定的是___________ 。
A. B.
B. C.
C.
(2)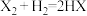 (X代表
(X代表 、
、 、
、 )的反应是
)的反应是___________ 反应(填“吸热”或“放热”)。
(3)相同条件下, (X代表
(X代表 、
、 、
、 )分别与氢气反应,消耗等物质的量的氢气时,放出或吸收热量最多的是
)分别与氢气反应,消耗等物质的量的氢气时,放出或吸收热量最多的是___________ 。
(4)若无上表中的数据,你能正确回答出问题(3)吗?请说明理由。___________ 。
(5)写出 和
和 反应的热化学方程式:
反应的热化学方程式:___________ 。
 物质中的化学键所消耗的能量
物质中的化学键所消耗的能量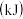 :
:| 物质 |  |  |  |  |  |  |  |
能量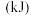 | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答下列问题:
(1)下列氢化物中,最稳定的是
A.
 B.
B. C.
C.
(2)
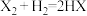 (X代表
(X代表 、
、 、
、 )的反应是
)的反应是(3)相同条件下,
 (X代表
(X代表 、
、 、
、 )分别与氢气反应,消耗等物质的量的氢气时,放出或吸收热量最多的是
)分别与氢气反应,消耗等物质的量的氢气时,放出或吸收热量最多的是(4)若无上表中的数据,你能正确回答出问题(3)吗?请说明理由。
(5)写出
 和
和 反应的热化学方程式:
反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知:2H2+O2 2H2O。
2H2O。
(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量___________ 。
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:___________ 。
②如把H2改为甲烷,则负极反应式为:_______ ,该甲烷燃料电池总反应的离子方程式为:________ 。
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为_______ ;若导线中转移电子2mol,则标况下,正极消耗的O2为_______ L
 2H2O。
2H2O。(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量
(2)原电池是直接把化学能转化为电能的装置。如图为原电池装置示意图:

①若A、B均为铂片,电解质为氢氧化钠溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,写出通入氢气的一极的电极反应式为:
②如把H2改为甲烷,则负极反应式为:
③已知N2H4(g)-空气燃料电池,电解质溶液为KOH溶液,则负极的电极反应式为
您最近一年使用:0次



