氯酸镁[Mg(ClO3)]常做催熟剂、除草剂等。实验室利用卤块(主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2的工艺流程如图:
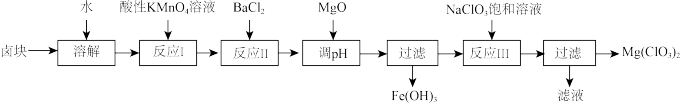
部分氢氧化物开始沉淀及沉淀完全的pH如表所示:
下列说法正确的是

部分氢氧化物开始沉淀及沉淀完全的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 8.9 |
| 沉淀完全的pH | 3.2 | 9.7 | 10.9 |
A.反应I的离子方程式为MnO +5Fe2++4H2O=Mn2++5Fe3++8OH- +5Fe2++4H2O=Mn2++5Fe3++8OH- |
B.反应II后溶液中大量存在的离子是Mg2+、Ba2+、Fe3+、SO 、Cl- 、Cl- |
| C.调pH时应控制溶液的pH在1.5~3.2 |
| D.反应III属于复分解反应,能够发生的原因是因为生成溶解度相对较小的Mg(ClO3)2 |
更新时间:2022-09-23 13:47:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组离子在指定溶液中一定能大量共存的是
A.麦芽糖溶液中:MnO 、Na+、 、Na+、 、H+ 、H+ |
B.该溶液加水后c(H+)/c(OH-)值变大:K+、Cu2+、Br-、 |
C. 溶液:CH3COO-、Ba2+、 溶液:CH3COO-、Ba2+、 、Br- 、Br- |
D.能使pH试纸变深蓝色的溶液:K+、Na+、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列各组离子在相应的条件下一定能大量共存的是
A.滴入甲基橙试液显红色的溶液中:K+、Na+、 、Cl- 、Cl- |
B.水电离产生的c(OH-)=1×10-10 mol/L的溶液中:Fe2+、Na+、 、Cl- 、Cl- |
C.溶液中c(H+)=1×10-14mol/L的溶液中:K+、Na+、 、S2- 、S2- |
D.0.1 mol/L的NaAlO2溶液中:K+、Al3+、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列离子方程式书写正确的是
A.金属Na投入 溶液中: 溶液中: |
B.碳酸钙与稀硝酸反应: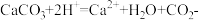 |
C.向碳酸氢铵溶液中加入过量的NaOH溶液: +OH-=NH3·H2O +OH-=NH3·H2O |
D.过量的Fe和稀硝酸反应: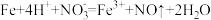 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某反应化学方程式为aP+bCuSO4+cH2O=dCu+eH3PO4+fH2SO4,下列选项中的数字与化学方程式中的a、b、c、d、e、f一一对应的是
| 选项 | a | b | c | d | e | f |
| A | 2 | 5 | 8 | 5 | 2 | 5 |
| B | 3 | 4 | 6 | 4 | 3 | 6 |
| C | 5 | 2 | 8 | 2 | 5 | 8 |
| D | 2 | 2 | 4 | 2 | 2 | 4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】工业利用含镍废料(以镍铁钙合金为主)制取NiC2O4(草酸镍),再经高温煅烧NiC2O4制取Ni2O3的流程如图所示。已知:NiC2O4、CaC2O4均难溶于水;Fe3+完全沉淀的pH约为3.7。下列说法正确的是
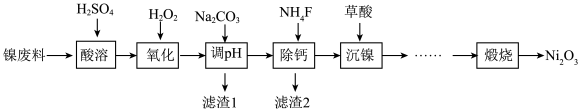
| A.酸溶时,可加入大量硫酸来提高“酸溶”效率 |
| B.调pH时,加入Na2CO3溶液,目的是使Fe3+转化为Fe2(CO3)3沉淀 |
C.沉镍时,发生反应的离子方程式为:Ni2++C2O =NiC2O4↓ =NiC2O4↓ |
D.煅烧时,反应的化学方程式为:2NiC2O4 Ni2O3+3CO↑+CO2↑ Ni2O3+3CO↑+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某黑色固体粉末可能是 Fe、FeO、CuO、C 中一种或几种。为了探究其成分,小明同学按照下 图所示流程进行了实验。

关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中一定含有 Fe;
②若步骤Ⅱ中无明显现象,则固体乙中最多只能 有四种物质;
③若步骤Ⅱ中 有气泡产生,则原固体可能是纯净物也可能是混合物;
④若步骤Ⅱ中有红色固体析出,则固体乙中一定无 CuO;
⑤固 体乙呈红色,则原固体中一定含有 Fe 和 CuO。 以上说法中正确的个数是

关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中一定含有 Fe;
②若步骤Ⅱ中无明显现象,则固体乙中最多只能 有四种物质;
③若步骤Ⅱ中 有气泡产生,则原固体可能是纯净物也可能是混合物;
④若步骤Ⅱ中有红色固体析出,则固体乙中一定无 CuO;
⑤固 体乙呈红色,则原固体中一定含有 Fe 和 CuO。 以上说法中正确的个数是
| A.1 个 | B.2 个 | C.3 个 | D.4 个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】铝土矿中主要含有Al2O3,还有少量Fe2O3,SiO2杂质,从铝土矿中冶炼金属铝方法如图所示(步骤①、②、③中每步反应结束后经过过滤才进行下一步反应)。下列有关说法不正确的是


| A.电解熔融氧化铝制取金属铝时加入冰晶石的作用是降低氧化铝熔融所需的温度 |
| B.步骤②的作用是除去母液1中的Fe3+和H+ |
C.步骤③生成沉淀的离子反应方程式为AlO +CO2+2H2O=HCO +CO2+2H2O=HCO +Al(OH)3↓ +Al(OH)3↓ |
| D.将步骤①和步骤②顺序颠倒,再通入足量CO2也能得到氢氧化铝沉淀 |
您最近一年使用:0次




