完成下列问题
(1)①写出实验室制备 胶体的化学方程式:
胶体的化学方程式:_______ 。
②分离提纯 胶体的方法是
胶体的方法是_______ 。
(2)下列几种导电性变化图象,把符合要求的图象序号填在相应的题目后面括号中。
A. B.
B.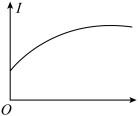 C.
C.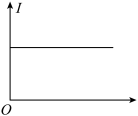
①向 溶液中通入
溶液中通入 直至过量
直至过量_______
②向 溶液通入少量
溶液通入少量
_______
③向氨水中通入 直至过量
直至过量_______
④向饱和石灰水中不断通入
_______
(3)向足量过氧化钠固体中通入一定量的 充分反应。写出上述反应的化学方程式,并用“双线桥”法表示电子转移的方向和数目:
充分反应。写出上述反应的化学方程式,并用“双线桥”法表示电子转移的方向和数目:_______ 。
(1)①写出实验室制备
 胶体的化学方程式:
胶体的化学方程式:②分离提纯
 胶体的方法是
胶体的方法是(2)下列几种导电性变化图象,把符合要求的图象序号填在相应的题目后面括号中。
A.
 B.
B. C.
C.
①向
 溶液中通入
溶液中通入 直至过量
直至过量②向
 溶液通入少量
溶液通入少量
③向氨水中通入
 直至过量
直至过量④向饱和石灰水中不断通入

(3)向足量过氧化钠固体中通入一定量的
 充分反应。写出上述反应的化学方程式,并用“双线桥”法表示电子转移的方向和数目:
充分反应。写出上述反应的化学方程式,并用“双线桥”法表示电子转移的方向和数目:
更新时间:2022-09-15 08:49:14
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等,Na2FeO4可用作净水剂等。
(1)氯化铁溶液加入氨水反应的离子方程式为___________ 。
(2)氯化铁常用于净水,是因为铁离子转化为 胶体,使水中悬浮物聚沉,
胶体,使水中悬浮物聚沉, 胶体分散质微粒直径的范围是
胶体分散质微粒直径的范围是___________ 。实验室利用饱和氯化铁溶液制备 胶体的离子方程式为:
胶体的离子方程式为:
___________ 。
(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得: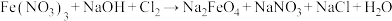 (未配平)。上述反应中氧化剂为
(未配平)。上述反应中氧化剂为___________ ,还原产物为___________ ,消耗1个Cl2转移电子数为___________ 。
(1)氯化铁溶液加入氨水反应的离子方程式为
(2)氯化铁常用于净水,是因为铁离子转化为
 胶体,使水中悬浮物聚沉,
胶体,使水中悬浮物聚沉, 胶体分散质微粒直径的范围是
胶体分散质微粒直径的范围是 胶体的离子方程式为:
胶体的离子方程式为:(3)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得:
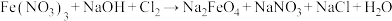 (未配平)。上述反应中氧化剂为
(未配平)。上述反应中氧化剂为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】用分类的思想研究物质及其性质是学习化学的一种重要方法。现有下列九种物质:① ,②干冰,③饱和
,②干冰,③饱和 溶液,④稀硫酸,⑤
溶液,④稀硫酸,⑤ ,⑥液态氯化氢,⑦
,⑥液态氯化氢,⑦ 胶体,⑧蔗糖,⑨铜片
胶体,⑧蔗糖,⑨铜片
(1)上述物质中,属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 能导电的有___________ 。
(2)请写出⑤的电离方程式___________ 。
(3)由③制备⑦的化学方程式为___________ 。
 ,②干冰,③饱和
,②干冰,③饱和 溶液,④稀硫酸,⑤
溶液,④稀硫酸,⑤ ,⑥液态氯化氢,⑦
,⑥液态氯化氢,⑦ 胶体,⑧蔗糖,⑨铜片
胶体,⑧蔗糖,⑨铜片(1)上述物质中,属于电解质的有
(2)请写出⑤的电离方程式
(3)由③制备⑦的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】请回答下列问题:
(1)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备Fe(OH)3胶体的化学反应方程式:_______ 。
(2)向所得的Fe(OH)3胶体中逐滴加入硫酸溶液至过量,出现的现象:_______ ,原因:_______ 。
(3)欲除去Fe(OH)3胶体中混有的NaCl,操作名称是_______ 。
(4)当光束通过下列物质时,不能观察到丁达尔现象的是
(5)下列实际应用与胶体知识有关的是
(1)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备Fe(OH)3胶体的化学反应方程式:
(2)向所得的Fe(OH)3胶体中逐滴加入硫酸溶液至过量,出现的现象:
(3)欲除去Fe(OH)3胶体中混有的NaCl,操作名称是
(4)当光束通过下列物质时,不能观察到丁达尔现象的是
| A.淀粉溶液 | B.蔗糖溶液 | C.一定条件下形成的云、雾、烟 | D.Fe(OH)3胶体 |
| A.高压静电除尘 | B.血液透析 | C.明矾净水 | D.用盐卤制豆腐 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题
(1)FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请完成NaClO3氧化FeCl2的离子方程式:
____ +____Fe2++______=____Cl-+____Fe3++________,
+____Fe2++______=____Cl-+____Fe3++________,____________
(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________ 。
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________ 。
(3)NO被H2O2氧化为 的离子方程式为
的离子方程式为___________ 。
(4)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中 (B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和
(B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和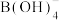 ,其离子方程式为
,其离子方程式为___________ 。
(1)FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请完成NaClO3氧化FeCl2的离子方程式:
____
 +____Fe2++______=____Cl-+____Fe3++________,
+____Fe2++______=____Cl-+____Fe3++________,(2)①PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
②PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
(3)NO被H2O2氧化为
 的离子方程式为
的离子方程式为(4)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中
 (B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和
(B元素的化合价为+3价)与Fe2+反应生成纳米铁粉、H2和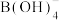 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】填写下列表格
| 实验 | 现象 | 离子反应方程式 |
| ①向盛有2mLCuSO4溶液的试管中加入2mLNaOH溶液 | ||
| ②向盛有2mLNaOH稀溶液的试管里滴入几滴酚酞溶液,再用滴管向试管里慢慢滴入稀盐酸 | ||
| ③向盛有2mLNa2CO3溶液的试管加入2mL盐酸溶液 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在反应2H2SO4 (浓)+Cu CuSO4+2H2O+SO2 ↑中,
CuSO4+2H2O+SO2 ↑中,
(1)氧化剂是________ ;还原剂是________ ;氧化产物是________ ;还原产物是_______
(2)作为氧化剂的H2SO4和参加反应H2SO4物质的量之比为________ ;被还原的H2SO4和未被还原的H2SO4物质的量之比为________ ;氧化产物和还原产物物质的量之比为________ ;氧化剂和还原剂物质的量之比为________ ;
(3)在下面的化学方程式上用双线桥标电子转移的方向和数目2H2SO4 (浓)+Cu CuSO4+2H2O+SO2 ↑
CuSO4+2H2O+SO2 ↑_________
(4)有1mol H2SO4参加反应,被氧化的Cu为______ mol,转移的电子数目为________ mol,生成的SO2为______ L(标准状况下)。
 CuSO4+2H2O+SO2 ↑中,
CuSO4+2H2O+SO2 ↑中,(1)氧化剂是
(2)作为氧化剂的H2SO4和参加反应H2SO4物质的量之比为
(3)在下面的化学方程式上用双线桥标电子转移的方向和数目2H2SO4 (浓)+Cu
 CuSO4+2H2O+SO2 ↑
CuSO4+2H2O+SO2 ↑(4)有1mol H2SO4参加反应,被氧化的Cu为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氧化还原反应是一类重要的化学反应,在工农业生产、日常生活中都有广泛的用途。亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应: 2NaNO2+4HI=2NO↑+2NaI+I2+2H2O
(1)用双线桥法标出该反应中电子转移的方向及数目:_______ ,被氧化的原子与被还原的原子数目之比为______ 。
(2)自来水中的 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。
____ Al+___  +
+_____ =____  +
+____ N2↑+____
(1)用双线桥法标出该反应中电子转移的方向及数目:
(2)自来水中的
 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。 +
+ +
+
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)以下物质中能导电的是____ (填序号,下同),属于电解质的是____ ,属于非电解质的是____ 。
①石墨 ②干冰 ③ MgO ④NaCl晶体 ⑤BaSO4固体 ⑥酒精溶液 ⑦氨水 ⑧熔融的KNO3 ⑨液态HCl
(2)在3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O的反应中,硝酸在反应中表现出来的性质是_______ ;氧化产物是_______ (填化学式);离子方程式为________ 。
(3)维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_____ 性(填氧化性或还原性)。
(4)以高锰酸钾为原料制备O2。写出该反应的化学方程式,并标出双线桥____________ 。
①石墨 ②干冰 ③ MgO ④NaCl晶体 ⑤BaSO4固体 ⑥酒精溶液 ⑦氨水 ⑧熔融的KNO3 ⑨液态HCl
(2)在3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O的反应中,硝酸在反应中表现出来的性质是
(3)维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(4)以高锰酸钾为原料制备O2。写出该反应的化学方程式,并标出双线桥
您最近一年使用:0次

 溶液与饱和NaHCO3溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下LiHCO3
溶液与饱和NaHCO3溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下LiHCO3

