完成下列问题
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应中还原剂是_______ ,氧化剂是_______ 。
(2)现有下列物质:①Cu、②HCl、③NH3、④NaCl、⑤CaCO3、⑥稀硫酸、⑦NaHSO4,其中属于电解质,但熔融状态下并不导电的是_______ (填序号),请写出NaHSO4在水溶液中的电离方程式_______ 。
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑。该反应中还原剂是
(2)现有下列物质:①Cu、②HCl、③NH3、④NaCl、⑤CaCO3、⑥稀硫酸、⑦NaHSO4,其中属于电解质,但熔融状态下并不导电的是
更新时间:2022-09-29 07:50:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求完成以下填空:
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是___________ (填序号),属于非电解质的有 ___________ (填序号),利用以上物质写出与离子方程式“H++OH- =H2O”相对应的一个化学方程式:___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目___________ (注明得失)。
②当消耗3g的NO时得到氧化产物的质量为___________ ,转移的电子的物质的量是 ___________ 。
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是___________ (填字母)。
A.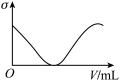 B.
B.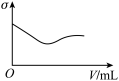 C.
C.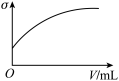
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②当消耗3g的NO时得到氧化产物的质量为
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是
A.
 B.
B. C.
C.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)现有以下物质,①纯 、②Cu、③
、②Cu、③ 固体、④熔融的
固体、④熔融的 、⑤酒精、⑥
、⑤酒精、⑥ 、⑦液氯、⑧
、⑦液氯、⑧ 溶液。
溶液。
能导电的物质有_______ (填序号,下间),属于非电解质的是_______ ,属于弱电解质的是_______ 。
(2)已知 (次磷酸)与足量的NaOH反应只生成一种盐
(次磷酸)与足量的NaOH反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。 属于
属于_______ 酸(填序号),
a.一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸
(3)已知高铁酸钾( )中的铁为+6价,是一种新型兼具净水和消毒功能的试剂,它能与盐酸发生如下反应
)中的铁为+6价,是一种新型兼具净水和消毒功能的试剂,它能与盐酸发生如下反应
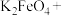 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
①配平该化学方程式____
②_______ 是氧化剂,_______ 是还原产物。
③被氧化的HCl与参加反应的HCl的物质的量之比为_______ 。
(1)现有以下物质,①纯
 、②Cu、③
、②Cu、③ 固体、④熔融的
固体、④熔融的 、⑤酒精、⑥
、⑤酒精、⑥ 、⑦液氯、⑧
、⑦液氯、⑧ 溶液。
溶液。能导电的物质有
(2)已知
 (次磷酸)与足量的NaOH反应只生成一种盐
(次磷酸)与足量的NaOH反应只生成一种盐 ,
, 水溶液中存在
水溶液中存在 分子。
分子。 属于
属于a.一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸
(3)已知高铁酸钾(
 )中的铁为+6价,是一种新型兼具净水和消毒功能的试剂,它能与盐酸发生如下反应
)中的铁为+6价,是一种新型兼具净水和消毒功能的试剂,它能与盐酸发生如下反应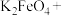 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
①配平该化学方程式
②
③被氧化的HCl与参加反应的HCl的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学与人类生活密切相关,现有以下物质:A.NaHCO3 B.Fe(OH)3胶体 C.冰醋酸(固态醋酸) D.葡萄糖(C6H12O6) E.K2Cr2O7 F.ClO2 G.Cu。请回答下列问题:
(1)①以上物质中属于电解质的是___________ (填字母序号)。
②A在水溶液中的电离方程式为___________ 。
(2)葡萄糖注射液标签上的部分内容如图所示:
①葡萄糖的摩尔质量为___________ 。
②该注射液中葡萄糖的物质的量浓度为___________ mol/L。(保留两位小数)
(3)实验室用K2Cr2O7固体配制500mL1mol/L的K2Cr2O7溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、___________ 、___________ 。定容时仰视刻度线会导致溶液浓度___________ (填“偏高”“偏低”或“无影响”)。
(4)ClO2是一种消毒效率高,污染小的水处理剂,实验室可通过以下反应制得: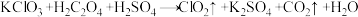 (未配平),在相同条件下,反应中产生的ClO2与CO2的体积比是
(未配平),在相同条件下,反应中产生的ClO2与CO2的体积比是___________ 。
(1)①以上物质中属于电解质的是
②A在水溶液中的电离方程式为
(2)葡萄糖注射液标签上的部分内容如图所示:
| 5%葡萄糖(C6H12O6)注射液 [性状]本品为无色透明溶液,甜味。 [规格]1000mL:50g |
②该注射液中葡萄糖的物质的量浓度为
(3)实验室用K2Cr2O7固体配制500mL1mol/L的K2Cr2O7溶液。配制时必需的玻璃仪器有:烧杯、量筒、玻璃棒、
(4)ClO2是一种消毒效率高,污染小的水处理剂,实验室可通过以下反应制得:
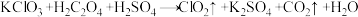 (未配平),在相同条件下,反应中产生的ClO2与CO2的体积比是
(未配平),在相同条件下,反应中产生的ClO2与CO2的体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是_______ 。
(2)通过实验可初步确定自来水中_______ (填“含有”或“不含有”)大量Ca2+、Mg2+;
(3)自来水中所含阴离子可以确定有_______ ,理由是(用离子方程式表示)_______ 。
II.NaHSO4通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热熔化时只能电离出两种不同离子。试回答下列问题:
(1)NaHSO4在水中和熔融状态下的电离有什么不同?(用电离方程式表示)_______ 。
(2)某同学探究溶液的导电性与离子浓度的关系,做了如下实验,滴定管是用于滴加BaCl2或NaOH溶液的仪器(烧杯中为NaHSO4溶液):

①滴加BaCl2溶液灯泡明亮程度有何变化?_______ 。
②滴加NaOH溶液灯泡明亮程度有何变化?_______ 。
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的Na2CO3溶液,又有白色沉淀生成;
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO3溶液,也产生白色沉淀。
请回答以下问题:
(1)不用做实验就可排除的离子是
(2)通过实验可初步确定自来水中
(3)自来水中所含阴离子可以确定有
II.NaHSO4通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热熔化时只能电离出两种不同离子。试回答下列问题:
(1)NaHSO4在水中和熔融状态下的电离有什么不同?(用电离方程式表示)
(2)某同学探究溶液的导电性与离子浓度的关系,做了如下实验,滴定管是用于滴加BaCl2或NaOH溶液的仪器(烧杯中为NaHSO4溶液):

①滴加BaCl2溶液灯泡明亮程度有何变化?
②滴加NaOH溶液灯泡明亮程度有何变化?
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)下列物质 ①Al ②NH3 ③CO2 ④H2SO4 ⑤AgCl ⑥蔗糖 ⑦NaCl溶液 ⑧盐酸 ⑨ 熔融KCl。
属于电解质的是_____________ ,属于非电解质的是 ________ ,能导电的是__________ 。(填序号)
(2)写出下列物质的电离方程式:
Na3PO4________________________________________________ ,
(NH4)2SO4__________________________________________________ 。
属于电解质的是
(2)写出下列物质的电离方程式:
Na3PO4
(NH4)2SO4
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂_______________ ,还原剂_________________ ;
(2)氧化产物______________________ ,还原产物________________ ;
(3)氧化剂与还原剂的质量之比_______________ ;
(4)用单线桥的方法表示该反应的电子转移情况_________________________ ;
(5)用双线桥的方法表示该反应的电子转移情况_________________ 。
(1)氧化剂
(2)氧化产物
(3)氧化剂与还原剂的质量之比
(4)用单线桥的方法表示该反应的电子转移情况
(5)用双线桥的方法表示该反应的电子转移情况
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)反应Fe2O3+2Al═Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是_______ 。在该反应中_______ 元素的化合价升高,该元素的原子_______ 电子,被_______ ;而_______ 元素的化合价降低,该元素的原子_______ 电子,被_______ 。该反应中,Fe2O3发生了_______ 反应,Al发生了_______ 反应,_______ 是氧化剂,_______ 是氧化产物,_______ 是还原剂。
(2)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目_______ 。
(3)写出Cu和AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目_______ 。
(1)反应Fe2O3+2Al═Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是
(2)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目
(3)写出Cu和AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】KClO3和浓盐酸在一定温度下反应会生成易爆物二氧化氯,其变化可表述为:___________KClO3+___________HCl(浓)=___________KCl+___________ClO2↑+___________Cl2↑+ ___________H2O
(1)氧化剂是___________ ,还原剂是___________ ;氧化产物是___________ ,还原产物是___________ 。
(2)浓盐酸在反应中显示出来的性质是___________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)请配平上述化学方程式___________ 。
(1)氧化剂是
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)请配平上述化学方程式
您最近一年使用:0次

 (CO
(CO ),试剂:
),试剂: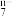 +14H+=6Fe3++2R3++7H2O,则R2O
+14H+=6Fe3++2R3++7H2O,则R2O

