按要求完成以下填空:
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是___________ (填序号),属于非电解质的有 ___________ (填序号),利用以上物质写出与离子方程式“H++OH- =H2O”相对应的一个化学方程式:___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目___________ (注明得失)。
②当消耗3g的NO时得到氧化产物的质量为___________ ,转移的电子的物质的量是 ___________ 。
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是___________ (填字母)。
A.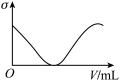 B.
B.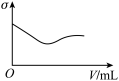 C.
C.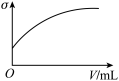
(1)现有下列10种物质:①稀盐酸,②纯醋酸,③干冰,④H2SO4,⑤AgCl,⑥熔融硝酸钠,⑦液态氯化氢,⑧Ba(OH)2,⑨Al2O3,⑩C2H5OH
上述物质中能导电的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②当消耗3g的NO时得到氧化产物的质量为
(3)下列所列举的是3张在一定温度下物质的导电能力(σ)随新物质加入量(V)的变化曲线图,向饱和食盐水中不断通入二氧化碳相符的变化曲线图是
A.
 B.
B. C.
C.
更新时间:2024-04-04 12:40:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有以下11种物质,请回答下列问题:
①铝②氧化钠③酒精④氨水⑤二氧化碳⑥碳酸钠⑦氢氧化钡溶液⑧硫酸氢钠⑨氯化氢⑩硫酸铝⑪稀硫酸
(1)上述物质中属于电解质的是___________ (填序号),属于非电解质的是___________ (填序号)
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为___________ 。
(3)写出物质⑧溶于水的电离方程式:___________ 。
(4)将足量的⑤通入澄清石灰水中,发生总反应的离子方程式为___________ 。
(5)取⑦和⑧的溶液以物质的量之比1:1发生反应的离子方程式为___________ 。
①铝②氧化钠③酒精④氨水⑤二氧化碳⑥碳酸钠⑦氢氧化钡溶液⑧硫酸氢钠⑨氯化氢⑩硫酸铝⑪稀硫酸
(1)上述物质中属于电解质的是
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(3)写出物质⑧溶于水的电离方程式:
(4)将足量的⑤通入澄清石灰水中,发生总反应的离子方程式为
(5)取⑦和⑧的溶液以物质的量之比1:1发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)现有以下物质:① 溶液 ②氨气 ③熔融氧化钠 ④盐酸 ⑤
溶液 ②氨气 ③熔融氧化钠 ④盐酸 ⑤ ⑥蔗糖 ⑦铜。能导电的有
⑥蔗糖 ⑦铜。能导电的有 ______ ;属于电解质的有______ 。(请用相应编号填写)
(2)选择适当的分离方法填空(填字母)。a.萃取分液 b.升华 c.结晶 d.分液 e.蒸馏 f.过滤
①从自来水中获得少量纯净的水______ 。
②从含有少量氯化钠的硝酸钾粉末中提纯硝酸钾______ 。
③用苯提取溴水中的溴单质______ 。
(3)用化学方程式表示工业制粗硅的原理______ 。
(1)现有以下物质:①
 溶液 ②氨气 ③熔融氧化钠 ④盐酸 ⑤
溶液 ②氨气 ③熔融氧化钠 ④盐酸 ⑤ ⑥蔗糖 ⑦铜。能导电的有
⑥蔗糖 ⑦铜。能导电的有 (2)选择适当的分离方法填空(填字母)。a.萃取分液 b.升华 c.结晶 d.分液 e.蒸馏 f.过滤
①从自来水中获得少量纯净的水
②从含有少量氯化钠的硝酸钾粉末中提纯硝酸钾
③用苯提取溴水中的溴单质
(3)用化学方程式表示工业制粗硅的原理
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列物质:① ②
② ③稀醋酸 ④石墨 ⑤固体
③稀醋酸 ④石墨 ⑤固体 ⑥
⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧酒精。请将序号分别填入下面的横线处:
溶液 ⑧酒精。请将序号分别填入下面的横线处:
(1)上述物质中属于酸性氧化物的是_______ ,属于酸式盐的是_______ 。
(2)上述状态可导电的_______ 属于电解质的是_______ 属于非电解质的是_______ 。
(3)写出⑥在水溶液中的电离方程式为_______ 。
(4)写出 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
(5)向⑥中加入 溶液至不再产生沉淀,反应的离子方程式为
溶液至不再产生沉淀,反应的离子方程式为_______ 。
 ②
② ③稀醋酸 ④石墨 ⑤固体
③稀醋酸 ④石墨 ⑤固体 ⑥
⑥ 溶液 ⑦
溶液 ⑦ 溶液 ⑧酒精。请将序号分别填入下面的横线处:
溶液 ⑧酒精。请将序号分别填入下面的横线处:(1)上述物质中属于酸性氧化物的是
(2)上述状态可导电的
(3)写出⑥在水溶液中的电离方程式为
(4)写出
 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为(5)向⑥中加入
 溶液至不再产生沉淀,反应的离子方程式为
溶液至不再产生沉淀,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列物质属于电解质且能导电的是
| A.食盐晶体 |
| B.乙醇 |
| C.水银 |
| D.熔融的生石灰 |
| E.固体BaSO4 |
| F.KNO3溶液 |
| G.熔融的氢氧化钠 |
| H.液态氯化氢 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)某兴趣小组做电解质导电实验,如图所示。
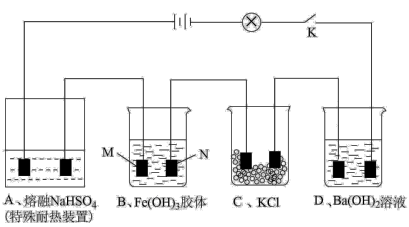
回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法___________ (写出一种方法即可)。
②装置A中电解质的电离方程式___________ ,在水溶液能与Fe反应生成氢气的离子方程式___________ 。
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是___________ (填①或②)。
②B点对应的溶液呈___________ (填“酸”、“碱”或“中”)性。
③起始点到D点之间发生反应的离子方程式为___________ 。
(1)某兴趣小组做电解质导电实验,如图所示。

回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法
②装置A中电解质的电离方程式
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是
②B点对应的溶液呈
③起始点到D点之间发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②的离子方程式为____
(2)反应②中,氧化产物与还原产物的质量比为_____
(3)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为____
(4)已知反应④:4HCl+O2 2Cl2+2H2O(g),该反应也能制得氯气。提醒一下,反应条件简单容易就发生,说明性质强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提醒一下,反应条件简单容易就发生,说明性质强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为____
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O ②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
(1)反应②的离子方程式为
(2)反应②中,氧化产物与还原产物的质量比为
(3)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为
(4)已知反应④:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气。提醒一下,反应条件简单容易就发生,说明性质强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气。提醒一下,反应条件简单容易就发生,说明性质强烈。则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原是一类重要的反应。
(1)已知反应:①Cu+2Fe3+=Cu2++2Fe2+,②Cu2++Fe=Cu+Fe2+,两个反应中各种离子的氧化性从强到弱的顺序是_____________ 。
(2)在反应MnO2+4HCl(浓) MnCl2+C12↑+2H2O中,当有0.2 mol电子转移时,产生氯气的体积(标准状况)是
MnCl2+C12↑+2H2O中,当有0.2 mol电子转移时,产生氯气的体积(标准状况)是__________________ 。
(3)用双线桥标出下列反应中电子转移的方向和数目,并指出氧化剂和还原剂。
Cl2 + SO2 + 2H2O = H2SO4 + 2HCl 双线桥_____________________________________
氧化剂:_____________ ,还原剂:_____________ ;
(4)已知反应: Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
铜与稀硝酸反应的离子方程式是_____________________________________ 。
(1)已知反应:①Cu+2Fe3+=Cu2++2Fe2+,②Cu2++Fe=Cu+Fe2+,两个反应中各种离子的氧化性从强到弱的顺序是
(2)在反应MnO2+4HCl(浓)
 MnCl2+C12↑+2H2O中,当有0.2 mol电子转移时,产生氯气的体积(标准状况)是
MnCl2+C12↑+2H2O中,当有0.2 mol电子转移时,产生氯气的体积(标准状况)是(3)用双线桥标出下列反应中电子转移的方向和数目,并指出氧化剂和还原剂。
Cl2 + SO2 + 2H2O = H2SO4 + 2HCl 双线桥
氧化剂:
(4)已知反应: Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
铜与稀硝酸反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO+2CO═N2+2CO2。
(1)碳元素的化合价_______ (填“升高”或“降低”),被_______ (填“氧化”或“还原”),CO是_______ 剂(填“氧化”或“还原”),NO是_______ 剂(填“氧化”或“还原”),发生_______ 反应。(填“氧化”或“还原”)
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2_______ 。
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2_______ 。
(4)若反应中消耗了2molCO,则生成N2的物质的量为_______ mol,转移电子的物质的量为_______ mol。
(1)碳元素的化合价
(2)用双线桥表示此反应中的电子得失情况2NO+2CO═N2+2CO2
(3)用单线桥表示此反应中的电子转移情况2NO+2CO═N2+2CO2
(4)若反应中消耗了2molCO,则生成N2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】配平下列方程式
(1) ;
;________ 。
(2) ;
;________ 。
(1)
 ;
;(2)
 ;
;
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.海带中含有丰富的碘,某学习小组设计并进行以下实验:
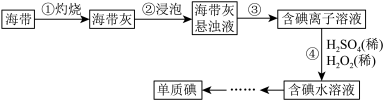
(1)步骤③的实验操作所用。用到的玻璃仪器有___________ 。步骤④的离子反应方程式为: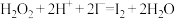 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。
(2)写出潮湿环境下KI与氧气反应的化学方程式:___________ 。
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:
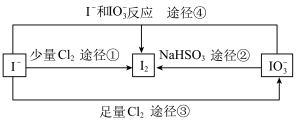
(3)四个途径中属于氧化还原反应的是___________ (填序号)。
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为: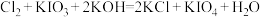 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(5)比较I2、 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:___________ 。

(1)步骤③的实验操作所用。用到的玻璃仪器有
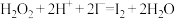 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。(2)写出潮湿环境下KI与氧气反应的化学方程式:
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:

(3)四个途径中属于氧化还原反应的是
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:
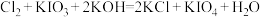 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)比较I2、
 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2015年8月12日天津港的爆炸事故中,有700 t氰化钠放在现场。NaCN为白色结晶颗粒(或粉末),熔点为563.7℃,沸点为1496℃,易溶于水,易水解,有剧毒。
回答下列问题:
(1)含NaCN的废液______________ (填“能”或“不能”)直接排放。
(2)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,写出其反应的化学方程式:___________________ 。该反应中氧化剂的电子式为________________ 。
(3)常见合成氰化钠的反应有以下三步:
①2Na+2M =2NaNH2+H2
②2NaNH2+C=Q+2H2↑
③Q+C=2NaCN
反应中M、Q两物质的化学式分别为_______ 、________ ,在反应②中,若生成1mol H2,则转移的电子数是_______ 。
回答下列问题:
(1)含NaCN的废液
(2)常温下,氰化钠能与双氧水反应,生成小苏打和某种碱性气体,大大降低其毒性,写出其反应的化学方程式:
(3)常见合成氰化钠的反应有以下三步:
①2Na+2M =2NaNH2+H2
②2NaNH2+C=Q+2H2↑
③Q+C=2NaCN
反应中M、Q两物质的化学式分别为
您最近一年使用:0次



