I.海带中含有丰富的碘,某学习小组设计并进行以下实验:
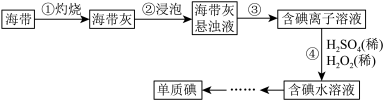
(1)步骤③的实验操作所用。用到的玻璃仪器有___________ 。步骤④的离子反应方程式为: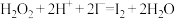 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是___________ ,还原剂是___________ 。步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现蓝色,说明有碘单质产生。
II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失, 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。
(2)写出潮湿环境下KI与氧气反应的化学方程式:___________ 。
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:
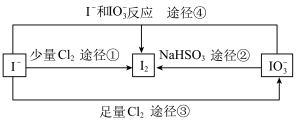
(3)四个途径中属于氧化还原反应的是___________ (填序号)。
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为: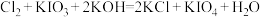 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(5)比较I2、 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:___________ 。

(1)步骤③的实验操作所用。用到的玻璃仪器有
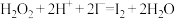 ,该离子反应中的氧化剂是
,该离子反应中的氧化剂是II.碘称为“智力元素”。过去食盐中KI作为加碘剂,但由于空气中氧气的作用,容易引起碘的损失,
 被氧气氧化成碘单质(I2),同时得到强碱性物质。
被氧气氧化成碘单质(I2),同时得到强碱性物质。(2)写出潮湿环境下KI与氧气反应的化学方程式:
III.现在的食盐里改添加性质稳定的KIO3,以满足人们需要。几种粒子之间有如图所示关系:

(3)四个途径中属于氧化还原反应的是
(4)在碱性条件下碘酸钾能被氯气氧化为高碘酸钾(KIO4),反应方程式为:
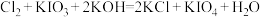 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)比较I2、
 和Cl2的氧化性强弱:
和Cl2的氧化性强弱:
更新时间:2023-12-19 09:27:30
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据下列变化或现象回答相应的问题。
①木炭完全燃烧②打开汽水瓶盖,有气泡产生 ③盐酸洒落在大理石地板上,有气泡产生④铁钉置于硫酸铜溶液中,铁钉表面上附上一层铜 ⑤用硝酸酸化的硝酸银检验自来水中的氯离子⑥铁器生锈⑦用硫酸可以清洗铁锈⑧二氧化碳通入澄清的石灰水变浑浊
(1)属于氧化还原反应的是________ (填序号)
(2)写出变化④⑦⑧的离子方程式
④_______ ⑦_______ ⑧________
①木炭完全燃烧②打开汽水瓶盖,有气泡产生 ③盐酸洒落在大理石地板上,有气泡产生④铁钉置于硫酸铜溶液中,铁钉表面上附上一层铜 ⑤用硝酸酸化的硝酸银检验自来水中的氯离子⑥铁器生锈⑦用硫酸可以清洗铁锈⑧二氧化碳通入澄清的石灰水变浑浊
(1)属于氧化还原反应的是
(2)写出变化④⑦⑧的离子方程式
④
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下几种物质:A.硝酸钾固体 B.纯醋酸 C.胆矾( )晶体 D.熔融的
)晶体 D.熔融的 E.乙醇 F.蔗糖 G.氯气 H.干冰 I.铝 J.碳酸氢钠固体 K.硫酸钾溶液 L.氨水。按要求回答下列问题:
E.乙醇 F.蔗糖 G.氯气 H.干冰 I.铝 J.碳酸氢钠固体 K.硫酸钾溶液 L.氨水。按要求回答下列问题:
(1)①以上物质中能导电的是___________ (填字母,下同)。
②以上物质中属于电解质的是___________ 。
③以上物质中属于氧化物的是___________ 。
④以上物质中属于混合物的是___________ 。
⑤以上物质中属于有机化合物的是___________ 。
⑥以上物质中属于单质且在氧化还原反应中只作还原剂的是___________ 。
(2)A溶于水的电离方程式为___________ ;D与K反应的离子方程式为___________ 。
 )晶体 D.熔融的
)晶体 D.熔融的 E.乙醇 F.蔗糖 G.氯气 H.干冰 I.铝 J.碳酸氢钠固体 K.硫酸钾溶液 L.氨水。按要求回答下列问题:
E.乙醇 F.蔗糖 G.氯气 H.干冰 I.铝 J.碳酸氢钠固体 K.硫酸钾溶液 L.氨水。按要求回答下列问题:(1)①以上物质中能导电的是
②以上物质中属于电解质的是
③以上物质中属于氧化物的是
④以上物质中属于混合物的是
⑤以上物质中属于有机化合物的是
⑥以上物质中属于单质且在氧化还原反应中只作还原剂的是
(2)A溶于水的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: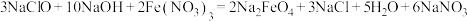 。回答下列问题:
。回答下列问题:
(1)用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
(2)制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)该反应的离子方程式为___________ 。
(4) 中Fe的价态为
中Fe的价态为___________ 价, 可用于自来水杀菌消毒的原因是
可用于自来水杀菌消毒的原因是___________ 。
(5)该反应中,每消耗 ,生成
,生成 的物质的量
的物质的量___________ mol,转移的电子数目为___________ (用 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: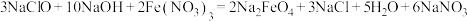 。回答下列问题:
。回答下列问题:(1)用氯气制备
 的反应原理为
的反应原理为(2)制备高铁酸钠的反应中
 体现了
体现了(3)该反应的离子方程式为
(4)
 中Fe的价态为
中Fe的价态为 可用于自来水杀菌消毒的原因是
可用于自来水杀菌消毒的原因是(5)该反应中,每消耗
 ,生成
,生成 的物质的量
的物质的量 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)比较Br-与Fe2+还原性相对强弱:Br-___ Fe2+(填“>”、“<”、“=”);用一个化学方程式说明Br-与Fe2+还原性相对强弱___ 。
(2)KSCN溶液是高中阶段常用试剂,其阴离子对应酸为HSCN(硫氰化氢),硫氰化氢分子中各原子均具有稀有气体稳定结构。写出HSCN(硫氰化氢)的结构式___ 。
(3)元素N与Cl的非金属性均较强,但常温下氮气远比氯气稳定,主要原因是___ 。
(2)KSCN溶液是高中阶段常用试剂,其阴离子对应酸为HSCN(硫氰化氢),硫氰化氢分子中各原子均具有稀有气体稳定结构。写出HSCN(硫氰化氢)的结构式
(3)元素N与Cl的非金属性均较强,但常温下氮气远比氯气稳定,主要原因是
您最近一年使用:0次
【推荐2】实验室迅速制取少量氯气可利用如下反应: KMnO4+ HCl→ KCl+MnCl2+ Cl2+ H2O(未配平),此反应常温下就可以迅速进行,结合信息,回答下列问题:
(1)上述反应中被氧化的元素为_____ ,还原产物________ 。
(2)当生成3.36L(标况下)Cl2,转移电子的物质的量为________
(3)Fe2+也能与MnO4-反应生成Mn2+,反应后Fe2+转化为_____ ,反应中Fe2+表现_____ (填“氧化”或“还原”,下同)性,发生_____ 反应。
(4)如果上述化学方程式中KMnO4和MnCl2的化学计量数都是2,则 HCl的化学计量数是____ 。
(5)实验室通常利用MnO2浓盐酸共热反应制取氯气,据此可知 KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为_________ 。
(1)上述反应中被氧化的元素为
(2)当生成3.36L(标况下)Cl2,转移电子的物质的量为
(3)Fe2+也能与MnO4-反应生成Mn2+,反应后Fe2+转化为
(4)如果上述化学方程式中KMnO4和MnCl2的化学计量数都是2,则 HCl的化学计量数是
(5)实验室通常利用MnO2浓盐酸共热反应制取氯气,据此可知 KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室常用KMnO4氧化溶质质量分数为36.5%的盐酸来快速制取氯气。方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)此反应中的氧化剂是___________ ,氧化产物是___________ ,还原性:HCl___________ MnCl2(填“大于”或“小于”)。
(2)若有1molKMnO4参加反应,转移电子的物质的量为___________ mol。
(3)2molKMnO4完全反应,产生的Cl2在标准状况下的体积为___________ L,有___________ molHCl发生反应,有___________ molHCl被氧化。
(4)若此盐酸的密度为1.2g·cm-3,其物质的量浓度为___________ 。HCl的电离方程式是___________ 。
(5)Cl2是一种有毒气体,实验室常用NaOH溶液来处理尾气。已知Cl2通入70℃的NaOH水溶液中,能同时发生两个自身的氧化还原反应(未配平):
NaOH+Cl2→NaCl+NaClO+H2O,NaOH+Cl2→NaCl+NaClO3+H2O。
反应完成后测得溶液中NaClO与NaClO3的数目之比为5∶2,则该溶液中NaCl与NaClO3的数目之比为___________ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)此反应中的氧化剂是
(2)若有1molKMnO4参加反应,转移电子的物质的量为
(3)2molKMnO4完全反应,产生的Cl2在标准状况下的体积为
(4)若此盐酸的密度为1.2g·cm-3,其物质的量浓度为
(5)Cl2是一种有毒气体,实验室常用NaOH溶液来处理尾气。已知Cl2通入70℃的NaOH水溶液中,能同时发生两个自身的氧化还原反应(未配平):
NaOH+Cl2→NaCl+NaClO+H2O,NaOH+Cl2→NaCl+NaClO3+H2O。
反应完成后测得溶液中NaClO与NaClO3的数目之比为5∶2,则该溶液中NaCl与NaClO3的数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】反应孕育着能量和物质变化,有些反应风驰电掣,流光溢彩,体现了化学之美。
(1)氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。若化学计量数b=3,d=4,则c=_______ 。
(2)将含lmol的H2O2溶液和含0.2molKMnO4的酸性溶液混合,紫色褪去,产生气泡。
①该气体是_______ 。
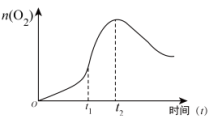
②产生气泡的速率与时间关系如图所示:推测t1~t2产生气泡的速率加快的原因_______ (只答一条即可);最终共产生气体_______ mol。
(3)在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有表中的若干种离子:
取该溶液100mL进行如表实验(气体体积在标准状况下测定):
将一定含有的离子及其物质的量浓度填入表中。
(4)已知固体Na2SO3受热易分解。实验流程和结果如图:
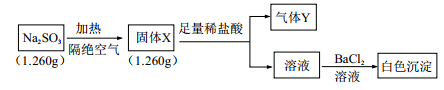
气体Y是一种纯净物,在标准状况下的密度为1.518g•L-1,请回答:
①气体Y分子式_______ ,白色沉淀的化学式_______ 。
②该流程中Na2SO3受热分解的化学方程式_______ 。
(1)氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为aHClO3=bO2↑+cCl2↑+dHClO4+eH2O。若化学计量数b=3,d=4,则c=
(2)将含lmol的H2O2溶液和含0.2molKMnO4的酸性溶液混合,紫色褪去,产生气泡。
①该气体是
②产生气泡的速率与时间关系如图所示:推测t1~t2产生气泡的速率加快的原因

(3)在Na+浓度为0.5mol•L-1的某澄清溶液中,还可能含有表中的若干种离子:
| 阳离子 | K+、Ag+、Ba2+ |
| 阴离子 | CO 、SiO 、SiO 、SO 、SO |
| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| II | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称重得固体质量 | 固体质量为2.4g |
| III | 在II的溶液中滴加BaCl2溶液 | 无明显现象 |
| 一定含有的离子 | Na+ | |||
| c/(mol•L-1) | 0.5 |

气体Y是一种纯净物,在标准状况下的密度为1.518g•L-1,请回答:
①气体Y分子式
②该流程中Na2SO3受热分解的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,完成下面题目。
(1)铅在蓄电池时发生的电池反应式为放电 ,正极反应式为
,正极反应式为_______ 。
(2) 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_
,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移________ 摩尔电子。
(3)将铝片和铜片用连接,插入硝酸中,原电池,正极为_______ (填入“铜”或“ 铝”,下同)将其插件烧成原电池,将其作为答案_______ 。
(4)锂电池的体积小、性能好,是常用的一次电池。该电池反应原理如图所示,其中电解质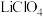 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成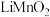 。
。

①外电路的电子方向是由_______ (填字母,下同)极流向_______ 极。
②电池正极反应式为_______ 。
③ 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(1)铅在蓄电池时发生的电池反应式为放电
 ,正极反应式为
,正极反应式为(2)
 溶液常用于腐蚀印刷电路铜板,发生反应:
溶液常用于腐蚀印刷电路铜板,发生反应: ,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_
,若将 此反应设计成原电池,则被腐蚀铜的质量为1.28g时,线路中转移_(3)将铝片和铜片用连接,插入硝酸中,原电池,正极为
(4)锂电池的体积小、性能好,是常用的一次电池。该电池反应原理如图所示,其中电解质
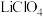 溶于混合有机溶剂中,
溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成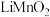 。
。
①外电路的电子方向是由
②电池正极反应式为
③
 可与KOH和
可与KOH和 在高温下反应,生成
在高温下反应,生成 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据反应事实推理反应方程式(属于离子反应的,写出离子反应方程式)。
(1)硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:_____________
(2)用KIO3氧化硫酸溶液中的KI:___________________
(3)用硫酸酸化的高锰酸钾溶液与硫酸亚铁反应:______________
(4)Na2SO3和Cl2反应生成H2SO4:___________
(5)久置油画白色(PbSO4)易变黑色(PbS),用双氧水揩擦后即可恢复,写出所发生反应的化学方程式:___ 。
(1)硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:
(2)用KIO3氧化硫酸溶液中的KI:
(3)用硫酸酸化的高锰酸钾溶液与硫酸亚铁反应:
(4)Na2SO3和Cl2反应生成H2SO4:
(5)久置油画白色(PbSO4)易变黑色(PbS),用双氧水揩擦后即可恢复,写出所发生反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现含有NaCl、MgCl2、CaCl2的混合液,某同学欲提取纯净的NaCl晶体,设计了如下实验:

请回答下列问题:
(1)写出沉淀中所含物质的化学式_________ ,①中加入的过量试剂为_____ 。
(2)上述流程中,加入过量稀盐酸的目的是______________ 。
(3)操作I的名称是_____ ,操作Ⅱ的名称是_____ 。
(4)操作I的要点是一帖二低三靠,其中二低是指__________ ,____________ 。操作Ⅱ中当______ (填仪器名称)中____________________________ (填现象)时停止加热。

请回答下列问题:
(1)写出沉淀中所含物质的化学式
(2)上述流程中,加入过量稀盐酸的目的是
(3)操作I的名称是
(4)操作I的要点是一帖二低三靠,其中二低是指
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某再回收利用公司对一厨房铁铝合金废旧家具进行回收利用,其流程如下图所示:
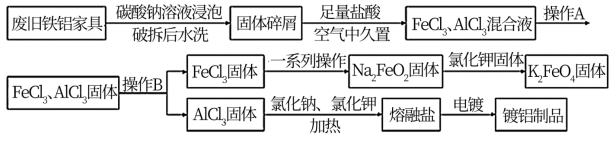
请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是_______________ ;在空气中久置的目的是_________________ 。
(2)同条件下Na2FeO4溶解度__________ K2FeO4溶解度(填“低于”,“高于”, “不确定”),推测K2FeO4在净水方面的作用_______________ 。(至少答两条)
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用__________ 。
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为___________________ 。(写出一个电极反应即可)
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为______________________ 。
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为____________ 。

请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是
(2)同条件下Na2FeO4溶解度
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为
您最近一年使用:0次



