回答下列问题
(1)某兴趣小组做电解质导电实验,如图所示。
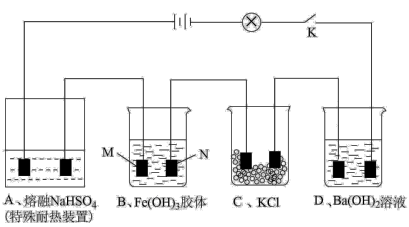
回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法___________ (写出一种方法即可)。
②装置A中电解质的电离方程式___________ ,在水溶液能与Fe反应生成氢气的离子方程式___________ 。
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是___________ (填①或②)。
②B点对应的溶液呈___________ (填“酸”、“碱”或“中”)性。
③起始点到D点之间发生反应的离子方程式为___________ 。
(1)某兴趣小组做电解质导电实验,如图所示。

回答下列问题:
①闭合开关K,发现灯泡不亮,使灯泡变亮的方法
②装置A中电解质的电离方程式
(2)向两份相同的Ba(OH)2溶液中,分别滴入浓度相等H2SO4和KHSO4,其导电能力随滴入溶液体积变化的曲线如下图所示。

①滴加H2SO4溶液的曲线是
②B点对应的溶液呈
③起始点到D点之间发生反应的离子方程式为
更新时间:2024-01-09 07:01:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质,是认识电解质的性质的前提:以下有①~⑩种物质:①H2 ②石墨 ③ HCl ④CO2 ⑤NaHCO3 ⑥熔融Ba(OH)2 ⑦氯水 ⑧稀硫酸 ⑨熔融硫酸铁 ⑩碳酸钙,请回答下列问题:
(1)上述状态下可导电的电解质的是_______ ;(填序号下同),属于非电解质的是________ ;氯水中具有漂白性的物质是________ (写化学式)。
(2)小苏打的水溶液能导电的原因是________ (用化学用语回答)。
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______ 。常用澄清石灰水检验CO2气体,反应的离子方程式是_______ 。
(4)40.0g硫酸铁固体溶于水配成250mL溶液, 的物质的量浓度为
的物质的量浓度为________ 。
(5)若将标准情况下aLHCl气体熔于1L水中,所得溶液稀盐酸的密度为dg/mL,则此时所得盐酸的物质的量浓度为______ mol·L-1。
(1)上述状态下可导电的电解质的是
(2)小苏打的水溶液能导电的原因是
(3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是
(4)40.0g硫酸铁固体溶于水配成250mL溶液,
 的物质的量浓度为
的物质的量浓度为(5)若将标准情况下aLHCl气体熔于1L水中,所得溶液稀盐酸的密度为dg/mL,则此时所得盐酸的物质的量浓度为______ mol·L-1。
A.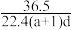 | B.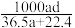 | C.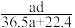 | D.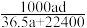 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
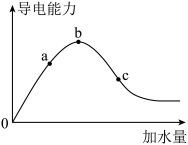
(1)“O”点导电能力为O的理由是_______ ;
(2)a、b、c三点溶液中c(H+)由小到大的顺序为_______ ;
(3)a、b、c三点中醋酸电离程度最大的是_______ ;水的电离程度最大的是_______ 。
(4)若使c点溶液的c(CH3COO-)提高,溶液的c(H+)减小,可采取的措施是_______。
①盐酸 ②冰醋酸 ③固体KOH ④加水 ⑤固体CH3COONa ⑥Zn粒

(1)“O”点导电能力为O的理由是
(2)a、b、c三点溶液中c(H+)由小到大的顺序为
(3)a、b、c三点中醋酸电离程度最大的是
(4)若使c点溶液的c(CH3COO-)提高,溶液的c(H+)减小,可采取的措施是_______。
①盐酸 ②冰醋酸 ③固体KOH ④加水 ⑤固体CH3COONa ⑥Zn粒
| A.①②③④⑤⑥ | B.①②③⑥ | C.①②⑤⑥ | D.③⑤⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】科学家在研究化学物质常对其进行分类,以便对同类物质的性质进行深入研究,物质分类及转化思想贯穿整个化学学科学习的始终。
下列物质:①硫酸;②硝酸钾溶液;③铜;④Na2O固体;⑤Ba(OH)2固体;⑥K2CO3固体;⑦二氧化碳;⑧熔融KHSO4;⑨AgCl固体;⑩氨气;
(1)能导电的是___________ (填序号,下同),属于电解质的是___________ ,属于非电解质的是___________ 。
(2)写出⑤、⑥在水溶液中的电离方程式:⑤___________ ,⑥___________ 。
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准是:___________ ;
(4)检验②中金属阳离子的实验方法是___________ (填实验操作的名称),确定该离子存在的现象是___________ 。
下列物质:①硫酸;②硝酸钾溶液;③铜;④Na2O固体;⑤Ba(OH)2固体;⑥K2CO3固体;⑦二氧化碳;⑧熔融KHSO4;⑨AgCl固体;⑩氨气;
(1)能导电的是
(2)写出⑤、⑥在水溶液中的电离方程式:⑤
(3)从物质的组成看KNO3、K2CO3、KHSO4都属于钾盐,其分类标准是:
(4)检验②中金属阳离子的实验方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)从对化合物的分类方法出发,指出下列各组物质中与其他类型不同的一种物质:
①Na2O CaO SO2 CuO______
②NaHCO3 Ca(HCO3)2 NH4HCO3 K2CO3______
(2)①石墨②胆矾③盐酸④KOH固体⑤Fe⑥乙醇⑦氨水⑧熔融BaSO4⑨醋酸⑩CO2⑪NaCl溶液,能导电的是______ ,电解质是 _________ ;
(3)写出下列物质在水溶液中的电离方程式:①NaHCO3______ ②KHSO4_____ ;
(4)若将NaHSO4与Ba(OH)2混合至SO42-完全沉淀,该反应的离子方程式为:__ 。
(1)从对化合物的分类方法出发,指出下列各组物质中与其他类型不同的一种物质:
①Na2O CaO SO2 CuO
②NaHCO3 Ca(HCO3)2 NH4HCO3 K2CO3
(2)①石墨②胆矾③盐酸④KOH固体⑤Fe⑥乙醇⑦氨水⑧熔融BaSO4⑨醋酸⑩CO2⑪NaCl溶液,能导电的是
(3)写出下列物质在水溶液中的电离方程式:①NaHCO3
(4)若将NaHSO4与Ba(OH)2混合至SO42-完全沉淀,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温时,向体积均为V0、浓度均为1mol/L的HClO2和HBF4两种酸溶液中分别加水,稀释至体积为V,稀释过程中溶液pH随( )的变化如下图所示。
)的变化如下图所示。

回答下列问题:
(1)HBF4为___________ 酸(填“强”或“弱”)。
(2)HClO2的电离方程式为___________ 。
(3)b→c过程中,HBF4溶液被稀释了___________ 倍。
(4)中和等体积、pH均为3的这两种酸溶液,消耗NaOH的物质的量较多的是___________ (写出化学式)。
(5)依据a点,Ka(HClO2)=___________ (结果保留两位有效数字)。
 )的变化如下图所示。
)的变化如下图所示。
回答下列问题:
(1)HBF4为
(2)HClO2的电离方程式为
(3)b→c过程中,HBF4溶液被稀释了
(4)中和等体积、pH均为3的这两种酸溶液,消耗NaOH的物质的量较多的是
(5)依据a点,Ka(HClO2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据电解质溶液的知识,回答下列问题:
已知0.1mol·L-1的NaHSO4溶液中H+的浓度为0.1mol·L-1。
(1)写出NaHSO4在水溶液中的电离方程式:___________________________ 。
(2)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1:1混合,离子方程式为_______________ 。
(3)若向Ba(OH)2溶液中滴加NaHSO4溶液至溶液恰好呈中性,反应的离子方程式为___ 。
(4)向NaAlO2中滴加NaHSO4溶液,现象为:________________ ;请你用离子方程式解释产生上述现象的原因_____________________________ 。
已知0.1mol·L-1的NaHSO4溶液中H+的浓度为0.1mol·L-1。
(1)写出NaHSO4在水溶液中的电离方程式:
(2)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1:1混合,离子方程式为
(3)若向Ba(OH)2溶液中滴加NaHSO4溶液至溶液恰好呈中性,反应的离子方程式为
(4)向NaAlO2中滴加NaHSO4溶液,现象为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按要求回答下列问题:
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:_______ ;常用澄清石灰水检验CO2气体的离子方程式是_______ 。
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是_______ ;反应片刻后,可观察到有气体产生,其离子方程式是_______ 。
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片( )治疗胃酸过多的离子方程式为
)治疗胃酸过多的离子方程式为_______ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是 ,此物质不溶于水],反应的离子方程式为
,此物质不溶于水],反应的离子方程式为_______ 。
(4)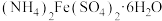 俗称摩尔盐,它是一种复盐,写出它的水溶液与足量稀氢氧化钠溶液混合时发生反应的离子方程式
俗称摩尔盐,它是一种复盐,写出它的水溶液与足量稀氢氧化钠溶液混合时发生反应的离子方程式_______ 。
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(
 )治疗胃酸过多的离子方程式为
)治疗胃酸过多的离子方程式为②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是
 ,此物质不溶于水],反应的离子方程式为
,此物质不溶于水],反应的离子方程式为(4)
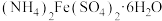 俗称摩尔盐,它是一种复盐,写出它的水溶液与足量稀氢氧化钠溶液混合时发生反应的离子方程式
俗称摩尔盐,它是一种复盐,写出它的水溶液与足量稀氢氧化钠溶液混合时发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质,请按要求完成以下两个问题。
(1)配平酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
__ H2O2+ ___  +
+____ =__ Mn2++___ O2↑+__
(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:____________________ 、_______________________ 。
(1)配平酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
 +
+(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
您最近一年使用:0次

 的物质的量浓度为
的物质的量浓度为

