常温时,向体积均为V0、浓度均为1mol/L的HClO2和HBF4两种酸溶液中分别加水,稀释至体积为V,稀释过程中溶液pH随( )的变化如下图所示。
)的变化如下图所示。

回答下列问题:
(1)HBF4为___________ 酸(填“强”或“弱”)。
(2)HClO2的电离方程式为___________ 。
(3)b→c过程中,HBF4溶液被稀释了___________ 倍。
(4)中和等体积、pH均为3的这两种酸溶液,消耗NaOH的物质的量较多的是___________ (写出化学式)。
(5)依据a点,Ka(HClO2)=___________ (结果保留两位有效数字)。
 )的变化如下图所示。
)的变化如下图所示。
回答下列问题:
(1)HBF4为
(2)HClO2的电离方程式为
(3)b→c过程中,HBF4溶液被稀释了
(4)中和等体积、pH均为3的这两种酸溶液,消耗NaOH的物质的量较多的是
(5)依据a点,Ka(HClO2)=
更新时间:2022-01-27 15:46:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按照要求书写方程式
(1)醋酸的电离方程式______________________________________________________
(2)小苏打治疗胃酸过多的离子反应方程式____________________________________
(3)澄清石灰水通入过量二氧化碳的离子反应方程式__________________________________
(4)碳酸氢钙溶液中加入少量苛性钠溶液的离子反应方程式_____________________________
(5)配平该方程式并用双线桥表示电子转移方向和数目
______ ______
______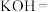 ______
______ ______
______ ______
______
______________________________________________________
(6)完成该方程式并用单线桥表示电子转移方向和数目某氧化还原反应中,反应物与生成物共有如下几种: ,
, ,
, ,
, ,
, ,
, 和
和 ,已知
,已知 在反应中得到电子
在反应中得到电子
______________________________________________________
(1)醋酸的电离方程式
(2)小苏打治疗胃酸过多的离子反应方程式
(3)澄清石灰水通入过量二氧化碳的离子反应方程式
(4)碳酸氢钙溶液中加入少量苛性钠溶液的离子反应方程式
(5)配平该方程式并用双线桥表示电子转移方向和数目
______
 ______
______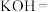 ______
______ ______
______ ______
______
(6)完成该方程式并用单线桥表示电子转移方向和数目某氧化还原反应中,反应物与生成物共有如下几种:
 ,
, ,
, ,
, ,
, ,
, 和
和 ,已知
,已知 在反应中得到电子
在反应中得到电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请运用所学知识,按照要求完成以下填空:
燃料电池具有能量转化率高等优点,工作时从负极连续通入 、①
、① 等燃料,从正极连续通入
等燃料,从正极连续通入 ,二者在电池内部(还有②KOH或③
,二者在电池内部(还有②KOH或③ 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 、④
、④ 或⑤
或⑤ 溶液等,同时产生电能。
溶液等,同时产生电能。
(1)在上述短文标有序号的物质中,属于电解质的是_______ (填序号,下同):属于酸性氧化物的是_______ 。
(2)请写出一种与 互为同素异形的物质
互为同素异形的物质_______ 。
(3)写出上文有序号物质中一种酸的电离方程式_______ 。
(4)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备 胶体的化学反应方程式
胶体的化学反应方程式_______ 。
燃料电池具有能量转化率高等优点,工作时从负极连续通入
 、①
、① 等燃料,从正极连续通入
等燃料,从正极连续通入 ,二者在电池内部(还有②KOH或③
,二者在电池内部(还有②KOH或③ 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 、④
、④ 或⑤
或⑤ 溶液等,同时产生电能。
溶液等,同时产生电能。(1)在上述短文标有序号的物质中,属于电解质的是
(2)请写出一种与
 互为同素异形的物质
互为同素异形的物质(3)写出上文有序号物质中一种酸的电离方程式
(4)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备
 胶体的化学反应方程式
胶体的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列物质:① 固体②
固体② ③
③ ④石墨⑤固体
④石墨⑤固体 ⑥熔融
⑥熔融 ⑦
⑦ 溶液⑧酒精。请将序号分别填入下面的横线处:
溶液⑧酒精。请将序号分别填入下面的横线处:
(1)上述状态可导电且属于电解质的有___________ 。
(2)属于弱电解质的是___________ ,属于非电解质的是___________ 。
(3)写出 和
和 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 、___________ 。
(4)写出 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(5)向⑥的水溶液中加入 溶液至不再产生沉淀,反应的离子方程式为
溶液至不再产生沉淀,反应的离子方程式为___________ 。
 固体②
固体② ③
③ ④石墨⑤固体
④石墨⑤固体 ⑥熔融
⑥熔融 ⑦
⑦ 溶液⑧酒精。请将序号分别填入下面的横线处:
溶液⑧酒精。请将序号分别填入下面的横线处:(1)上述状态可导电且属于电解质的有
(2)属于弱电解质的是
(3)写出
 和
和 在水溶液中的电离方程式为
在水溶液中的电离方程式为(4)写出
 和足量
和足量 溶液反应的离子方程式为
溶液反应的离子方程式为(5)向⑥的水溶液中加入
 溶液至不再产生沉淀,反应的离子方程式为
溶液至不再产生沉淀,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.水的电离平衡曲线如图所示。若以A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态为B点。
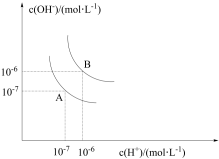
(1)在100℃时,Kw的表达式为________ ,在此温度下,Kw的值为________ mol2/L2。
(2)在室温下,将pH=9的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为________ 。
(3)室温时将pH为3的硫酸溶液稀释100倍,稀释后溶液中,c( )和c(H+)之比为
)和c(H+)之比为________ 。
Ⅱ.现有溶质为①CH3COOH,②HCl、③H2SO4的三种溶液,根据要求回答下列问题:
(1)写出①的电离方程式:________ 。
(2)当它们pH相同时,其物质的量浓度最大的是________ (填序号)。
(3)当它们的物质的量浓度相同时,其pH最小的是________ (填序号)。
(4)在室温下,将c(H+)均为0.1mol/L的三种酸分别加水稀释至原来的10倍,c(H+)由大到小的顺序为________ (填序号)。
(5)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为________ 。
(6)三种酸溶液的pH相同时,若消耗等量的Zn,则需三种酸溶液的体积大小关系为________ (填序号)。

(1)在100℃时,Kw的表达式为
(2)在室温下,将pH=9的Ba(OH)2溶液与pH=5的稀盐酸混合,欲使混合溶液pH=7,则Ba(OH)2溶液与盐酸的体积比为
(3)室温时将pH为3的硫酸溶液稀释100倍,稀释后溶液中,c(
 )和c(H+)之比为
)和c(H+)之比为Ⅱ.现有溶质为①CH3COOH,②HCl、③H2SO4的三种溶液,根据要求回答下列问题:
(1)写出①的电离方程式:
(2)当它们pH相同时,其物质的量浓度最大的是
(3)当它们的物质的量浓度相同时,其pH最小的是
(4)在室温下,将c(H+)均为0.1mol/L的三种酸分别加水稀释至原来的10倍,c(H+)由大到小的顺序为
(5)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为
(6)三种酸溶液的pH相同时,若消耗等量的Zn,则需三种酸溶液的体积大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题
(1)在常温下,将浓度均为 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=___________ (已知lg5=0.7)
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
试回答下列问题:
①下列四种离子结合质子能力最强的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
②常温下将 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是___________ 。
A. B.
B. C.
C. D.
D. E.
E.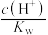
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
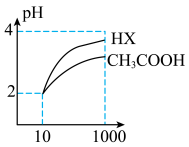
稀释后,HX溶液中水电离出来的
___________ (填“>”、“<”或“=”)醋酸溶液中水电离出来的 ;
; 的电离平衡常数
的电离平衡常数___________ (填“>”、“<”或“=”)HX的电离平衡常数,理由是___________ 。
(1)在常温下,将浓度均为
 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
| 化学式 |  |  |  |
| 电离平衡常数 |  |  、 、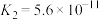 |  |
①下列四种离子结合质子能力最强的是
a.
 b.
b. c.
c. d.
d.
②常温下将
 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是A.
 B.
B. C.
C. D.
D. E.
E.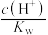
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

稀释后,HX溶液中水电离出来的

 ;
; 的电离平衡常数
的电离平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】强弱电解质在水中的行为是不同的。
(1)醋酸在水中的电离方程式为_______ ;醋酸电离平衡常数表达式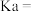
_______ 。
(2)室温下,用 溶液分别滴定
溶液分别滴定 的醋酸和盐酸溶液,滴定曲线如图所示。
的醋酸和盐酸溶液,滴定曲线如图所示。
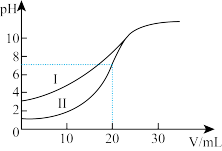
①Ⅱ表示滴定_______ 的曲线(填“盐酸”或“醋酸”)。
②当滴定到 时,消耗
时,消耗 溶液的体积大的是
溶液的体积大的是_______ (填“盐酸”或“醋酸”)。
③当 时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是
时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是_______ 。
④在上述滴定过程中,需要使用的玻璃仪器是_______ (填序号)。
A.碱式滴定管 B.锥形瓶 C.容量瓶 D.玻璃棒
(1)醋酸在水中的电离方程式为
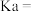
(2)室温下,用
 溶液分别滴定
溶液分别滴定 的醋酸和盐酸溶液,滴定曲线如图所示。
的醋酸和盐酸溶液,滴定曲线如图所示。
①Ⅱ表示滴定
②当滴定到
 时,消耗
时,消耗 溶液的体积大的是
溶液的体积大的是③当
 时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是
时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是④在上述滴定过程中,需要使用的玻璃仪器是
A.碱式滴定管 B.锥形瓶 C.容量瓶 D.玻璃棒
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
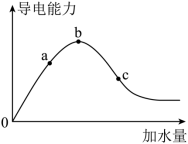
(1)“O”点导电能力为0的理由是_______ ;
(2)a、b、c三点溶液中c(H+)由小到大的顺序为_______ ;
(3)a、b、c三点中醋酸电离程度最大的是_______ ;
(4)若使c点溶液的c(CH3COO-)提高,溶液的c(H+)减小,可采取的措施是加入_______。
①盐酸 ②冰醋酸 ③固体KOH ④加水 ⑤固体CH3COONa ⑥Zn粒

(1)“O”点导电能力为0的理由是
(2)a、b、c三点溶液中c(H+)由小到大的顺序为
(3)a、b、c三点中醋酸电离程度最大的是
(4)若使c点溶液的c(CH3COO-)提高,溶液的c(H+)减小,可采取的措施是加入_______。
①盐酸 ②冰醋酸 ③固体KOH ④加水 ⑤固体CH3COONa ⑥Zn粒
| A.①②③④⑤⑥ | B.①②③⑥ | C.①②⑤⑥ | D.③⑤⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有常温下A、B、C、D四种溶液,它们分别是CH3COOH溶液、 HCl溶液、氨水、NaOH溶液中的一种,其相关数据如下:
(1)其中水的电离程度最大的是________ (填字母,下同)。
(2)将四份溶液同等稀释10倍后,溶液的pH最大的是________ 。
(3)某同学用B溶液分别滴定20.00 mL A溶液和20.00 mL C溶液,得到如图所示两条滴定曲线。
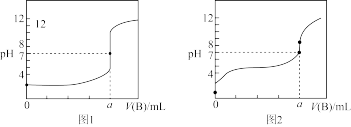
①a=________ mL,B溶液滴定C溶液的曲线是________ (填“图1”或“图2”)。
②图2中,当加入的B溶液为a mL时,溶液中离子浓度的大小关系为________ 。
| 溶液 | 物质的量浓度 | pH | 电离常数 |
| A | 0.01 mol·L-1 | 1.8×10-5 | |
| B | 12 | ||
| C | 0.01 mol·L-1 | ||
| D | 12 | 1.8×10-5 |
(2)将四份溶液同等稀释10倍后,溶液的pH最大的是
(3)某同学用B溶液分别滴定20.00 mL A溶液和20.00 mL C溶液,得到如图所示两条滴定曲线。

①a=
②图2中,当加入的B溶液为a mL时,溶液中离子浓度的大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:

(1)“O”点时,醋酸不能导电的原因是_____ 。
(2)a、b、c三点对应的溶液中c(H+)由小到大的顺序为_____ 。写出b点醋酸的电离方程式______ ,则醋酸的电离平衡常数Ka的表达式是______ 。
(3)a、b、c三点对应的溶液中,CH3COOH电离程度最大的是________ 。
(4)若使c点对应溶液中c(CH3COO-)增大,则下列措施中可行的是_____ 。
A.加热 B.加入NaOH稀溶液 C.加水 D.加入KOH固体 E.加入CH3COONa固体 F.加入锌粒

(1)“O”点时,醋酸不能导电的原因是
(2)a、b、c三点对应的溶液中c(H+)由小到大的顺序为
(3)a、b、c三点对应的溶液中,CH3COOH电离程度最大的是
(4)若使c点对应溶液中c(CH3COO-)增大,则下列措施中可行的是
A.加热 B.加入NaOH稀溶液 C.加水 D.加入KOH固体 E.加入CH3COONa固体 F.加入锌粒
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)已知室温时,0.1 mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=_______ mol∙L-1
②HA的电离平衡常数K=_______ 。
③由HA电离出的c(H+)约为水电离出的c(H+)的_______ 倍。
(2)部分弱酸的电离平衡常数如表:用“>”“<”或“=”填空。
①在相同浓度的HCOOH和HClO的溶液中,溶液导电能力:HCOOH_______ HClO。
② 的电离平衡常数表达式为
的电离平衡常数表达式为_______
③将少量CO2气体通入NaClO溶液中,写出该反应离子方程式_______ 。
(1)已知室温时,0.1 mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=
②HA的电离平衡常数K=
③由HA电离出的c(H+)约为水电离出的c(H+)的
(2)部分弱酸的电离平衡常数如表:用“>”“<”或“=”填空。
| 弱酸 | HCOOH | H2CO3 | HClO |
| 电离平衡常数/25 ℃ | K=1.77×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
②
 的电离平衡常数表达式为
的电离平衡常数表达式为③将少量CO2气体通入NaClO溶液中,写出该反应离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某一元弱酸(用HA表示)在水中的电离方程式是HA H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向___________ (填“正”或“逆”)反应方向移动。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向___________ (填“正”或“逆”)反应方向移动,溶液中c(A-)将___________ (填“增大”“减小”或“不变”,下同),溶液中c(OH-)将___________ 。
(3)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),则溶液显
)=c(Cl-),则溶液显___________ 性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=___________
(4)①现有室温下pH均为5的 溶液和
溶液和 溶液。两种溶液中,
溶液。两种溶液中,
___________ 。
② 和
和 两种溶液中,由水电离出的
两种溶液中,由水电离出的 分别为
分别为___________ 、___________ 。
 H++A-,回答下列问题:
H++A-,回答下列问题:(1)向溶液中加入适量NaA固体,以上平衡将向
(2)若向溶液中加入适量NaCl溶液,以上平衡将向
(3)在25℃下,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(4)①现有室温下pH均为5的
 溶液和
溶液和 溶液。两种溶液中,
溶液。两种溶液中,
②
 和
和 两种溶液中,由水电离出的
两种溶液中,由水电离出的 分别为
分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是一些物质在常温时的电离平衡常数:
(1)表中①②③④的酸性由强到弱的顺序为___________ (填标号)。
(2)常温下,0.1 mol/L NaHC2O4溶液显___________ (填“酸”、“碱”或“中”)性,理由是___________ 。
(3)请写出向 溶液中通入少量CO2气体发生反应的离子方程式:
溶液中通入少量CO2气体发生反应的离子方程式:___________ 。
(4)等浓度的(NH4)2CO3、(NH4)2C2O4、NH4Cl、CH3COONH4溶液中 的浓度由大到小的顺序是
的浓度由大到小的顺序是___________ 。
(5)等浓度、等体积的醋酸和氨水混合后溶液中各离子浓度大小关系是___________ 。
(6)向等体积、等pH的醋酸和草酸溶液中分别加入足量的质量、大小都相同的镁条,反应结束后收集到氢气的体积分别为V1、V2,其大小关系为___________ ,反应相同时间内的平均反应速率分别为v1、v2,其大小关系为___________ 。
(7)请利用以下装置和提供的试剂(乙酸溶液、碳酸钠粉末、饱和碳酸钠溶液、饱和碳酸氢钠溶液、苯酚钠溶液)设计比较CH3COOH、H2CO3和 酸性强弱的实验方案:
酸性强弱的实验方案:_______ (要说明各装置盛装的溶液)。
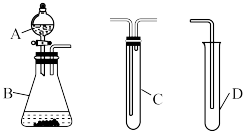
| ① | ② | ③ | ④ | ⑤ | |
| 物质 | CH3COOH | H2CO3 | H2C2O4 |  | NH3·H2O |
| K | 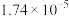 | 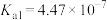  | 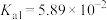 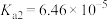 | 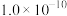 | 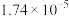 |
(2)常温下,0.1 mol/L NaHC2O4溶液显
(3)请写出向
 溶液中通入少量CO2气体发生反应的离子方程式:
溶液中通入少量CO2气体发生反应的离子方程式:(4)等浓度的(NH4)2CO3、(NH4)2C2O4、NH4Cl、CH3COONH4溶液中
 的浓度由大到小的顺序是
的浓度由大到小的顺序是(5)等浓度、等体积的醋酸和氨水混合后溶液中各离子浓度大小关系是
(6)向等体积、等pH的醋酸和草酸溶液中分别加入足量的质量、大小都相同的镁条,反应结束后收集到氢气的体积分别为V1、V2,其大小关系为
(7)请利用以下装置和提供的试剂(乙酸溶液、碳酸钠粉末、饱和碳酸钠溶液、饱和碳酸氢钠溶液、苯酚钠溶液)设计比较CH3COOH、H2CO3和
 酸性强弱的实验方案:
酸性强弱的实验方案:
您最近一年使用:0次



