回答下列问题
(1)在常温下,将浓度均为 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=___________ (已知lg5=0.7)
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
试回答下列问题:
①下列四种离子结合质子能力最强的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
②常温下将 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是___________ 。
A. B.
B. C.
C. D.
D. E.
E.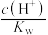
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
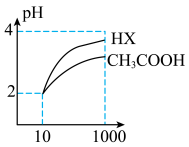
稀释后,HX溶液中水电离出来的
___________ (填“>”、“<”或“=”)醋酸溶液中水电离出来的 ;
; 的电离平衡常数
的电离平衡常数___________ (填“>”、“<”或“=”)HX的电离平衡常数,理由是___________ 。
(1)在常温下,将浓度均为
 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
| 化学式 |  |  |  |
| 电离平衡常数 |  |  、 、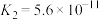 |  |
①下列四种离子结合质子能力最强的是
a.
 b.
b. c.
c. d.
d.
②常温下将
 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是A.
 B.
B. C.
C. D.
D. E.
E.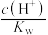
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

稀释后,HX溶液中水电离出来的

 ;
; 的电离平衡常数
的电离平衡常数
更新时间:2023-11-13 14:36:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,现有5种溶液:
①pH=1的稀硫酸② 稀硫酸③pH=1的盐酸④pH=1的氢氟酸⑤
稀硫酸③pH=1的盐酸④pH=1的氢氟酸⑤ 氢氟酸溶液
氢氟酸溶液
常温下,氢氟酸的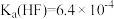 。
。
(1)若锌片形状相同,在相同条件下与上述5种溶液反应,开始产生氢气的速率最快的是______ 。(填写序号)
(2)等体积的上述5种溶液分别与足量的锌粒完全反应,在相同条件下产生氢气体积最大的是___________ 。(填写序号)
(3)等体积的①、②、③、⑤溶液与等浓度的氢氧化钠溶液恰好完全中和,消耗NaOH溶液体积最大的是___________ 。(填写序号)
(4)③中水电离出的 为
为___________  。
。
(5)25℃时,⑤中 约为
约为___________  。
。
①pH=1的稀硫酸②
 稀硫酸③pH=1的盐酸④pH=1的氢氟酸⑤
稀硫酸③pH=1的盐酸④pH=1的氢氟酸⑤ 氢氟酸溶液
氢氟酸溶液常温下,氢氟酸的
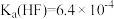 。
。(1)若锌片形状相同,在相同条件下与上述5种溶液反应,开始产生氢气的速率最快的是
(2)等体积的上述5种溶液分别与足量的锌粒完全反应,在相同条件下产生氢气体积最大的是
(3)等体积的①、②、③、⑤溶液与等浓度的氢氧化钠溶液恰好完全中和,消耗NaOH溶液体积最大的是
(4)③中水电离出的
 为
为 。
。(5)25℃时,⑤中
 约为
约为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲、乙、丙、丁代表不同的一元酸,常温下,将它们分别和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合后溶液的pH如下表所示:
完成下列填空:
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?___________
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为___________ 。
(3)从实验3分析,该混合溶液中离子浓度由大到小的顺序是___________ 。
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=___________ mol·L-1
| 实验序号 | 所用酸 | c(HA)/mol·L-1 | c(NaOH)/mol·L-1 | 混合后溶液的pH |
| 实验1 | 甲 | 0.1000 | 0.1000 | pH=a |
| 实验2 | 乙 | 0.1200 | 0.1000 | pH=7 |
| 实验3 | 丙 | 0.2000 | 0.1000 | pH>7 |
| 实验4 | 丁 | 0.1000 | 0.1000 | pH=10 |
(1)从实验1情况分析,如何判断HA是强酸还是弱酸?
(2)实验2的混合溶液中c(A-)和c(Na+)的大小关系为
(3)从实验3分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析实验4数据,写出混合溶液中下列算式的精确结果(列式即可):c(Na+)-c(A-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】任何物质的水溶液都存在水的电离平衡,其电离方程式可表示为H2O H++OH-。请回答下列有关问题:
H++OH-。请回答下列有关问题:
(1)现欲使水的电离平衡向右移动,且所得溶液呈酸性,可以选择的方法有_______ 。
A.加热至100℃ B.加入NaHSO4(s) C.加入CH3COONa(s) D.加入NH4Cl(s)
(2)在t℃时,测得0.01 mol/L的NaOH溶液的pH=11,则该温度下水的离子积为_______ ,此温度_______ 25 ℃(选填“大于”“小于”或“等于”)。
(3)在25℃时,将pH=a的NaOH溶液Va L与pH=b的HCl溶液Vb L混合,请填写下列空白:
①若所得溶液呈中性,且a=11,b=3,则Va∶Vb=_______ 。
②若所得混合溶液的pH=10,且a=12,b=2,则Va∶Vb=_______ 。
 H++OH-。请回答下列有关问题:
H++OH-。请回答下列有关问题:(1)现欲使水的电离平衡向右移动,且所得溶液呈酸性,可以选择的方法有
A.加热至100℃ B.加入NaHSO4(s) C.加入CH3COONa(s) D.加入NH4Cl(s)
(2)在t℃时,测得0.01 mol/L的NaOH溶液的pH=11,则该温度下水的离子积为
(3)在25℃时,将pH=a的NaOH溶液Va L与pH=b的HCl溶液Vb L混合,请填写下列空白:
①若所得溶液呈中性,且a=11,b=3,则Va∶Vb=
②若所得混合溶液的pH=10,且a=12,b=2,则Va∶Vb=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有常温下的六份溶液:①0.01mol·L-1CH3COOH溶液;②0.01mol·L-1HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液;⑤0.01mol·L-1CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;⑥0.01mol·L-1HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是__ (填序号,下同),水的电离程度相同的是__ 。
(2)若将②③混合后所得溶液pH=7,则消耗溶液的体积:②__ ③。(填“>”“<”或“=”)
(3)将六份溶液同等程度稀释10倍后,溶液的pH:
①__ ②,③__ ④,⑤___ ⑥。(填“>”“<”或“=”)
(1)其中水的电离程度最大的是
(2)若将②③混合后所得溶液pH=7,则消耗溶液的体积:②
(3)将六份溶液同等程度稀释10倍后,溶液的pH:
①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有常温条件下甲、乙、丙三种溶液,甲为 0.1 mol·L-1 的 NaOH 溶液, 乙为 0.1 mol·L-1的 HCl 溶液,丙为 0.1 mol·L-1 的 CH3COOH 溶液,试回答下列问题:
(1)甲溶液的 pH=_____ 。
(2)丙溶液中存在的电离平衡为_____ (用电离方程式表示)。
(3)甲、乙、丙三种溶液中由水电离出的 c(OH-)的大小关系为_____ 。
A. 甲=乙=丙 B. 甲=乙>丙 C.甲=乙<丙 D.无法判断
(4)某同学用甲溶液分别滴定 20.00 mL 乙溶液和 20.00 mL 丙溶液,得到如图所示两 条滴定曲线,请完成有关问题:

①甲溶液滴定丙溶液的曲线是_____ (填“图 1”或“图 2”);
②a=_____ mL。
(5)将等体积的甲溶液和丙溶液混合后,溶液呈_____ (填“酸性”、“中性”或 “碱性”)。溶液中离子浓度大小顺序为_________ 。
(1)甲溶液的 pH=
(2)丙溶液中存在的电离平衡为
(3)甲、乙、丙三种溶液中由水电离出的 c(OH-)的大小关系为
A. 甲=乙=丙 B. 甲=乙>丙 C.甲=乙<丙 D.无法判断
(4)某同学用甲溶液分别滴定 20.00 mL 乙溶液和 20.00 mL 丙溶液,得到如图所示两 条滴定曲线,请完成有关问题:

①甲溶液滴定丙溶液的曲线是
②a=
(5)将等体积的甲溶液和丙溶液混合后,溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)100°C时,KW=1.0×10﹣12,在该温度下,测得0.1mol/LNa2A溶液pH=6.
①H2A在水溶液中的电离方程式为_____ ;
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,与盐酸相比,H2A溶液产生的H2____ (填“多”、“少”或“一样多”).
(2)将0.4 mol/L HB溶液与0.2 mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液中c(Na+)>c(B-)。
①混合溶液中c(B﹣)_____ c(HB)(填“>”、“<” 或“=”);
②混合溶液中c(HB)+ c(B-)_____ 0.2mol/L(填“>”、“<”或“=”).
(3)已知在常温下常见弱酸的电离平衡常数Ka如表所示:
①少量二氧化碳通入NaClO溶液中的离子方程式_____ ;
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是_____ (填编号);
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c( CH3COO-)﹣c( CH3COOH)=___ mol/L(用数值列出计算式即可).
①H2A在水溶液中的电离方程式为
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,与盐酸相比,H2A溶液产生的H2
(2)将0.4 mol/L HB溶液与0.2 mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液中c(Na+)>c(B-)。
①混合溶液中c(B﹣)
②混合溶液中c(HB)+ c(B-)
(3)已知在常温下常见弱酸的电离平衡常数Ka如表所示:
| 溶质 | CH3COOH | H2CO3 | HClO | HCN |
| 电离平衡常数Ka | 1.75×10-5 | Ka1=4.4×10-7 Ka2=4.7×10-11 | 3.2×10-8 | 6.2×10-10 |
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c( CH3COO-)﹣c( CH3COOH)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有25℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中
_____ (填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式_____________ ;所得溶液的pH____ (填“<”“>”或“=”)7,用离子方程式表示其原因___________________________
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则c(SO42-)=________ 。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是______________ 。
(5)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是_____ (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______ (填”正向”“不”或“逆向”)移动,所滴加氨水的浓度为_______ mol·L-1。(NH3·H2O的电离平衡常数取Kb=2×10-5 mol·L-1)
(1)若向氨水中加入少量硫酸铵固体,此时溶液中

(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则c(SO42-)=
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是
(5)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)已知,常温下几种物质的电离常数如下: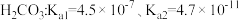 HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式
HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式___________ 。
(2)若向NaHSO3溶液中加入少量的Cl2,则溶液中pH将___________ (填“增大”“减小”或“不变”)。
(3)能证明Na2SO3溶液中存在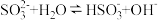 水解平衡
水解平衡 事实是___________(填序号)。
事实是___________(填序号)。
(4)已知室温下: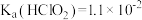 ,
,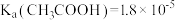 。25℃时,浓度均为0.1mol· L-1的NaClO2溶液和CH3COONa溶液,两溶液中
。25℃时,浓度均为0.1mol· L-1的NaClO2溶液和CH3COONa溶液,两溶液中
______ (填“>”“<”或“=”) 。若要使两溶液的pH相等,应
。若要使两溶液的pH相等,应_____ (填序号)。
a.向NaClO2溶液中加适量水 b.向NaClO2溶液中加适量NaOH固体
c.向CH3COONa溶液中加CH3COONa固体 d.向CH3COONa溶液中加适量的水
(5)直接加热CuCl2溶液得不到纯净的无水CuCl2固体,原因是___________ (用离子方程式表示)。
(1)已知,常温下几种物质的电离常数如下:
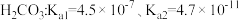 HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式
HClO:Ka=3.0×10-8。少量二氧化碳通入到次氯酸钠中的化学方程式(2)若向NaHSO3溶液中加入少量的Cl2,则溶液中pH将
(3)能证明Na2SO3溶液中存在
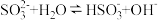 水解平衡
水解平衡 事实是___________(填序号)。
事实是___________(填序号)。| A.滴入酚酞溶液变红,再加H2SO4溶液红色褪去 |
| B.滴入酚酞溶液变红,微热后红色加深 |
| C.滴入酚酞溶液变红,再加BaCl2溶液后产生沉淀且红色褪去 |
| D.滴入酚酞溶液变红,再加NaOH溶液红色加深 |
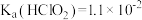 ,
,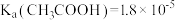 。25℃时,浓度均为0.1mol· L-1的NaClO2溶液和CH3COONa溶液,两溶液中
。25℃时,浓度均为0.1mol· L-1的NaClO2溶液和CH3COONa溶液,两溶液中
 。若要使两溶液的pH相等,应
。若要使两溶液的pH相等,应a.向NaClO2溶液中加适量水 b.向NaClO2溶液中加适量NaOH固体
c.向CH3COONa溶液中加CH3COONa固体 d.向CH3COONa溶液中加适量的水
(5)直接加热CuCl2溶液得不到纯净的无水CuCl2固体,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】溶洞的形成主要源于石灰岩受地下水的长期溶蚀,发生反应:CaCO3+CO2+H2O=Ca(HCO3)2。当受热或压强突然减小时溶解的Ca(HCO3)2会分解,从而形成钟乳石、石笋等奇妙景观。
(1)写出Ca(HCO3)2受热分解的离子方程式____ ;从平衡移动的角度解释压强减小时Ca(HCO3)2分解的原因_______ 。
(2)向Ca(HCO3)2饱和溶液中滴加酚酞,溶液呈很浅的红色。由此可得到的结论是:饱和溶液中Ca(HCO3)2水解程度__________ 且___________ 。
(3)常温下,H2CO3的电离常数Ka2=4.7×10-11。若测得5.0×10-3 mol/L Ca(HCO3)2溶液的pH为8.0,则溶液中c(CO32-)与c(OH-)的比值为___________ (简要写出计算过程)。
(1)写出Ca(HCO3)2受热分解的离子方程式
(2)向Ca(HCO3)2饱和溶液中滴加酚酞,溶液呈很浅的红色。由此可得到的结论是:饱和溶液中Ca(HCO3)2水解程度
(3)常温下,H2CO3的电离常数Ka2=4.7×10-11。若测得5.0×10-3 mol/L Ca(HCO3)2溶液的pH为8.0,则溶液中c(CO32-)与c(OH-)的比值为
您最近一年使用:0次



