填空
(1)醋酸在水溶液中的电离方程式为_______ 。
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2固体和H2O(1)。已知室温下2 gSiH4自燃放出热量89.2 kJ,该反应的热化学方程式为:_______ 。
(3)已知反应:N2(g) + O2(g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △ H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g)的反应焓变△H4为:_______ (用含△H1、△H2、△H3的式子表示)。
(1)醋酸在水溶液中的电离方程式为
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2固体和H2O(1)。已知室温下2 gSiH4自燃放出热量89.2 kJ,该反应的热化学方程式为:
(3)已知反应:N2(g) + O2(g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △ H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g)的反应焓变△H4为:
更新时间:2022-09-18 16:36:05
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】现有六种物质:①KHSO4固体 ②铝 ③CO2 ④氨水 ⑤液态HCl ⑥熔融Al2(SO4)3
(1)上述物质中,属于非电解质的是___________ (填序号,下同),除②以外, 能导电的是___________ ;将⑤加入到④中溶液的导电能力变化是___________ (填“增强”、“减弱”或“基本不变”)。
(2)⑥的电离方程式为___________ 。
(3)碳酸氢钠溶液与①的水溶液反应的离子方程式为___________ 。
(1)上述物质中,属于非电解质的是
(2)⑥的电离方程式为
(3)碳酸氢钠溶液与①的水溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求回答下列问题
(1)侯氏制碱法制得的“碱”的化学式:_______ 。
(2)写出碳酸氢钠在水中的电离方程式:_______ 。
(3)写出铁与水蒸气反应的化学方程式:_______ 。
(4)写出工业制漂白粉的化学方程式_______ 。
(1)侯氏制碱法制得的“碱”的化学式:
(2)写出碳酸氢钠在水中的电离方程式:
(3)写出铁与水蒸气反应的化学方程式:
(4)写出工业制漂白粉的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】NaHSO4通常为晶体,易溶于水,它溶于水时电离出三种不同的离子,溶液显酸性。NaHSO4受热熔化时只能电离出两种不同离子。试回答下列问题:
(1)NaHSO4在熔融状态下电离方程式为:___________ 。
(2)NaHSO4在物质分类中属于(酸、破、盐)中哪一类物质?___________ 。
(3)现有下列物质:①KCl晶体②液态HCl③CO2④汞⑤CaCO3固体⑥稀硫酸⑦酒精C2H5OH⑧熔融的NaCl。其中属于混合物的是(填序号,下同)___________ ;属于电解质的是___________ ;属于非电解质的是___________ ;能导电的有___________ 。
(1)NaHSO4在熔融状态下电离方程式为:
(2)NaHSO4在物质分类中属于(酸、破、盐)中哪一类物质?
(3)现有下列物质:①KCl晶体②液态HCl③CO2④汞⑤CaCO3固体⑥稀硫酸⑦酒精C2H5OH⑧熔融的NaCl。其中属于混合物的是(填序号,下同)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物[Mn(L)3]( ClO4)2是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知△H2= -299kJ/mol,则△H1 (kJ/mol )为_____________
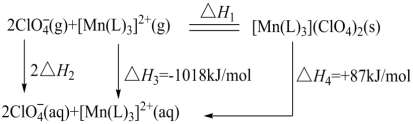
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
(a)CH4(g)+CO2(g) 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1
(b)CO2(g)+H2(g) CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2
(c)CH4(g) C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3
(d)2CO(g) CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4
(e)CO(g)+H2(g) H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5
根据盖斯定律,反应a的∆H1=_______ (写出一个代数式即可)。
(3)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应的热化学方程式为___________________________________ 。
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46kJ的热量。请写出KOH的稀溶液与的H2SO4稀溶液发生中和反应,表示中和热的热化学方程式为___________________ 。
(5)1mol CH4(g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:________________ 。

(1)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世瞩目的成就。碳酰肼类化合物[Mn(L)3]( ClO4)2是种优良的含能材料,可作为火箭推进剂的组分,其相关反应的能量变化如图所示,已知△H2= -299kJ/mol,则△H1 (kJ/mol )为
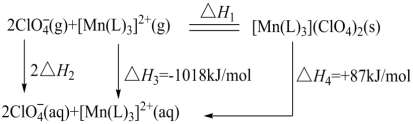
(2)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
(a)CH4(g)+CO2(g)
 2CO(g)+2H2(g) ∆H1
2CO(g)+2H2(g) ∆H1(b)CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2
CO(g)+H2O(g) ∆H2(c)CH4(g)
 C(s)+2H2(g) ∆H3
C(s)+2H2(g) ∆H3(d)2CO(g)
 CO2(g)+C(s) ∆H4
CO2(g)+C(s) ∆H4(e)CO(g)+H2(g)
 H2O(g)+C(s) ∆H5
H2O(g)+C(s) ∆H5根据盖斯定律,反应a的∆H1=
(3)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59kJ热量,则该反应的热化学方程式为
(4)已知含11.2gKOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46kJ的热量。请写出KOH的稀溶液与的H2SO4稀溶液发生中和反应,表示中和热的热化学方程式为
(5)1mol CH4(g)完全燃烧生成气态水的能量变化和1molS(g)燃烧的能量变化如图所示。在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为: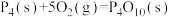 ;
;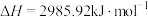 ;
;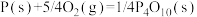 ;
;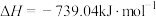 。1mol白磷转化为红磷时
。1mol白磷转化为红磷时______ (释放、吸收)______ kJ的热量。
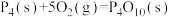 ;
;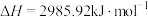 ;
;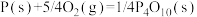 ;
;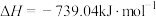 。1mol白磷转化为红磷时
。1mol白磷转化为红磷时
您最近一年使用:0次



