X、Y、Z、W、M、R、Q是短周期主族元素,部分元素的原子半径和化合价信息如下表所示:
M的焰色反应为黄色;X、Y、R位于周期表中不同周期;Q的单质为半导体材料。
(1)Y元素在周期表中的位置是_______ ;构成化合物 的化学键类型是
的化学键类型是_______ 。
(2)写出X、Y、R按原子个数之比为1:1:1形成的化合物的电子式_______ 。
(3)Y与W相比,非金属性较强的是_______ (用元素符号表示),下列事实能证明这一结论的是_______ (选填字母序号)。
a.常温下W的单质呈固态,Y的单质呈气态
b.Y与W形成的化合物中W呈正价
c.Y、W和M反应时,lmolY原子所得电子数少于1molW原子所得电子
d.Y的气态氢化物比W的气态氢化物稳定
(4)Q单质能与NaOH溶液反应放出 ,请写出该反应的离子方程式
,请写出该反应的离子方程式_______ 。
| X | Y | Z | W | |
| 原子半径/(nm) | 0.074 | 0.099 | 0.075 | 0.102 |
| 最高或最低化合价 | +7 | +5 | +6 | |
| −2 | −1 | −3 | −2 |
(1)Y元素在周期表中的位置是
 的化学键类型是
的化学键类型是(2)写出X、Y、R按原子个数之比为1:1:1形成的化合物的电子式
(3)Y与W相比,非金属性较强的是
a.常温下W的单质呈固态,Y的单质呈气态
b.Y与W形成的化合物中W呈正价
c.Y、W和M反应时,lmolY原子所得电子数少于1molW原子所得电子
d.Y的气态氢化物比W的气态氢化物稳定
(4)Q单质能与NaOH溶液反应放出
 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
更新时间:2022-09-22 20:37:12
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有A、B、C、D四种短周期主族元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图所示。回答下列问题:

(1)根据以上条件,A、B、C、D四种元素中有一种元素不能确定,它可代表2种元素,这2种元素是____ ,____ 。(填元素符号)。
(2)B、C可以形成1种3原子分子,该分子中B、C原子都达到8电子稳定结构,请写出该3原子分子的电子式____
(3)写出B原子的核外电子排布式____
(4)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:____ 。
(5)NH3•H2O的电离方程式为NH3•H2O⇌ +OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构
+OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构________ (填字母代号)。
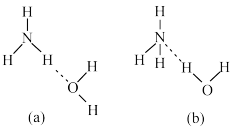

(1)根据以上条件,A、B、C、D四种元素中有一种元素不能确定,它可代表2种元素,这2种元素是
(2)B、C可以形成1种3原子分子,该分子中B、C原子都达到8电子稳定结构,请写出该3原子分子的电子式
(3)写出B原子的核外电子排布式
(4)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:
(5)NH3•H2O的电离方程式为NH3•H2O⇌
 +OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构
+OH-,试判断NH3溶于水后形成的NH3•H2O的合理结构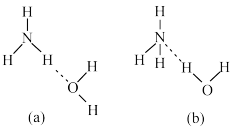
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D四种元素,A元素形成的-2价阴离子比氦的核外电子数多8个。B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质。C为原子核内有12个中子的二价金属,当2.4gC与足量热水反应时,在标准状态下放出氢气2.24L。D的M层上有7个电子。
(1) A、B、C、D各是什么元素(写元素符号):
A______ B______ C______ D_____
(2)用电子式表示C与D形成化合物的过程:_____ 。
(3)写出B、D的最高价氧化物的水化物反应的化学方程式:_____________ 。
(1) A、B、C、D各是什么元素(写元素符号):
A
(2)用电子式表示C与D形成化合物的过程:
(3)写出B、D的最高价氧化物的水化物反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,请参照元素①—⑥的位置回答下列问题:

(1)元素①的一种核素中,含有 1 个质子和 1 个中子,表示该核素组成的符号是_______ 。
(2)⑤的原子结构示意图是_______ 。
(3)上述元素中,原子半径最大的是_______ (写元素符号)。
(4)下列说法正确的是_______ (填序号)。
a.②、③组成的化合物只有一种
b.②的气态氢化物稳定性高于⑤
c.⑥在化合物中呈现的最高化合价为+7 价
(5)金属性: ③_______ ④( 填“>”或“<”),列举一条能证明该结论的实验事实:____ 。
(6)写出⑤的最高价氧化物对应水化物与Cu反应的化学方程式_______ 。写出⑥的单质置换出溴单质反应的离子方程式_______ 。

(1)元素①的一种核素中,含有 1 个质子和 1 个中子,表示该核素组成的符号是
(2)⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)下列说法正确的是
a.②、③组成的化合物只有一种
b.②的气态氢化物稳定性高于⑤
c.⑥在化合物中呈现的最高化合价为+7 价
(5)金属性: ③
(6)写出⑤的最高价氧化物对应水化物与Cu反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、P、Q、W、R、T是元素周期表短期中最常见的主族元素,且原子序数依次增大,其相关信息如下表:
(1)W元素位于周期表第________ 周期______ 族;T离子的结构示意图为____________ 。
(2)将Q、Z、R的简单离子的半径从大到小排序___________ (用离子符号表示);R、T两种元素的最高价氧化物对应水化物的酸(或碱)性由强到弱的顺序为__________ (用化学式表示)。
(3) X、Y、Z三种元素的简单氢化物中,稳定性最强的化合物的电子式为_________ ,化合物P2R溶液在空气中长期放置,会和氧气反应生成与过氧化钠的结构相似的物质P2R2,其溶液显黄色,则P2R2的电子式为______________ 。
(5)Q的单质能与X、Z形成的某种化合物反应,写出其化学方程式:______________ 。
(6)X与Q形成的lmol化合物Q2X3与水反应,生成2molMg(OH)2和1mol某气态烃,该烃分子中碳氢质量比为9: 1,写出该气态烃的结构简式_______ ,并写出Q2X3与水反应的化学方程式________ 。
| 元素 | 相关信息 |
| X | 其某一种同位素,被用作相对原子质量的标准 |
| Y | 其最高价氧化物对应水化物能与其气态氢化物发生化合反应 |
| P | 是短周期中(除稀有气体外)原子半径最大的元素 |
| Q | 存在质量数为25、中子数为13的核素 |
| W | 位于周期表第13列 |
| R | 与Z同族, 且最高价氧化物对应水化物的浓溶液常温下与W 单质会出现钝化现象 |
(1)W元素位于周期表第
(2)将Q、Z、R的简单离子的半径从大到小排序
(3) X、Y、Z三种元素的简单氢化物中,稳定性最强的化合物的电子式为
(4)根据下表中的信息,判断下列化合物固态时的晶体类型(填“离子晶体”……等)。
化合物 | x3Y4 | R2T2 |
主要物理性质 | 硬度可以和金刚石相媲美,熔点>3600℃ | 常温下是一种橙黄色液体,熔点为-76°C |
晶体类型 |
(5)Q的单质能与X、Z形成的某种化合物反应,写出其化学方程式:
(6)X与Q形成的lmol化合物Q2X3与水反应,生成2molMg(OH)2和1mol某气态烃,该烃分子中碳氢质量比为9: 1,写出该气态烃的结构简式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、R、W为原子序数依次增大的五种短周期元素。X原子最外层电子数是次外层的3倍;Y是短周期元素中金属性最强的元素;Z是生活中的常见金属,其氧化物常做耐高温材料;R最高正价与最低负价代数和为4;W的单质常用于漂白工业。回答下列问题:
(1)R元素的名称为:___________ ,W在周期表中的位置为:___________ 。
(2)已知W与Z单质化合得到的化合物甲在熔融状态下不能导电,但在水中能导电,由此可以判断甲属于___________ 化合物(选填:“离子”或“共价”),属于___________ (选填:“电解质”或“非电解质”)
(3)工业上常用Z单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种原子个数比为1∶1的坚硬耐磨的化合物,试写出该反应的化学方程式___________ 。
(4)化合物乙由元素X、Y组成,乙能与水剧烈反应,并产生大量气泡,与 反应产生氧气,乙可用做呼吸面具、潜水艇、太空舱等的供氧剂,且具有强氧化性,写出乙与
反应产生氧气,乙可用做呼吸面具、潜水艇、太空舱等的供氧剂,且具有强氧化性,写出乙与 反应的化学方程式
反应的化学方程式___________ 。
(5)为比较元素X和R的非金属性强弱,下列方法不可行的是___________ 。
a.比较这两种元素的单质与氢气化合的难易
b.比较这两种元素的气态氢化物的稳定性
c.比较这两种元素最高价含氧酸的酸性强弱
d.比较这两种元素氢化物水溶液的酸性强弱
(1)R元素的名称为:
(2)已知W与Z单质化合得到的化合物甲在熔融状态下不能导电,但在水中能导电,由此可以判断甲属于
(3)工业上常用Z单质与氨气在1700℃发生置换反应,生成一种最轻的气体和一种原子个数比为1∶1的坚硬耐磨的化合物,试写出该反应的化学方程式
(4)化合物乙由元素X、Y组成,乙能与水剧烈反应,并产生大量气泡,与
 反应产生氧气,乙可用做呼吸面具、潜水艇、太空舱等的供氧剂,且具有强氧化性,写出乙与
反应产生氧气,乙可用做呼吸面具、潜水艇、太空舱等的供氧剂,且具有强氧化性,写出乙与 反应的化学方程式
反应的化学方程式(5)为比较元素X和R的非金属性强弱,下列方法不可行的是
a.比较这两种元素的单质与氢气化合的难易
b.比较这两种元素的气态氢化物的稳定性
c.比较这两种元素最高价含氧酸的酸性强弱
d.比较这两种元素氢化物水溶液的酸性强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种元素。

回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式:___________ 。
(2)D的简单气态氢化物的VSEPR模型为___________ ,分子的空间结构为___________ 。
(3)第一电离能H___________ X(填“>”“<”或“=”),其原因是___________ 。
(4)电负性E___________ M(填“>”“<”或“=”)。
(5)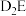 的沸点比
的沸点比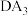 的沸点低,其原因是
的沸点低,其原因是___________ 。
(6) 的空间结构为
的空间结构为___________ ,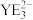 的键角比
的键角比 的键角小的原因是
的键角小的原因是___________ 。

回答下列问题:
(1)请写出H的单质与二氧化碳反应的方程式:
(2)D的简单气态氢化物的VSEPR模型为
(3)第一电离能H
(4)电负性E
(5)
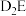 的沸点比
的沸点比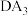 的沸点低,其原因是
的沸点低,其原因是(6)
 的空间结构为
的空间结构为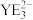 的键角比
的键角比 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分,回答以下问题:
(1) 与
与 的原子半径大小关系是:
的原子半径大小关系是:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)F与 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F___________  (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是___________ (填化学式)。
(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是___________ (填化学式)。
(4) 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为___________ (填“离子键”或“共价键”)。
(5)地壳中含量最高的金属元素是___________ ,能用来做光导纤维的是___________ 元素的氧化物(填元素符号)。
(6)C位于元素周期表中第___________ 周期第___________ 族,易以碳碳键和碳氢键形成甲烷 、乙烷
、乙烷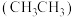 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于___________ (填“同系物”或“同分异构体”);乙烷与乙烯可相互转化,如:

 生成
生成 的反应类型为
的反应类型为___________
| C | N | F | ||||
 |  |  |  |  |  |
 与
与 的原子半径大小关系是:
的原子半径大小关系是:
 (填“>”或“<”)。
(填“>”或“<”)。(2)F与
 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是
(4)
 与
与 组成
组成
 所含的化学键类型为
所含的化学键类型为(5)地壳中含量最高的金属元素是
(6)C位于元素周期表中第
 、乙烷
、乙烷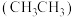 、乙烯
、乙烯 等烃类化合物。甲烷与乙烷属于
等烃类化合物。甲烷与乙烷属于
 生成
生成 的反应类型为
的反应类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图所示,a~i为9种短周期元素,其原子半径的相对大小、最高正价或最低负价变化如下:

根据判断出的元素回答问题:
(1)c在周期表中的位置是___________ (用化学符号表示,下同)。
(2)c、d的氢化物稳定性强弱为___________>___________,___________ ,h、i的最高价氧化物对应水化物的酸性强弱___________>___________,___________ 。
(3)f最高价氧化物对应水化物和e的最高价氧化物对应水化物反应的离子方程式为___________ 。
(4)某同学欲用如图所示装置证明b、g非金属性强弱,则X中试剂为盐酸,Y中试剂为碳酸钙固体,则Z中试剂为___________ ,W中反应的离子方程式为___________ 。


根据判断出的元素回答问题:
(1)c在周期表中的位置是
(2)c、d的氢化物稳定性强弱为___________>___________,
(3)f最高价氧化物对应水化物和e的最高价氧化物对应水化物反应的离子方程式为
(4)某同学欲用如图所示装置证明b、g非金属性强弱,则X中试剂为盐酸,Y中试剂为碳酸钙固体,则Z中试剂为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表是学习和研究化学科学的主要工具。下表是元素周期表的一部分,按要求作答。
(1)元素a位于周期表中第_______ 周期_______ 族。
(2)元素b属于_______ (填“金属”或“非金属”)元素,它的最高化合价是_______ 。
(3)碳的原子结构示意图为_______ 。
(4)地壳中含量最多的元素是_______ 。
(5)O与S中,原子半径较大的是_______ ,Cl-和K+中,离子半径较大的是_______ 。
(6) 与
与 中,热稳定性较弱的是
中,热稳定性较弱的是_______ 。
(7) 与
与 中,酸性较弱的是
中,酸性较弱的是_______ 。
(8)LiOH、 和KOH中,碱性最强的是
和KOH中,碱性最强的是_______ ,呈两性的是_______ 。
(9)元素Ca和Cl形成化合物的化学式是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
2 | Li | C | O | a | |||
3 | b | Al | Si | P | S | Cl | |
4 | K | Ca |
(2)元素b属于
(3)碳的原子结构示意图为
(4)地壳中含量最多的元素是
(5)O与S中,原子半径较大的是
(6)
 与
与 中,热稳定性较弱的是
中,热稳定性较弱的是(7)
 与
与 中,酸性较弱的是
中,酸性较弱的是(8)LiOH、
 和KOH中,碱性最强的是
和KOH中,碱性最强的是(9)元素Ca和Cl形成化合物的化学式是
您最近一年使用:0次



