铅蓄电池的总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O,请回答下列问题:
2PbSO4+2H2O,请回答下列问题:
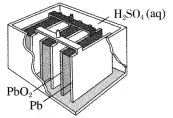
(1)放电时,正极的材料是_______ ;电解液中H2SO4浓度将变_______ (填“大”或“小”);电流方向从_______ (填“正”或“负”,下同)极流向_______ 极。当外电路通过1mol电子时,理论上负极板的质量增加_______ g。
(2)充电时Pb为_______ 极,Pb电极上的电极反应式为_______ 。
 2PbSO4+2H2O,请回答下列问题:
2PbSO4+2H2O,请回答下列问题:
(1)放电时,正极的材料是
(2)充电时Pb为
更新时间:2022-10-02 13:57:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图为氢氧燃料电池装置示意图。
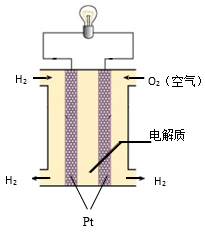
(1)该装置是利用反应 2H2+O2===2H2O 设计而成的,该反应能设计成电池的原因是___________________ 。
(2)该电池的正极反应物是_______________ ,判断依据是__________________ 。
(3)下列关于装置描述不正确 的是:__________ 。
a.导线是电子导体
b.该装置需要点燃才能产生电流
c.Pt电极主要作用是提供得失电子的场所
d.电子从通氧气一级沿导线转移到通氢气一级
(4)该装置是如何形成电流的?请进行完整说明:____________________ 。

(1)该装置是利用反应 2H2+O2===2H2O 设计而成的,该反应能设计成电池的原因是
(2)该电池的正极反应物是
(3)下列关于装置描述
a.导线是电子导体
b.该装置需要点燃才能产生电流
c.Pt电极主要作用是提供得失电子的场所
d.电子从通氧气一级沿导线转移到通氢气一级
(4)该装置是如何形成电流的?请进行完整说明:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学电池的发明,改变了人们的生活。___________ 。
(2)电流的流动方向是___________ ;能证明化学能转化为电能的实验现象是___________ 。
(3)常见的锌锰干电池构造示意图如下。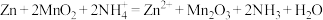 。
。
①该电池属于___________ (填“一次”、“二次”或“燃料”)电池。
②MnO2发生___________ (填“氧化”或“还原”)反应。
(2)电流的流动方向是
(3)常见的锌锰干电池构造示意图如下。
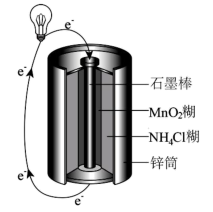
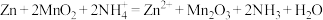 。
。①该电池属于
②MnO2发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1) 干电池应用广泛,其电解质溶液是
干电池应用广泛,其电解质溶液是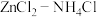 混合溶液。
混合溶液。
①该电池的负极材料是___________ 。电池工作时,电子流向___________ (填“正极”或“负极”)。
②若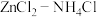 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速其电极的腐蚀,其主要原因是
,会加速其电极的腐蚀,其主要原因是___________ 。欲除去 ,最好选用下列试剂中的
,最好选用下列试剂中的___________ (填代号)。
A.NaOH B.Zn C.Fe D.
(2)目前已经使用的乙醇 燃料电池X极电极反应为
燃料电池X极电极反应为 ,则
,则
①X是___________ (填“正极”或“负极”),发生___________ (填“氧化”或“还原”)反应。该电池的电解质显___________ (填“酸性”“碱性”或“中性”)。
②若将电解质换成酸性介质,则正极反应为___________ ,通入乙醇的一极是___________ (填“正”或“负”)极。
③标准状况下,有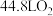 完全反应,则电路中转移
完全反应,则电路中转移___________ mol电子。
(1)
 干电池应用广泛,其电解质溶液是
干电池应用广泛,其电解质溶液是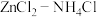 混合溶液。
混合溶液。①该电池的负极材料是
②若
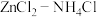 混合溶液中含有杂质
混合溶液中含有杂质 ,会加速其电极的腐蚀,其主要原因是
,会加速其电极的腐蚀,其主要原因是 ,最好选用下列试剂中的
,最好选用下列试剂中的A.NaOH B.Zn C.Fe D.

(2)目前已经使用的乙醇
 燃料电池X极电极反应为
燃料电池X极电极反应为 ,则
,则①X是
②若将电解质换成酸性介质,则正极反应为
③标准状况下,有
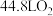 完全反应,则电路中转移
完全反应,则电路中转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
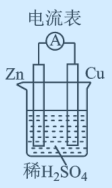
【推荐1】分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:
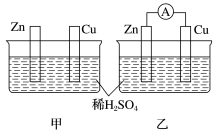
(1)以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向
F.乙溶液中 向铜片方向移动
向铜片方向移动
(2)变化过程中能量转化的主要形式:甲为_______ ;乙为_______ 。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:_______ ,总反应:_______ 。当电路中转移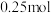 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为_______ g。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液氢离子浓度均减小
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向

F.乙溶液中
 向铜片方向移动
向铜片方向移动(2)变化过程中能量转化的主要形式:甲为
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式及总反应离子方程式:铜电极:
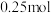 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组依据甲烷燃烧的反应原理,设计如图所示的装置。

(1)甲池中负极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为___________ (填“正极”“负极”“阴极”或“阳极”),乙池中总反应为___________ 。
(3)若乙池中溶液体积为 ,当B电极质量增加
,当B电极质量增加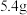 时,其
时,其 为
为___________ (忽略溶液体积变化);甲池中理论上消耗 的体积为
的体积为___________  (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中___________ (填“C”或“D”)极析出___________ g铜。

(1)甲池中负极的电极反应式为
(2)乙池中A(石墨)电极的名称为
(3)若乙池中溶液体积为
 ,当B电极质量增加
,当B电极质量增加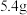 时,其
时,其 为
为 的体积为
的体积为 (标准状况下);假设乙池、丙池中的溶液均足量,丙池中
(标准状况下);假设乙池、丙池中的溶液均足量,丙池中
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。(电解质溶液均足量)。

请回答下列问题:
(1)甲池为___________ (填“原电池”“电解池”或“电镀池”),通入CH3OH电极的电极反应式为___________ 。
(2)乙池中A(石墨)电极的名称为___________ (填“正极”“负极”“阴极”或“阳极”),总反应离子方程式为:___________ 。
(3)当乙池中B极质量增加2.16 g时,甲池中理论上消耗O2的体积为___________ mL(标准状况下),此时若要将乙池复原需向乙池加一定量的___________ (填化学式)。
(4)丙池中电极C的电极反应为:___________ ,若丙池中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,丙中溶液的pH将___________ (填“增大”“减小”或“不变”)。

请回答下列问题:
(1)甲池为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加2.16 g时,甲池中理论上消耗O2的体积为
(4)丙池中电极C的电极反应为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应为__________ 。
(2)某学习小组依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计成原电池,则负极发生的电极反应为________ ,当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4g,则该原电池反应共转移了的电子数目是_________ 。
(3)燃料电池是一种高效、环境友好的供电装置,如下图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
①该电池的正极反应式__________________________ 。
②若该电池的效率80%,当外电路通过0.2mol电子时,消耗O2的体积____ L(标准状况)。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应为
(2)某学习小组依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计成原电池,则负极发生的电极反应为
(3)燃料电池是一种高效、环境友好的供电装置,如下图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①该电池的正极反应式
②若该电池的效率80%,当外电路通过0.2mol电子时,消耗O2的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应为 。
。
(1)铅蓄电池放电时,负极质量_______ (填“变大”“变小”或“不变”),正极反应式为_______ 。
(2)充电时,铅蓄电池的负极应连接外电源的_______ (填“正极”或“负极”)。
(3)用惰性电极电解足量饱和食盐水时,若用铅蓄电池作外电源,当两电极共收集到 (标准气体时,消耗铅蓄电池中
(标准气体时,消耗铅蓄电池中 的物质的量为
的物质的量为_______ 。
(4)若用铅蓄电池作外电源进行粗铜的精炼,则连接粗铜的电极为_______ (填“Pb”或“PbO2”)。
Ⅱ.一氧化碳催化加氢制甲醇的反应原理为
已知断开 下列化学键吸收的能量如下表所示:
下列化学键吸收的能量如下表所示:
(5)上表中的x为_______ 。
 。
。(1)铅蓄电池放电时,负极质量
(2)充电时,铅蓄电池的负极应连接外电源的
(3)用惰性电极电解足量饱和食盐水时,若用铅蓄电池作外电源,当两电极共收集到
 (标准气体时,消耗铅蓄电池中
(标准气体时,消耗铅蓄电池中 的物质的量为
的物质的量为(4)若用铅蓄电池作外电源进行粗铜的精炼,则连接粗铜的电极为
Ⅱ.一氧化碳催化加氢制甲醇的反应原理为

已知断开
 下列化学键吸收的能量如下表所示:
下列化学键吸收的能量如下表所示:| 化学键 |  |  | 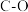 |  |  (CO的化学键) (CO的化学键) |
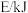 | x | 413 | 348 | 463 | 1076 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)锌锰(Zn﹣MnO2)干电池应用广泛,其电解质溶液是ZnCl2﹣NH4Cl混合溶液。
①电池工作时,电子流向_____ (填“正极”或“负极”)。
②若ZnCl2﹣NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是_____________________________________________ .
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。请根据上述情况判断:
①该蓄电池放电时,电解质溶液中阴离子移向_____ (填“正极”或“负极”);充电时,正极的电极反应式为:_____________________________ (用离子方程式表示);充电时,正极附近溶液的pH_____ (填“变大”、“减小”或“不变”)。
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是_____ .
①电池工作时,电子流向
②若ZnCl2﹣NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。请根据上述情况判断:
①该蓄电池放电时,电解质溶液中阴离子移向
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050molCl2,这时电池内消耗的H2SO4的物质的量至少是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。

已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO -2e-=PbSO4
-2e-=PbSO4
正极PbO2+4H++SO +2e-=PbSO4+2H2O
+2e-=PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式_____________ 。
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为________ 极。
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量)时,
①若收集到11.2 L(标准状况下)氯气,溶液pH=____________ 。
②若铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为________ L。

已知:铅蓄电池在放电时发生下列电极反应:
负极Pb+SO
 -2e-=PbSO4
-2e-=PbSO4正极PbO2+4H++SO
 +2e-=PbSO4+2H2O
+2e-=PbSO4+2H2O(1)请写出电解饱和食盐水的化学方程式
(2)若在电解池中C极一侧滴酚酞试液,电解一段时间后未呈红色,说明铅蓄电池的A极为
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量)时,
①若收集到11.2 L(标准状况下)氯气,溶液pH=
②若铅蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】酸性锌锰干电池是一种常用的一次电池,其结构如图所示。该电池在放电过程产生MnOOH和Zn(NH3)2Cl2。回答下列问题:
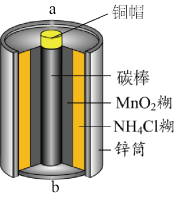
(1)该电池的正极为____ (填“a”或“b”)极,该电池总反应的化学方程式为____ 。
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。
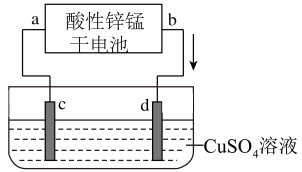
①电解一段时间后,石墨电极d出现的现象为____ ;石墨电极c上的电极反应式为____ 。
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为_____ (忽略电解前后溶液体积变化)。欲将电解后的溶液恢复至原溶液,应加入的试剂是____ ,其质量为____ g。

(1)该电池的正极为
(2)如图为电解100mL2.0mol·L-1CuSO4溶液的装置,该装置的电源为上述酸性锌锰干电池。

①电解一段时间后,石墨电极d出现的现象为
②当上述电池消耗3.25gZn时,电解后溶液中c(H+)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
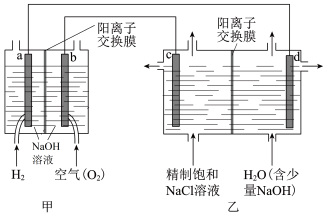
(1)a电极反应式是_______ 。
(2)乙装置中电解饱和NaCl溶液的化学方程式为_______ 。
(3)结合化学用语解释d极区产生NaOH的原因_______ 。
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用_______ 。
(5)下列说法正确的是_______ 。

(1)a电极反应式是
(2)乙装置中电解饱和NaCl溶液的化学方程式为
(3)结合化学用语解释d极区产生NaOH的原因
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用
(5)下列说法正确的是
| A.甲装置可以实现电能向化学能转化 |
| B.甲装置中Na+透过阳离子交换膜向a极移动 |
| C.乙装置中c极一侧流出的是淡盐水 |
| D.理论上,每消耗2.24LH2(标况下),可制得0.2molNaOH |
您最近一年使用:0次



