某学习小组为探究化合物X(仅含3种元素)的组成和性质,设计并完成如图实验(假设各步反应均完全,反应中气体完全逸出)。
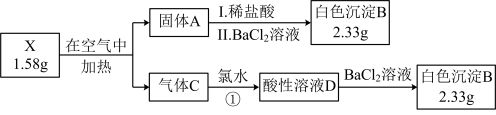
已知:固体A的焰色实验呈黄色;气体C可使品红溶液褪色,且加热后品红恢复红色。
(1)B的化学式是_______ ,写出C与氯水反应的离子方程式_______ 。
(2)X与稀硫酸反应产生气体C,并生成黄色沉淀,请写出X与稀硫酸反应的离子方程式_______ 。

已知:固体A的焰色实验呈黄色;气体C可使品红溶液褪色,且加热后品红恢复红色。
(1)B的化学式是
(2)X与稀硫酸反应产生气体C,并生成黄色沉淀,请写出X与稀硫酸反应的离子方程式
更新时间:2022-09-26 14:32:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组在一化工厂周围收集到一包10 g重的白色粉末状固体(已知其可能由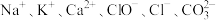 组成),欲探究其组成,进行了下列实验:
组成),欲探究其组成,进行了下列实验:
实验1:将白色粉末状固体溶于适量水中,过滤后得到50 mL滤液和1.165 g固体。
实验2:将实验1中所得固体加入盐酸中,完全溶解,有能使澄清石灰水变浑浊的气体产生。
实验3:将实验1中所得滤液分成两份,一份滴入纯碱溶液,无明显现象;将另一份溶液稀释至50 mL,向其中滴入2 mol/L的稀硫酸,仅产生黄绿色气体。当不再产生黄绿色气体时,测得消耗10 mL稀硫酸(不考虑反应可逆);再向溶液中加入10 mL2 mol/LBa(NO3)2溶液,恰好使 沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
(1)由实验1可推断白色粉末状固体中含有___________ (填离子符号)。
(2)写出实验2中固体溶于盐酸的离子方程式:___________ 。
(3)实验3中滴入稀硫酸时发生反应的离子方程式为___________ 。
(4)白色粉末状固体中氯元素的质量为___________ g。
(5)通过计算,判断该白色粉末状固体___________ (填“含”或“不含”) 元素,若含有
元素,若含有 元素,则实验1的滤液中c(K+)=
元素,则实验1的滤液中c(K+)=___________ mol/L(若不含,此空不填);还可以通过___________ 判断白色粉末状固体是否含有 元素。
元素。
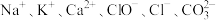 组成),欲探究其组成,进行了下列实验:
组成),欲探究其组成,进行了下列实验:实验1:将白色粉末状固体溶于适量水中,过滤后得到50 mL滤液和1.165 g固体。
实验2:将实验1中所得固体加入盐酸中,完全溶解,有能使澄清石灰水变浑浊的气体产生。
实验3:将实验1中所得滤液分成两份,一份滴入纯碱溶液,无明显现象;将另一份溶液稀释至50 mL,向其中滴入2 mol/L的稀硫酸,仅产生黄绿色气体。当不再产生黄绿色气体时,测得消耗10 mL稀硫酸(不考虑反应可逆);再向溶液中加入10 mL2 mol/LBa(NO3)2溶液,恰好使
 沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。(1)由实验1可推断白色粉末状固体中含有
(2)写出实验2中固体溶于盐酸的离子方程式:
(3)实验3中滴入稀硫酸时发生反应的离子方程式为
(4)白色粉末状固体中氯元素的质量为
(5)通过计算,判断该白色粉末状固体
 元素,若含有
元素,若含有 元素,则实验1的滤液中c(K+)=
元素,则实验1的滤液中c(K+)= 元素。
元素。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
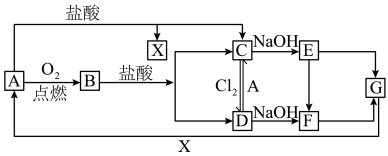
(1)写出A、C、F、G的化学式:A_______ ;C______ ;F_____ ;G_____ 。
(2)保存C溶液时要加固体A的原因是(用离子方程式解释)______ 。
(3)写出C→D的离子方程式_________ 。
(4)写出E→F的化学方程式:________ 。

(1)写出A、C、F、G的化学式:A
(2)保存C溶液时要加固体A的原因是(用离子方程式解释)
(3)写出C→D的离子方程式
(4)写出E→F的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E均为常见的物质,在一定的条件下相互转化关系如图所示(反应条件和部分产物已省略)。请回答:

(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为_______ ,A与E在一定条件下反应生成D的化学方程式为______________________ 。
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为酸,且C的组成中含有与A相同的元素。C的化学式为_________ ,A与E的水溶液反应生成D的离子方程式为___________ 。

(1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为
(2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为酸,且C的组成中含有与A相同的元素。C的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室用MnO2和浓盐酸反应制取Cl2,并进行Cl2性质的探究,发生装置如图①。

回答下列问题:
(1)仪器甲的名称是_______ 。
(2)制得的气体除去HCl杂质后,为得到干燥的Cl2,应通过_______ 装置(填“②”、“③”或“④”)。

(3)如图1,若在A处通入未干燥的氯气,当关闭B处弹簧夹时,C处的红布条看不到明显现象,当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是_______。
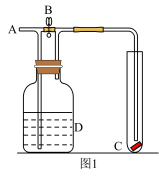
(4)如图2能证明氯水具有漂白性的是_______ (填“a”、“b”、“c”或“d”),其现象为_______ 。


回答下列问题:
(1)仪器甲的名称是
(2)制得的气体除去HCl杂质后,为得到干燥的Cl2,应通过

(3)如图1,若在A处通入未干燥的氯气,当关闭B处弹簧夹时,C处的红布条看不到明显现象,当打开B处的弹簧夹后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是_______。

| A.饱和食盐水 | B.NaOH溶液 | C.H2O | D.浓硫酸 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用下图所示装置在实验室制取纯净、干燥的 并探究其性质,回答下列问题:
并探究其性质,回答下列问题:

(1)发生装置中制取 的化学方程式是
的化学方程式是_______ 。
(2)除杂装置①中的试剂是_______ 。
(3)将虚线框中的收集装置补充完整_______ 。
(4)将制得的 溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象
溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象不能 得出相应结论的是_______ (填字母)。
 并探究其性质,回答下列问题:
并探究其性质,回答下列问题:
(1)发生装置中制取
 的化学方程式是
的化学方程式是(2)除杂装置①中的试剂是
(3)将虚线框中的收集装置补充完整
(4)将制得的
 溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象
溶于水得到氯水。在探究新制氯水成分及性质的实验中,依据下列操作和现象| 操作 | 现象 | 结论 | |
| a | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含 |
| b | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含 |
| c | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
| d | 向淀粉碘化钾试纸上滴加少量氯水 | 试纸变蓝 | 氯水具有氧化性 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。
已知:①A中反应为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。
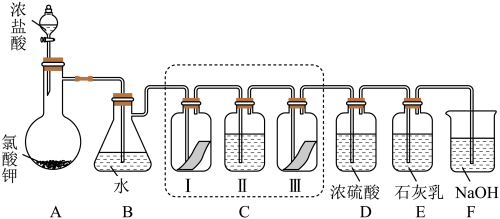
(1)写出B装置中反应的离子方程式_______ 。实验结束后,立即将B中溶液滴几滴在紫色石蕊试纸上,可观察到的现象是_______ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III 处依次放入的物质正确的是_______ (填编号)。
(3)F 装置的作用是(用离子方程式表示)_______
(4)为测定E中所得漂白粉的有效成分含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成分的质量分数为_______ (用含 a、b 的式子表示)。
已知:①A中反应为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。

(1)写出B装置中反应的离子方程式
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III 处依次放入的物质正确的是
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
(4)为测定E中所得漂白粉的有效成分含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2至不再产生沉淀为止,若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成分的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究小组在实验室研究Fe与浓H2SO4的反应,请按要求回答下列问题。
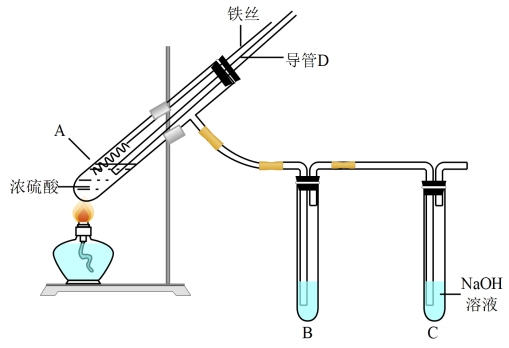
(1)仪器A的名称是___ ;试管C的作用是___ 。
(2)导管D的下端应位于___ (填“液面上”或“液面下”),导管D的作用有:①实验结束后排出装置中的SO2;②___ 。
(3)加热试管A,生成硫酸铁和SO2气体,写出该反应的化学方程式___ ;B的作用是检验产生的气体为SO2,可选用的试剂有___ 。
A.BaCl2溶液 B.品红溶液 C.酸性高锰酸钾溶液 D.饱和NaHSO3溶液
(4)加热过程中,始终未检测到可燃性气体;结束后,经检验A中既有Fe3+又有大量Fe2+,产生Fe2+的原因可能是___ (写离子方程式):检验反应后溶液中含有Fe2+的实验方案是___ 。

(1)仪器A的名称是
(2)导管D的下端应位于
(3)加热试管A,生成硫酸铁和SO2气体,写出该反应的化学方程式
A.BaCl2溶液 B.品红溶液 C.酸性高锰酸钾溶液 D.饱和NaHSO3溶液
(4)加热过程中,始终未检测到可燃性气体;结束后,经检验A中既有Fe3+又有大量Fe2+,产生Fe2+的原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学欲验证炭与浓硫酸反应产物的性质。现已将装置如图连接,请回答下列问题。

(1)烧瓶中发生反应的化学反应方程式是_______ 。
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是_______ ,通过洗气瓶C中无现象和_______ 的现象,证明反应有_______ (填化学式)生成。
(3)洗气瓶B中溶液颜色变浅,说明炭与浓硫酸反应的产物之一_______ (填化学式)具有_______ 的性质。
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到_______ 。

(1)烧瓶中发生反应的化学反应方程式是
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是
(3)洗气瓶B中溶液颜色变浅,说明炭与浓硫酸反应的产物之一
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】已知R为短周期主族元素,一种白色钠盐M的组成用通式 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:
(1)若在M溶液中滴加 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为__________ ,M的俗名是__________ 。
(2)若在M溶液中滴加 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为______________ 。
(3)若将M溶液加入酸性 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是__________ ,则M溶液和酸性 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为________ ,其中还原剂是__________ 。
(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为________ ,铜粉溶解的离子方程式为____________ ,工业上,氨催化氧化可制备X,其反应的化学方程式为__________ 。
 表示。为了探究R元素,进行如下实验:
表示。为了探究R元素,进行如下实验:(1)若在M溶液中滴加
 溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为
溶液,产生白色沉淀,过滤,在白色沉淀中滴加过量的盐酸,产生无色无味气体,白色沉淀完全溶解。则M的阴离子符号为(2)若在M溶液中滴加
 溶液,生成白色胶状物质,该白色胶状物质的化学式为
溶液,生成白色胶状物质,该白色胶状物质的化学式为(3)若将M溶液加入酸性
 溶液中,酸性
溶液中,酸性 溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是
溶液褪色;在M中滴加盐酸生成一种无色、有刺激性气味的气体,将该气体通入品红溶液中,品红溶液褪色,加热褪色的品红溶液,可能观察到的现象是 溶液反应使其溶液褪色的离子方程式为
溶液反应使其溶液褪色的离子方程式为(4)若在M溶液中加入铜粉,无明显现象,滴加适量稀硫酸,铜粉溶解,溶液变蓝色,生成气体X,将X与单质Y通入足量水中恰好发生化合反应,则同温同压下X与Y的体积比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某白色粉末A在农业上用作杀菌剂,进行下列实验:
①白色粉末A溶解在水中,得到蓝色溶液,分成等量的两份;
②在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀和蓝色溶液;
③在①中的另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
(1)A______________ B_______________ C_______________ (填化学式)
(2)反应③中的离子方程式为__________________________________________________
①白色粉末A溶解在水中,得到蓝色溶液,分成等量的两份;
②在其中一份蓝色溶液中加入适量的盐溶液B,恰好沉淀完全,过滤,得到白色沉淀和蓝色溶液;在此蓝色溶液中滴加酸化的AgNO3溶液又得到白色沉淀和蓝色溶液;
③在①中的另一份蓝色溶液中加入适量C溶液,恰好沉淀完全,过滤,得到蓝色沉淀和纯净的硫酸钾溶液。
根据实验现象推断:
(1)A
(2)反应③中的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】过二硫酸钾( )在高于100℃的条件下能发生分解反应:
)在高于100℃的条件下能发生分解反应: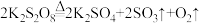 ,现称取一定质量的
,现称取一定质量的 固体(含有不分解的杂质),进行如下实验:加热过二硫酸钾使其完全分解,通过测定
固体(含有不分解的杂质),进行如下实验:加热过二硫酸钾使其完全分解,通过测定 的体积计算过二硫酸钾的纯度,并且收集
的体积计算过二硫酸钾的纯度,并且收集 (已知
(已知 的熔点为16.8℃)。
的熔点为16.8℃)。
(1)试从下图中选出必要的装置,连接成一套实验装置,这套装置从左向右的连接顺序(填装置编号)为_______→_______→_______→_______。_______
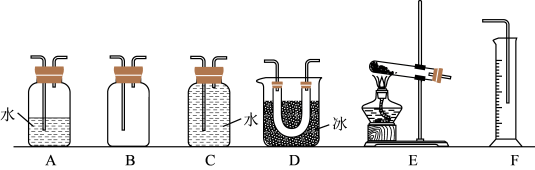
(2)将 与水反应,鉴定所得溶液中负离子的实验操作与相应的现象及结论是:
与水反应,鉴定所得溶液中负离子的实验操作与相应的现象及结论是:_______ 。
(3)硫酸工业中由 生成
生成 的化学方程式为:
的化学方程式为:_______ 。
(4)若实验时称取过二硫酸钾(式量为270)的质量为Wg,测得气体排出水的体积为amL(此时该气体的密度为143g/L),此过二硫酸钾的纯度为_______ 。
 )在高于100℃的条件下能发生分解反应:
)在高于100℃的条件下能发生分解反应: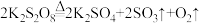 ,现称取一定质量的
,现称取一定质量的 固体(含有不分解的杂质),进行如下实验:加热过二硫酸钾使其完全分解,通过测定
固体(含有不分解的杂质),进行如下实验:加热过二硫酸钾使其完全分解,通过测定 的体积计算过二硫酸钾的纯度,并且收集
的体积计算过二硫酸钾的纯度,并且收集 (已知
(已知 的熔点为16.8℃)。
的熔点为16.8℃)。(1)试从下图中选出必要的装置,连接成一套实验装置,这套装置从左向右的连接顺序(填装置编号)为_______→_______→_______→_______。

(2)将
 与水反应,鉴定所得溶液中负离子的实验操作与相应的现象及结论是:
与水反应,鉴定所得溶液中负离子的实验操作与相应的现象及结论是:(3)硫酸工业中由
 生成
生成 的化学方程式为:
的化学方程式为:(4)若实验时称取过二硫酸钾(式量为270)的质量为Wg,测得气体排出水的体积为amL(此时该气体的密度为143g/L),此过二硫酸钾的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学习小组设计实验,探究二氧化硫的漂白性和还原性。
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。

①甲同学作对照实验的目的是______________________________________ 。
②足量碱石灰的作用是__________________________________________ 。
甲同学由此得出的实验结论是___________________________________________ 。
(2)还原性:
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是_________ ,检验该反应所得含氧酸根离子的方法是______ 。
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3溶液形成的混合色。 则②中红棕色变为浅绿色的原因是__________________ 。
乙同学得出的实验结论是:二氧化硫可还原三氯化铁。
(1)漂白性
甲同学用如图所示装置(气密性良好)进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。

①甲同学作对照实验的目的是
②足量碱石灰的作用是
甲同学由此得出的实验结论是
(2)还原性:
乙同学将SO2通入FeCl3溶液中,使其充分反应。
①SO2与FeCl3反应的离子方程式是
②实验中观察到溶液由黄色变为红棕色,静置一段时间,变为浅绿色。资料显示:红棕色为FeSO3 (墨绿色难溶物)与FeCl3溶液形成的混合色。 则②中红棕色变为浅绿色的原因是
乙同学得出的实验结论是:二氧化硫可还原三氯化铁。
您最近一年使用:0次



