钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。
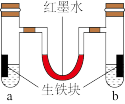
①红墨水柱两边的液面变为左低右高,则_______ (填“a”或“b”)试管内盛有食盐水。
②a试管中铁发生的是_______ (填“析氢”或“吸氧”)腐蚀,生铁中碳上发生的电极反应式为_______ 。
(2)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的_______ 极(填“正”或“负”)相连,把镀层金属铬作_______ 极(填“阳”或“阴”)。电镀铬时,不能用含有CrO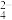 或Cr2O
或Cr2O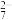 的溶液作电镀液,原因是
的溶液作电镀液,原因是_______ (用电极反应式表明原因)。
(3)利用如图装置,可以模拟铁的电化学保护。
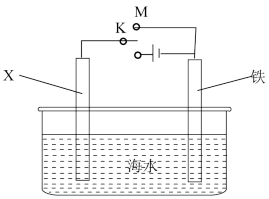
若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为_______ 若X为锌,开关K置于M处,铁棒上发生的电极反应式_______
(1)如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵溶液(显酸性)和食盐水,各加入生铁块,放置一段时间均被腐蚀。

①红墨水柱两边的液面变为左低右高,则
②a试管中铁发生的是
(2)钢铁表面常电镀一层铬(Cr)达到防腐蚀的目的,这是由于铬具有优良的抗腐蚀性能。电镀时,把待镀的金属制品与直流电源的
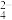 或Cr2O
或Cr2O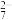 的溶液作电镀液,原因是
的溶液作电镀液,原因是(3)利用如图装置,可以模拟铁的电化学保护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于N处,该电化学保护法称为
更新时间:2022-10-13 17:55:12
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】要在铁制品上镀铜,
(1)阳极材料为________________ ,阴极材料为___________________ 电解质溶液选择_______________________ (用化学式表示)
(2)阴极反应为__________________________ ;阳极反应为_________________ 。
(1)阳极材料为
(2)阴极反应为
您最近一年使用:0次
【推荐2】钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程的有关问题。
(1)下列装置中的铁棒被腐蚀由慢到快的顺序是___________ 。
A.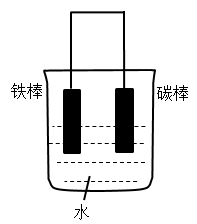 B.
B.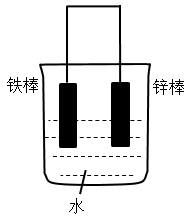
C.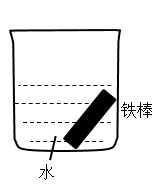 D.
D.
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图:

①B电极的电极反应式是___________ 。
②镀铜铁和镀锌铁在镀层破损后,___________ 更容易被腐蚀。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:
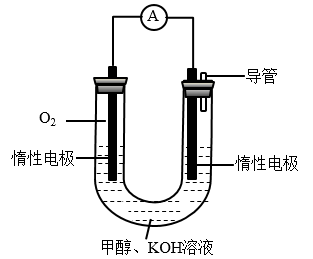
①该电池的能量转化形式为___________ 。
②工作一段时间后, 测得溶液的pH减小。请写出该电池的负极的电极反应式___________ 。
(4)电解液氨(NH3)可以获得H2,写出电解KNH2的液氨溶液(在液氨中KNH2=K++ )时,生成H2的电极反应式
)时,生成H2的电极反应式___________ 。
(1)下列装置中的铁棒被腐蚀由慢到快的顺序是
A.
 B.
B.
C.
 D.
D.
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图:

①B电极的电极反应式是
②镀铜铁和镀锌铁在镀层破损后,
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为
②工作一段时间后, 测得溶液的pH减小。请写出该电池的负极的电极反应式
(4)电解液氨(NH3)可以获得H2,写出电解KNH2的液氨溶液(在液氨中KNH2=K++
 )时,生成H2的电极反应式
)时,生成H2的电极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据所学电化学知识填空。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:
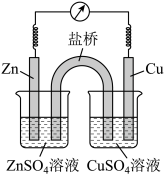
①Zn电极为电池的_______ (填“正极”或“负极”)。
②写出电极反应式:Zn电极_______ ,Cu电极_______ 。
③盐桥中向CuSO4溶液中迁移的离子是_______ (填离子符号)。
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:
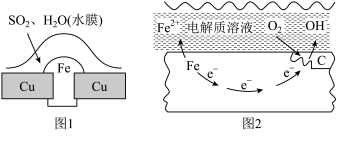
①图1中被腐蚀的金属为_______ (填化学式);图2中金属腐蚀类型属于_______ (填字母)。
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为_______ 。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:

①Zn电极为电池的
②写出电极反应式:Zn电极
③盐桥中向CuSO4溶液中迁移的离子是
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:

①图1中被腐蚀的金属为
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为
您最近一年使用:0次
【推荐2】(1)将下列物质进行分类:①正丁烷与异丁烷、②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)、④金刚石和石墨、⑤冰与水、⑥16O与18O、⑦干冰与二氧化碳,用数字序号回答下列问题:
①互为同素异形体的是___________ ;
②互为同分异构体的是___________ ;
③属于同位素的是___________ ;
④属于同一种化合物的是___________ ;
(2)乙醇(CH3CH2OH)在铜作催化剂时与氧气反应的方程式___________ 。
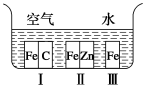
(3)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,如图所示,则铁被腐蚀的速率由慢到快 的顺序是___________ (填序号)。
①互为同素异形体的是
②互为同分异构体的是
③属于同位素的是
④属于同一种化合物的是
(2)乙醇(CH3CH2OH)在铜作催化剂时与氧气反应的方程式
(3)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,如图所示,则铁被腐蚀的速率

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为______________ 。
(2)利用如图装置,可以模拟铁的电化学防护。
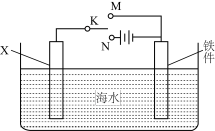
①若X为碳棒,则为减缓铁件的腐蚀,开关K应置于__________ 处。
②若X为锌,开关K置于M处,则该电化学防护法称为______________ 。
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为
(2)利用如图装置,可以模拟铁的电化学防护。

①若X为碳棒,则为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,则该电化学防护法称为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

(1)在相同条件下,三组装置中铁电极腐蚀最快的装置中正极反应式为__ ;
(2)为防止金属Fe被腐蚀,可以采用上述__ (填装置序号)装置原理进行防护;
(3)装置③中总反应的离子方程式为__ 。

(1)在相同条件下,三组装置中铁电极腐蚀最快的装置中正极反应式为
(2)为防止金属Fe被腐蚀,可以采用上述
(3)装置③中总反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是_______ (填装置序号),该装置中正极反应式为_______ ;为防止金属 被腐蚀,可以采用上述
被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中的石墨电极为_______ 极, 电极的电极反应式为
电极的电极反应式为_______ 。
(2)新型固体 隔膜电池广泛应用于电动汽车。电池反应为
隔膜电池广泛应用于电动汽车。电池反应为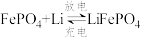 ,电解质为含
,电解质为含 的导电固体,且充、放电时电池内两极间的隔膜只允许
的导电固体,且充、放电时电池内两极间的隔膜只允许 自由通过而导电。该电池放电时
自由通过而导电。该电池放电时 向
向_______ 极移动(填“正”或“负”),负极反应为 ,则正极反应式为
,则正极反应式为_______ 。
(3)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图所示:

①写出该腐蚀过程中的电池反应方程式:_______ 。
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向_______ 。该防护方法名称为_______ 。
③写出修改后石墨电极的电极反应式:_______ 。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

在相同条件下,三组装置中铁电极腐蚀最快的是
 被腐蚀,可以采用上述
被腐蚀,可以采用上述 电极的电极反应式为
电极的电极反应式为(2)新型固体
 隔膜电池广泛应用于电动汽车。电池反应为
隔膜电池广泛应用于电动汽车。电池反应为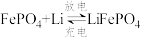 ,电解质为含
,电解质为含 的导电固体,且充、放电时电池内两极间的隔膜只允许
的导电固体,且充、放电时电池内两极间的隔膜只允许 自由通过而导电。该电池放电时
自由通过而导电。该电池放电时 向
向 ,则正极反应式为
,则正极反应式为(3)钢铁生锈现象随处可见,钢铁的电化学腐蚀原理如图所示:

①写出该腐蚀过程中的电池反应方程式:
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向
③写出修改后石墨电极的电极反应式:
您最近一年使用:0次

 四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。
四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。

