根据所学电化学知识填空。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:
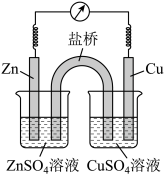
①Zn电极为电池的_______ (填“正极”或“负极”)。
②写出电极反应式:Zn电极_______ ,Cu电极_______ 。
③盐桥中向CuSO4溶液中迁移的离子是_______ (填离子符号)。
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:
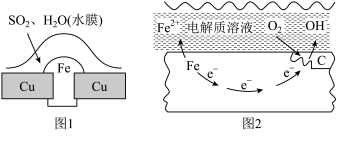
①图1中被腐蚀的金属为_______ (填化学式);图2中金属腐蚀类型属于_______ (填字母)。
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为_______ 。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:

①Zn电极为电池的
②写出电极反应式:Zn电极
③盐桥中向CuSO4溶液中迁移的离子是
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:

①图1中被腐蚀的金属为
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图2中铁的生锈过程中正极反应式为
更新时间:2023-03-13 15:07:24
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】利用原电池原理可以探究金属的活动性。
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片做___ 极(填“正”或“负”),锌片上发生的电极反应式是___ ;银片上发生的电极反应式是__ 。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g。此时产生标准状况下氢气的体积为___ L,通过导线的电子的物质的___ 量为mol。
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是___ 。(填序号)
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片做
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g。此时产生标准状况下氢气的体积为
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| ④将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中。
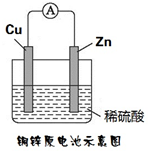
(1)外电路,电子从__________ 极流出。溶液中,阳离子向_______ 极移动。
(2)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为______________ 。
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_____(填序号)。
(4)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是____________(填字母代号)。

(1)外电路,电子从
(2)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为
(3)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_____(填序号)。
| A.无水乙醇 | B.醋酸溶液 | C.CuSO4溶液 | D.苯 |
| A.NaOH+HCl=NaCl+H2O | B.2H2+O2=2H2O |
| C.Fe+2FeCl3=3FeCl2 | D.2H2O=2H2↑+2O2↑ |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】利用人工光合作用合成甲酸的原理为2CO2+2H2O 2HCOOH+O2,装置如图所示。
2HCOOH+O2,装置如图所示。
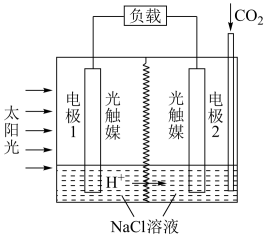
请回答下列问题:
(1)从能量角度分析,该装置将太阳能转化为___________ 。
(2)NaCl溶液的作用是___________ 。
(3)电极1为___________ (填“正极”或“负极”),电极2的电极反应式为___________ 。
(4)产生O2的电极是___________ (填“电极1”或“电极2”),每消耗0.5molCO2时,理论上生成O2体积为___________ (标准状况下)。
 2HCOOH+O2,装置如图所示。
2HCOOH+O2,装置如图所示。
请回答下列问题:
(1)从能量角度分析,该装置将太阳能转化为
(2)NaCl溶液的作用是
(3)电极1为
(4)产生O2的电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某学习小组用如图所示A、B装置分别探究金属锌与稀硫酸的反应,实验过程中A装置烧杯内的溶液温度升高,B装置的电流计指针发生偏转。
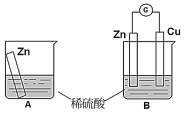
(1)A装置的烧杯中发生反应的离子方程式为_______ 。
(2)Cu板上的现象是_______ ,发生的电极反应是_______ 。
(3)从能量转化的角度看,A、B中反应物的总能量_______  填“大于”“小于”或“等于”
填“大于”“小于”或“等于” 生成物的总能量,A中主要是将化学能转化为
生成物的总能量,A中主要是将化学能转化为_______ ,B中主要是将化学能转化_______ 。
(4)该小组同学反思原电池的原理,其中观点正确的是_______  填字母
填字母 。
。
A.原电池反应的过程中可能没有电子发生转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生

(1)A装置的烧杯中发生反应的离子方程式为
(2)Cu板上的现象是
(3)从能量转化的角度看,A、B中反应物的总能量
 填“大于”“小于”或“等于”
填“大于”“小于”或“等于” 生成物的总能量,A中主要是将化学能转化为
生成物的总能量,A中主要是将化学能转化为(4)该小组同学反思原电池的原理,其中观点正确的是
 填字母
填字母 。
。A.原电池反应的过程中可能没有电子发生转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】依据氧化还原反应:2Ag+ (aq) + Cu(s) == Cu2+ (aq) + 2Ag (s)设计的原电池如下图。

请回答下列问题:
(1)电极X的材料是____________ ;电解质溶液Y是_____________ ;
(2)银电极为电池的_________ 极;银电极上发生的电极反应式______________ 。
(3)外电路中的电子是从________ 电极流向______ 电极(填电极的材料)。

请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子是从
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】I.由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________ 。
(2)装置乙中正极的电极反应式是________________________________________ 。
(3)四种金属活泼性由强到弱的顺序是______________________ 。
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。
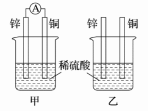
(1)下列叙述正确的是________ 。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是________________________________________________________________________ 。
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应________________________ 。
| 装置 |  | 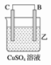 | 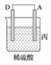 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)四种金属活泼性由强到弱的顺序是
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】为了延长锅炉的使用寿命,常在其内壁焊上锌片。请简要说明这种做法所依据的原理_______________ 。
您最近一年使用:0次
【推荐2】丰富多彩的生活材料:
(1)青奥会将于2014年8月在南京举行。青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念。
①用于青奥村工程的隔热保温材料聚氨酯属于___ (填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是___ (填字母)。
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和___ (填字母)。
a.金刚砂 b.石英 c.水玻璃
(2)生活中处处有化学,化学已渗透到我们的“衣、食、住、行”之中。
①铝合金是生活中常见的材料,具有密度小、强度高的优良性能。其在空气中不易生锈的原因是___ 。
②玻璃和钢铁是常用的建筑材料。普通玻璃是由Na2SiO3、CaSiO3、___ 等物质组成的;钢铁制品不仅可发生化学腐蚀,在潮湿的空气中还能发生___ 腐蚀,生成的铁锈的主要成分是___ (填化学式)。
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机。请写出高纯硅和氮气在1300℃反应制备氮化硅的化学方程式:___ 。
(1)青奥会将于2014年8月在南京举行。青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念。
①用于青奥村工程的隔热保温材料聚氨酯属于
a.有机高分子材料 b.无机非金属材料 c.金属材料
②青奥中心外墙的复合保温材料采用铝合金锁边。有关铝合金的性质正确的是
a.强度小 b.耐腐蚀 c.密度大
③青奥会议中心双塔采用了玻璃幕墙设计。制造玻璃的主要原料为纯碱、石灰石和
a.金刚砂 b.石英 c.水玻璃
(2)生活中处处有化学,化学已渗透到我们的“衣、食、住、行”之中。
①铝合金是生活中常见的材料,具有密度小、强度高的优良性能。其在空气中不易生锈的原因是
②玻璃和钢铁是常用的建筑材料。普通玻璃是由Na2SiO3、CaSiO3、
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机。请写出高纯硅和氮气在1300℃反应制备氮化硅的化学方程式:
您最近一年使用:0次
【推荐3】钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程的有关问题。
(1)下列装置中的铁棒被腐蚀由慢到快的顺序是___________ 。
A.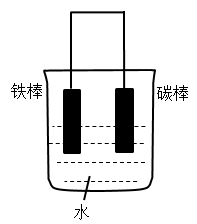 B.
B.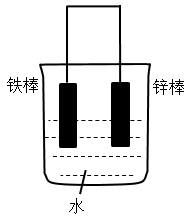
C.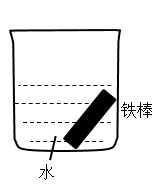 D.
D.
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图:

①B电极的电极反应式是___________ 。
②镀铜铁和镀锌铁在镀层破损后,___________ 更容易被腐蚀。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:
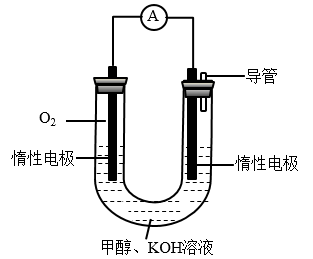
①该电池的能量转化形式为___________ 。
②工作一段时间后, 测得溶液的pH减小。请写出该电池的负极的电极反应式___________ 。
(4)电解液氨(NH3)可以获得H2,写出电解KNH2的液氨溶液(在液氨中KNH2=K++ )时,生成H2的电极反应式
)时,生成H2的电极反应式___________ 。
(1)下列装置中的铁棒被腐蚀由慢到快的顺序是
A.
 B.
B.
C.
 D.
D.
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图:

①B电极的电极反应式是
②镀铜铁和镀锌铁在镀层破损后,
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置:

①该电池的能量转化形式为
②工作一段时间后, 测得溶液的pH减小。请写出该电池的负极的电极反应式
(4)电解液氨(NH3)可以获得H2,写出电解KNH2的液氨溶液(在液氨中KNH2=K++
 )时,生成H2的电极反应式
)时,生成H2的电极反应式
您最近一年使用:0次



