I.由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________ 。
(2)装置乙中正极的电极反应式是________________________________________ 。
(3)四种金属活泼性由强到弱的顺序是______________________ 。
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。
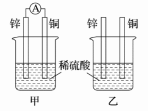
(1)下列叙述正确的是________ 。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是________________________________________________________________________ 。
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应________________________ 。
| 装置 |  | 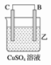 | 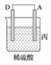 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)四种金属活泼性由强到弱的顺序是
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应
更新时间:2018-07-17 21:03:29
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】已知:2H2+O2 2H2O。
2H2O。
(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量____________________ 。
(2)原电池是直接把化学能转化为电能的装置。
I.航天技术上使用的氢-氧燃料电池具有高能、轻便和不污染环境等优点。下图是氢-氧燃料电池的装置图。则:
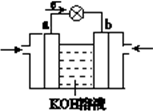
①溶液中OH-移向________ 电极(填“a”或“b”)。
②b电极附近pH_____________ 。(填增大、减小或不变)
③如把H2改为甲烷,则电极反应式为:正极:____________________________ ,负极:________________________________ 。
II.将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积___________________________________ L。(标准状况)
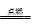 2H2O。
2H2O。(1)该反应1g氢气完全燃烧放出热量121.6kJ,其中断裂1molH-H键吸收436kJ,断裂1molO=O键吸收496kJ,那么形成1molH-O键放出热量
(2)原电池是直接把化学能转化为电能的装置。
I.航天技术上使用的氢-氧燃料电池具有高能、轻便和不污染环境等优点。下图是氢-氧燃料电池的装置图。则:

①溶液中OH-移向
②b电极附近pH
③如把H2改为甲烷,则电极反应式为:正极:
II.将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】将反应2H++Zn=Zn2++H2↑为依据设计一个原电池。
可选:Zn片、Mg片、Al片、石墨棒、稀硫酸、稀硝酸、导线、烧杯、U形管。
(1)画出原电池装置,标明正负极和电极材料,以及电解质溶液,标出电子转移的方向。___________
(2)写出电极反应式,负极:___________ 。正极:___________ 。
(3)H+离子向___________ 极移动,阴离子向___________ 极移动。(填“正”或“负”)
可选:Zn片、Mg片、Al片、石墨棒、稀硫酸、稀硝酸、导线、烧杯、U形管。
(1)画出原电池装置,标明正负极和电极材料,以及电解质溶液,标出电子转移的方向。
(2)写出电极反应式,负极:
(3)H+离子向
您最近一年使用:0次
【推荐1】某课外活动小组的同学在学习了电化学相关知识后,用如图装置进行实验,请回答下列问题:
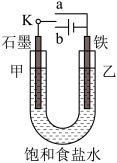
(1)实验一:将开关K与a连接,则乙电极上的反应式为___________________________________ 。
(2)实验一结束后,该研究小组的同学决定在乙电极表面上镀金属锌以防止铁被腐蚀,这种金属保护的原理名称是______________________ 。
(3)实验二:开关K与b连接,则甲为________ 极(填“正”“负”“阳”或“阴”);
(4)对于实验二,下列说法正确的是________ (填字母编号)。
A.溶液中Na+向甲极移动
B.从甲极处逸出的气体能使湿润的淀粉-KI试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
(5)当乙电极产生标准状况下224 mL气体,若剩余溶液体积为200 mL,则电解后所得溶液在常温下的pH为________ 。

(1)实验一:将开关K与a连接,则乙电极上的反应式为
(2)实验一结束后,该研究小组的同学决定在乙电极表面上镀金属锌以防止铁被腐蚀,这种金属保护的原理名称是
(3)实验二:开关K与b连接,则甲为
(4)对于实验二,下列说法正确的是
A.溶液中Na+向甲极移动
B.从甲极处逸出的气体能使湿润的淀粉-KI试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
(5)当乙电极产生标准状况下224 mL气体,若剩余溶液体积为200 mL,则电解后所得溶液在常温下的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以实验结果记录如下:
回答下列(1)、(2)小题:
⑴实验1中Al作的电极为____ (填“正极”或“负极”),Cu作的电极为____ (填“正极"或“负极”)。
⑵实验2观察到C(石墨)棒上产生的现象是____ ,负极的电极反应式为____ .如图是电解质为稀硫酸溶液的氢氧燃料电池。该电池的电子从电极____ 经过导线流向电极____ (填a或b)

| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Al、Cu | 稀盐酸 | 偏向Cu |
| 2 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
回答下列(1)、(2)小题:
⑴实验1中Al作的电极为
⑵实验2观察到C(石墨)棒上产生的现象是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
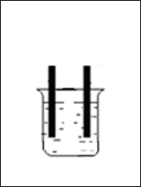
【推荐3】原电池是将化学能转化为电能的装置。如图,烧杯中是稀硫酸溶液
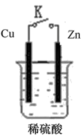
(1)当开关K断开时产生的现象为___________ 。
A.铜片不断溶解B.锌片不断溶解C.铜片上产生气泡D.锌片上产生气泡E.溶液逐渐变蓝
(2)闭合开关K,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为___________ 。
(3)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是___________ (填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D.
溶液 D. 溶液
溶液
(4)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池并画在框中___________ ,该原电池负极的电极材料为___________ ,负极的电极反应式为___________ 。

(1)当开关K断开时产生的现象为
A.铜片不断溶解B.锌片不断溶解C.铜片上产生气泡D.锌片上产生气泡E.溶液逐渐变蓝
(2)闭合开关K,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标况下的体积为
(3)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是
A.蒸馏水 B.NaCl溶液 C.
 溶液 D.
溶液 D. 溶液
溶液(4)FeCl3常用于腐蚀印刷电路铜板(2FeCl3+Cu=2FeCl2+CuCl2)请将此反应设计成原电池并画在框中

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图1是利用电化学装置将 转化为重要的化工原料
转化为重要的化工原料 的原理示意图。
的原理示意图。
(1)该装置将_______ 能转化为_______ 能。
(2)催化剂b表面 发生
发生_______ 反应,其附近溶液酸性_______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
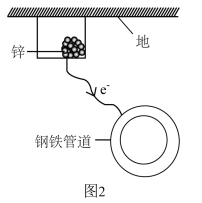
(4)用牺牲金属锌的方法来防止地下钢铁管道的腐蚀(如图2所示),则钢铁管道作_______ 极,负极的电极反应电极方程为_______ 。
 转化为重要的化工原料
转化为重要的化工原料 的原理示意图。
的原理示意图。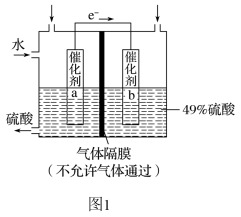
(1)该装置将
(2)催化剂b表面
 发生
发生(3)催化剂a表面的电极反应式:
(4)用牺牲金属锌的方法来防止地下钢铁管道的腐蚀(如图2所示),则钢铁管道作
您最近一年使用:0次
填空题
|
较易
(0.85)
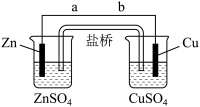
【推荐2】某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu:相对原子质量为64)。
按照实验步骤依次回答下列问题:
(1)导线中电子移动方向为___ (用a、b表示)。
(2)原电池的正极为__ 。
(3)写出装置中铜电极上的电极反应式:___ 。
(4)若装置中铜电极的质量增加32g,则导线中转移的电子数目为__ 。
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向__ (填“左侧”或“右侧”)烧杯移动。

按照实验步骤依次回答下列问题:
(1)导线中电子移动方向为
(2)原电池的正极为
(3)写出装置中铜电极上的电极反应式:
(4)若装置中铜电极的质量增加32g,则导线中转移的电子数目为
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
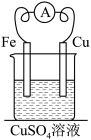
【推荐3】(1)由铜、铁和硫酸铜溶液组成的原电池中,作正极的是________ (填化学式),正极的电极反应式为____________________________ ;电子由______ (填“正”或“负”,下同)极经导线移向______ 极,总反应的离子方程式为_________________________ 。
(2)若以反应 来设计原电池,则电池的负极材料是
来设计原电池,则电池的负极材料是______________ (填化学式,下同),电解质溶液为________________ 溶液。
(2)若以反应
 来设计原电池,则电池的负极材料是
来设计原电池,则电池的负极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如下图所示),在每次实验时记录电压表指针的移动方向和电压表的读数如下表。已知构成两电极的金属,其金属活动性相差越大,电压表的读数越大,请依据表中数据判断:

(1)__________ 金属可能是最强的还原剂,__________ 金属一定不能从CuSO4溶液中置换出铜。
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到蓝色沉淀析出的是__________ (填字母)金属,其对应的原电池的负极反应式是__________ 。

| 金属 | 电子流动方向 | 电压/V |
| A | A→Cu | +0.78 |
| B | Cu→B | -0.15 |
| C | C→Cu | +1.35 |
| D | D→Cu | +0.03 |
(1)
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到蓝色沉淀析出的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图示实验中,把四根洁净的金属条A、B、C、D轮流放置在没有盐溶液的滤纸上面并压紧。在每次轮流实验时,记录了电压表指针的移动方向和电压表的读数(如右表)。
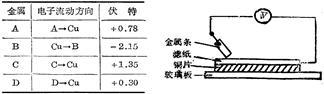
(1)_______________ 金属可能是最强的还原剂;
(2)_______________ 金属不能从硫酸铜溶液中置换铜。

(1)
(2)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】利用原电池原理可以探究金属的活动性。
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片做___ 极(填“正”或“负”),锌片上发生的电极反应式是___ ;银片上发生的电极反应式是__ 。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g。此时产生标准状况下氢气的体积为___ L,通过导线的电子的物质的___ 量为mol。
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是___ 。(填序号)
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片做
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g。此时产生标准状况下氢气的体积为
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| ④将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
您最近一年使用:0次



