回答下列问题:
(1)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是____ 。从废水中回收苯酚的方法:①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③通入某物质又析出苯酚。试写出②、③步反应的化学方程式:②____ ,③____ 。
(2)处理含苯酚的工业废水的流程如图所示。
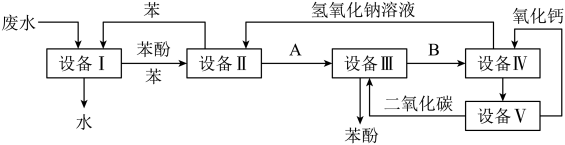
①在设备IV中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和____ 。通过____ (填写操作名称)操作,可以使产物相互分离。
②上面流程中,能循环使用的物质是C6H6、CaO、____ 、____ 。
(3)为测定废水中苯酚的含量,取此废水100mL,向其中滴加溴水至不再产生沉淀为止,得到沉淀0.331g,此废水中苯酚的含量是____ mg•L-1。
(1)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是
(2)处理含苯酚的工业废水的流程如图所示。

①在设备IV中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和
②上面流程中,能循环使用的物质是C6H6、CaO、
(3)为测定废水中苯酚的含量,取此废水100mL,向其中滴加溴水至不再产生沉淀为止,得到沉淀0.331g,此废水中苯酚的含量是
更新时间:2022-10-01 21:27:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学为验证酸性:醋酸>碳酸>苯酚,经仔细考虑,设计如下实验装置,请回答下列问题:

(1)A处的试剂是_______ (填序号,下同),B处的试剂是_______ 。
①醋酸溶液 ②CH3COONa溶液
③苯酚溶液 ④苯酚钠溶液
(2)装置Ⅱ中是_______ 溶液,其作用是_______ 。
(3)能证明三种酸的酸性强弱的现象_______ 。
(4)写出装置III中发生反应的化学方程式_______ 。

(1)A处的试剂是
①醋酸溶液 ②CH3COONa溶液
③苯酚溶液 ④苯酚钠溶液
(2)装置Ⅱ中是
(3)能证明三种酸的酸性强弱的现象
(4)写出装置III中发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】鉴别苯、苯酚溶液、碘化钾溶液、硝酸银溶液、己烯、四氯化碳时,只能用一种试剂,该试剂是______________ ;加入该试剂振荡,静置片刻,各种试样出现的相应现象是:
(1)苯_______________________ 。
(2)苯酚____________________ 。
(3)碘化钾______________________ 。
(4)硝酸银____________________ 。
(5)己烯_______________________ 。
(6)四氯化碳_______________________ 。
(1)苯
(2)苯酚
(3)碘化钾
(4)硝酸银
(5)己烯
(6)四氯化碳
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】G是有机化学重要的中间体,能用于合成多种药物和农药,G的一种合成路线如图:

已知:

 (呈碱性,易被氧化)
(呈碱性,易被氧化)
请回答下列问题:
(1) 除生成B外,还有HCl生成。A的结构简式:
除生成B外,还有HCl生成。A的结构简式:_______ ,用系统命名法命名为_______ 。
(2)C中官能团名称为_______ 。
(3)⑥的反应类型为_______ 。
(4)设置反应①的目的是_______ 。
(5)写出 的化学反应方程式
的化学反应方程式_______ 。
(6)写出同时满足下列条件的F的一种同分异构体的结构简式:_______ (任写一种)。
①能发生水解反应,能与 溶液发生显色反应;②能发生银镜反应;③分子中有5种不同化学环境的氢原子。
溶液发生显色反应;②能发生银镜反应;③分子中有5种不同化学环境的氢原子。
(7)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位:苯环上有羧基时,新引入的取代基连在苯环的间位。根据题中的信息,设计以甲苯为原料合成有机物 的流程图
的流程图_______ (无机试剂任选)。

已知:


 (呈碱性,易被氧化)
(呈碱性,易被氧化)请回答下列问题:
(1)
 除生成B外,还有HCl生成。A的结构简式:
除生成B外,还有HCl生成。A的结构简式:(2)C中官能团名称为
(3)⑥的反应类型为
(4)设置反应①的目的是
(5)写出
 的化学反应方程式
的化学反应方程式(6)写出同时满足下列条件的F的一种同分异构体的结构简式:
①能发生水解反应,能与
 溶液发生显色反应;②能发生银镜反应;③分子中有5种不同化学环境的氢原子。
溶液发生显色反应;②能发生银镜反应;③分子中有5种不同化学环境的氢原子。(7)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻、对位:苯环上有羧基时,新引入的取代基连在苯环的间位。根据题中的信息,设计以甲苯为原料合成有机物
 的流程图
的流程图
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钼酸钠(Na2MoO4)是一种冷却水系统的金属缓蚀剂,工业上通常利用钼精矿(MoS2中硫为-2价)制备金属钼和钼酸钠晶体的流程如图所示。

回答下列问题:
(1)在空气中焙烧时产生对环境有危害气体的化学式是___________ ,焙烧的化学方程式是___________ 。
(2)操作1的实验名称是___________ ,由此可推测MoO3为___________ 性氧化物,该反应的离子方程式为___________ ,进行操作2的步骤是___________ ,过滤、洗涤、干燥。
(3)操作3中硫元素被氧化为最高价,发生反应的离子方程式为___________ 。
(4)钼精矿中MoS2的测定:取钼精矿20g经操作3等,得到Mo的质量为8.64g,假设过程中钼利用率为90%,钼精矿中MoS2的质量分数为___________ 。
(5)电解法制备:用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如图甲所示。b电极上的电极反应式为___________ ,电解槽中使用___________ (填阳离子或阴离子)交换膜。某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图乙所示,要使溶液中钼酸根离子完全沉淀(浓度小于1×10-5mol•l-1),Ba2+的浓度最小为___________ mol•l-1。


回答下列问题:
(1)在空气中焙烧时产生对环境有危害气体的化学式是
(2)操作1的实验名称是
(3)操作3中硫元素被氧化为最高价,发生反应的离子方程式为
(4)钼精矿中MoS2的测定:取钼精矿20g经操作3等,得到Mo的质量为8.64g,假设过程中钼利用率为90%,钼精矿中MoS2的质量分数为
(5)电解法制备:用镍、钼作电极电解浓NaOH溶液制备钼酸钠(Na2MoO4)的装置如图甲所示。b电极上的电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钼酸钠晶体(Na2MoO4·2H2O)可抑制金属腐蚀。以钼精矿(主要成分为MoS2,含少量杂质)为原料,制备钼酸钠晶体的主要流程图如下。
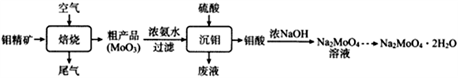
回答下列问题
(1)完成下列反应:_____ MoS2+ _____O2 _____SO2+ _____MoO3
_____SO2+ _____MoO3
在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是__________________ 。
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为____________________________ ;该反应说明MoO3______ (填“有”或“没有”)酸性氧化物的性质。
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则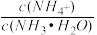 =
=_______ (用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,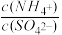 将
将_________ (填“变大”“不变”或“变小”)。
(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为_____________ 。
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是_____________ 。
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是___________ (填选项字母)。
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸

回答下列问题
(1)完成下列反应:
 _____SO2+ _____MoO3
_____SO2+ _____MoO3在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则
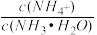 =
=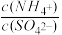 将
将(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为
| 温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 |
| 析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | ||||||
| 溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45. |
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】加碘食盐中含有的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至 开始分解,碘酸钾的溶解度随温度升高变化不大。在酸性条件下硝酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
开始分解,碘酸钾的溶解度随温度升高变化不大。在酸性条件下硝酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
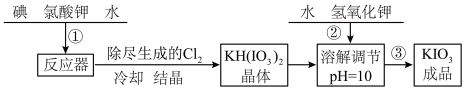
(1)步骤②中氢氧化钾的主要作用是_______
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过_______ 、过滤、洗涤、干燥等步骤
(3)已知: ;
;
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取 食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量
食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量 溶液,使
溶液,使 与
与 反应完全;最后加入指示剂,以物质的量浓度为
反应完全;最后加入指示剂,以物质的量浓度为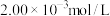 的
的 溶液滴定,消耗
溶液滴定,消耗 时恰好反应完全。
时恰好反应完全。
①在滴定过程中,所用的玻璃仪器为_______ 、_______
②该实验可以用_______ 作指示剂,滴定终点的现象是_______
③下列有关该滴定实验的说法不正确的是_______
A.滴定管在使用前必须检查是否漏水并润洗
B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁
D.终点读数时俯视会导致碘的含量偏低
 开始分解,碘酸钾的溶解度随温度升高变化不大。在酸性条件下硝酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
开始分解,碘酸钾的溶解度随温度升高变化不大。在酸性条件下硝酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:
(1)步骤②中氢氧化钾的主要作用是
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过
温度 | 20 | 40 | 60 | 80 |
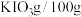 水 水 |  | 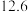 | 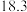 |  |
 ;
;
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取
 食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量
食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量 溶液,使
溶液,使 与
与 反应完全;最后加入指示剂,以物质的量浓度为
反应完全;最后加入指示剂,以物质的量浓度为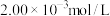 的
的 溶液滴定,消耗
溶液滴定,消耗 时恰好反应完全。
时恰好反应完全。①在滴定过程中,所用的玻璃仪器为
②该实验可以用
③下列有关该滴定实验的说法不正确的是
A.滴定管在使用前必须检查是否漏水并润洗
B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁
D.终点读数时俯视会导致碘的含量偏低
您最近一年使用:0次



