化学电池在通信、交通及日常生活中有着广泛的应用。
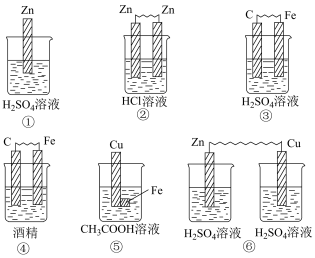
(1)下列装置中能够组成原电池的是_______ (填序号)。
(2)现有如下两个反应:A、 ;B、
;B、 。
。
①根据两反应本质,判断能否设计成原电池。如果不能,说明其原因_______ 。
②如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等_______ 。

(3)如图是某锌锰干电池的基本构造图。
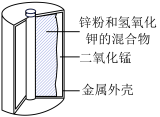
①该碱性锌锰干电池的总反应式为 ,该电池工作时正极的电极反应式是
,该电池工作时正极的电极反应式是_______ 。
②关于该电池的使用和性能,下列说法正确的是_______ 。(填字母,下同)
A.该电池属于蓄电池
B.电池工作时 向负极移动
向负极移动
C.该电池的电解质溶液是 溶液
溶液
D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式 表示不能用水溶液的原因:_______ 。
(1)下列装置中能够组成原电池的是

(2)现有如下两个反应:A、
 ;B、
;B、 。
。①根据两反应本质,判断能否设计成原电池。如果不能,说明其原因
②如果可以,请在下面方框内画出原电池装置图,注明电极材料和电解质溶液等

(3)如图是某锌锰干电池的基本构造图。

①该碱性锌锰干电池的总反应式为
 ,该电池工作时正极的电极反应式是
,该电池工作时正极的电极反应式是②关于该电池的使用和性能,下列说法正确的是
A.该电池属于蓄电池
B.电池工作时
 向负极移动
向负极移动C.该电池的电解质溶液是
 溶液
溶液D.该电池用完后可随意丢弃,不需要回收处理
(4)另一种常用的电池——锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用
21-22高一下·陕西延安·期中 查看更多[2]
(已下线)专题06 化学反应与电能(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)陕西省黄陵中学2021-2022学年高一下学期期中考试化学试题
更新时间:2022-10-08 09:21:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)如下图为某化学兴趣小组探究不同条件下化学能转变为电能的装置。请根据原电池原理回答问题:
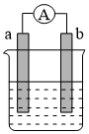
若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时, 向
向___________ 极(填a或b)移动,正极的电极反应式为___________ 。若电极a为Fe、电极b为Ag、电解质溶液为硝酸银,该原电池工作时,原电池的负极材料为___________ ,电子沿导线向___________ (填a或b)移动。
(2)用Cu+2FeCl3 =CuCl2+2FeCl2反应,设计一个原电池。
正极反应式为___________ 负极材料___________ 选用电解液为___________

若电极a为Zn、电极b为Cu、电解质溶液为稀硫酸,该装置工作时,
 向
向(2)用Cu+2FeCl3 =CuCl2+2FeCl2反应,设计一个原电池。
正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】市场出售的“暖贴”中的主要成分是铁粉、炭粉、木屑、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。
(1)请指出炭粉和氯化钠的作用________ 。
(2)请写出“暖贴”中所形成的原电池的电极反应式及电池反应方程式________ ,并分析铁锈产生的原因________ 。
(1)请指出炭粉和氯化钠的作用
(2)请写出“暖贴”中所形成的原电池的电极反应式及电池反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
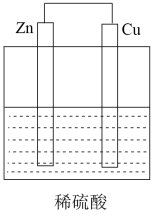
【推荐1】Ⅰ如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是____________ (填序号)。
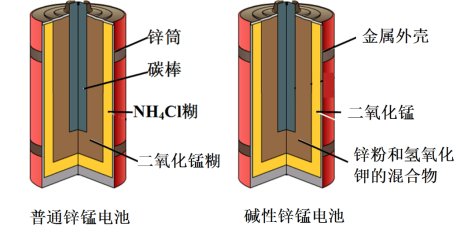
Ⅱ锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列问题:
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是_________ ,电解质的主要成分是__________ ;
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是______________________ 。
(2)下图表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属).
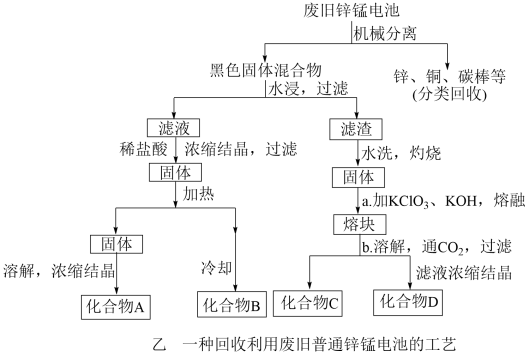
①图(乙)中产物的化学式分别为A________ ,B________ ;
②操作a中得到熔块的主要成分是K2MnO4.操作b中,绿色的K2MnO4溶液反应生成紫色溶液和一种黑色固体,该反应的离子方程式为_____________________________ 。
| 实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③SO42-向Cu极移动 ④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu→Zn ⑥正极反应式:Cu-2e-=Cu2+,发生氧化反应 |

Ⅱ锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列问题:

(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是
(2)下图表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属).

①图(乙)中产物的化学式分别为A
②操作a中得到熔块的主要成分是K2MnO4.操作b中,绿色的K2MnO4溶液反应生成紫色溶液和一种黑色固体,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)如图是锌锰干电池的基本构造图。
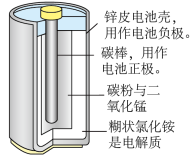
①该干电池工作时负极上的电极反应式是_______________ MnO2的作用是除去正极上的产物H2,本身生成Mn2O3,该反应的化学方程式是______________ 。
②关于该电池的使用和性能,说法正确的是( )
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
D.外电路中每通过0.2mol电子,负极的质量理论上减小6.5g
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 ( )
A .以上反应是可逆反应 B.以上反应不是可逆反应
C. 电池放电时Cd 做负极 D. 电池放电时Cd 做正极
(3)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米的耕地失去使用价值。在酸性土壤中这种污染更为严重这是因为___________ 。
(4)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,一般使用时间可长达十年,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因___________ 。
(1)如图是锌锰干电池的基本构造图。

①该干电池工作时负极上的电极反应式是
②关于该电池的使用和性能,说法正确的是
A.该电池可充电后反复使用
B.该电池可用于闹钟、收音机、照相机等
C.该电池使用后能投入火中,也可投入池塘中
D.外电路中每通过0.2mol电子,负极的质量理论上减小6.5g
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: Cd +2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难于溶水但能溶于酸,以下说法正确的是 A .以上反应是可逆反应 B.以上反应不是可逆反应
C. 电池放电时Cd 做负极 D. 电池放电时Cd 做正极
(3)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米的耕地失去使用价值。在酸性土壤中这种污染更为严重这是因为
(4)另一种常用的电池锂电池由于比容量(单位质量电极材料所能转换的电量)特别大而广泛用于心脏起搏器,一般使用时间可长达十年,它的负极材料用金属锂制成,电解质溶液需用非水溶液配制,请用化学方程式表示不能用水溶液的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100 g水)
回答下列问题:
(1)该电池的正极反应式为________________ ,电池反应的离子方程式____________
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗Zn______ g。(已知F=96500 C/mol)
溶解度/(g/100 g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(1)该电池的正极反应式为
(2)维持电流强度为0.5A,电池工作五分钟,理论消耗Zn
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读短文,回答问题。
锂离子电池是一种生活中常见的二次电池,常用于手机、笔记本电脑、电动车中。它主要依靠Li+在正极材料(LixCOO2)和负极材料(石墨)之间往返嵌入和脱嵌来工作。低温时,由于电解液粘度增大,电池中锂离子的迁移能力下降。低温充电时石墨嵌锂速度降低,Li+来不及嵌入石墨中形成LixC,便得到电子被还原,容易在负极表面析出金属锂,降低电池容量,影响电池安全。上海复旦大学开发了一款新型锂离子电池,其放电的工作原理如图1所示。该电池不仅在-40℃下放电比容量没有衰降,甚至在-70℃下该电池的容量保持率也能够达到常温的70%左右,极大地拓展了电池的应用范围。复旦大学团队采用凝固点低、可在极端低温条件下导电的乙酸乙酯基电解液,并采用不需要将锂离子嵌入到电极中即可完成充、放电的有机物电极,避免了低温条件下嵌入过程变慢。请依据文章内容回答下列问题。

(1)判断下列说法是否正确_________ (填“对”或“错”)。
①新型锂离子电池有望在地球极寒地区使用。
②在传统锂离子电池中,金属锂是负极材料。
③若新型锂离子电池在常温下的放电比容量为99mAh·g-1,则其在-40℃下的放电比容量为99mAh·g-1。
(2)新型锂离子电池放电时,正极是_________ (填“A”或“B”)。
(3)下列关于该新型锂离子电池可耐低温原因的推测中,不正确的是_________ (填字母)。
a.采用与传统不同的有机物电极
b.乙酸乙酯基电解液的凝固点低
c.锂离子不需要在正负极间移动
锂离子电池是一种生活中常见的二次电池,常用于手机、笔记本电脑、电动车中。它主要依靠Li+在正极材料(LixCOO2)和负极材料(石墨)之间往返嵌入和脱嵌来工作。低温时,由于电解液粘度增大,电池中锂离子的迁移能力下降。低温充电时石墨嵌锂速度降低,Li+来不及嵌入石墨中形成LixC,便得到电子被还原,容易在负极表面析出金属锂,降低电池容量,影响电池安全。上海复旦大学开发了一款新型锂离子电池,其放电的工作原理如图1所示。该电池不仅在-40℃下放电比容量没有衰降,甚至在-70℃下该电池的容量保持率也能够达到常温的70%左右,极大地拓展了电池的应用范围。复旦大学团队采用凝固点低、可在极端低温条件下导电的乙酸乙酯基电解液,并采用不需要将锂离子嵌入到电极中即可完成充、放电的有机物电极,避免了低温条件下嵌入过程变慢。请依据文章内容回答下列问题。

(1)判断下列说法是否正确
①新型锂离子电池有望在地球极寒地区使用。
②在传统锂离子电池中,金属锂是负极材料。
③若新型锂离子电池在常温下的放电比容量为99mAh·g-1,则其在-40℃下的放电比容量为99mAh·g-1。
(2)新型锂离子电池放电时,正极是
(3)下列关于该新型锂离子电池可耐低温原因的推测中,不正确的是
a.采用与传统不同的有机物电极
b.乙酸乙酯基电解液的凝固点低
c.锂离子不需要在正负极间移动
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)如图所示装置中,Cu 片是______________ (填“正极”或“负极”)。
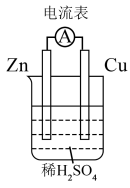
(2)写出负极发生的电极反应式__________ 。
(3)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
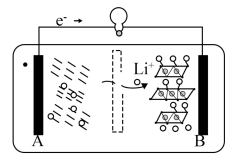
下列说法正确的是_________ (填序号)。
① A 为电池的正极
② 该装置实现了化学能转化为电能
③ 电池工作时,电池内部的锂离子定向移动
(4)在体积为1L的密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应: ,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
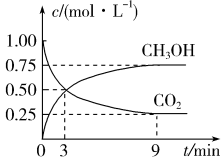
①3~9min内,v(H2)=_______ mol·L—1·min—1。
②能说明上述反应达到平衡状态的是________ (填序号)。
A.容器内CO2、H2、CH3OH、H2O(g)的浓度之比为1∶3∶1∶1
B.v正(CO2)∶v逆(H2)=1∶3
C.单位时间内消耗3mol H2,同时生成1mol CO2
D.混合气体的平均相对分子质量保持不变
③平衡混合气体中甲醇气体的体积分数____________ 。

(2)写出负极发生的电极反应式
(3)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。

下列说法正确的是
① A 为电池的正极
② 该装置实现了化学能转化为电能
③ 电池工作时,电池内部的锂离子定向移动
(4)在体积为1L的密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:
 ,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
①3~9min内,v(H2)=
②能说明上述反应达到平衡状态的是
A.容器内CO2、H2、CH3OH、H2O(g)的浓度之比为1∶3∶1∶1
B.v正(CO2)∶v逆(H2)=1∶3
C.单位时间内消耗3mol H2,同时生成1mol CO2
D.混合气体的平均相对分子质量保持不变
③平衡混合气体中甲醇气体的体积分数
您最近一年使用:0次




