现有以下物质:① NaOH溶液:②液氨:③BaCO3固体:④熔融KHSO4; ⑤Fe(OH)3胶体; ⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖 ;⑩矿泉水。请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明已制得Fe(OH)3胶体的具体操作方法是_______ 。
(3)写出④在水溶液中的电离方程式_______ 。
(4)在①溶液中缓缓通入少量的CO2可生成正盐,写出反应的化学方程式_______ 。
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明已制得Fe(OH)3胶体的具体操作方法是
(3)写出④在水溶液中的电离方程式
(4)在①溶液中缓缓通入少量的CO2可生成正盐,写出反应的化学方程式
更新时间:2022-10-20 16:08:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成以下各题:
I.生活和生产中常利用到胶体的性质,根据胶体的性质,用语言表述完成以下各空。
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁应急止血,其原理是________ 。
(2)明矾能净化水的原因是___________ 。
Ⅱ.根据信息完成相应的离子反应方程式:
(3)用过量氨水吸收工业尾气中的SO2___________ 。
(4)向NH4HCO3溶液中加少量NaOH溶液___________ 。
Ⅲ.根据信息完成相应的氧化还原反应方程式:
(5)Pb与C同主族,铅元素的化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物。已知PbO2具有强氧化性,与浓盐酸共热可生成Cl2和PbCl2。试写出Pb3O4与浓盐酸反应的化学方程式:_____ 。
(6)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4∶1的个数比配料,球磨3~5小时,然后升温至600~750℃,保温24小时,自然冷却到室温得产品,反应过程中生成两种常见气体,其中一种气体能够使澄清石灰石变浑浊,写出该反应的化学方程式:___________ 。
I.生活和生产中常利用到胶体的性质,根据胶体的性质,用语言表述完成以下各空。
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁应急止血,其原理是
(2)明矾能净化水的原因是
Ⅱ.根据信息完成相应的离子反应方程式:
(3)用过量氨水吸收工业尾气中的SO2
(4)向NH4HCO3溶液中加少量NaOH溶液
Ⅲ.根据信息完成相应的氧化还原反应方程式:
(5)Pb与C同主族,铅元素的化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物。已知PbO2具有强氧化性,与浓盐酸共热可生成Cl2和PbCl2。试写出Pb3O4与浓盐酸反应的化学方程式:
(6)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4∶1的个数比配料,球磨3~5小时,然后升温至600~750℃,保温24小时,自然冷却到室温得产品,反应过程中生成两种常见气体,其中一种气体能够使澄清石灰石变浑浊,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
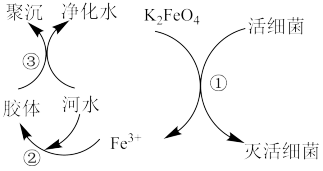
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性,该过程的还原产物是_______ (填离子符号);过程③属于_______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有_______ (填两个)。
(4)制备高铁酸钾常用的反应原理为 (反应未配平)。
(反应未配平)。
①该反应中,Cl元素的化合价由_______ 价变为_______ 价;通过该反应说明:在碱性条件下,氧化性
_______ (填“>”、“=”或“<”) 。
。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ ,将该反应改写为离子方程式:_______ 。
 ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
 (反应未配平)。
(反应未配平)。①该反应中,Cl元素的化合价由

 。
。②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在氯化铁溶液中存在下列平衡:FeCl3+3H2O Fe(OH)3+3HCl;△H>0。回答下列问题:
Fe(OH)3+3HCl;△H>0。回答下列问题:
(1)加热FeCl3溶液,溶液的颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入MgCl2溶液,产生的现象为_______ 。
(2)不断加热FeCl3溶液,蒸干其水分并灼烧得到的固体可能是_______ 。
(3)在配制FeCl3溶液时,为防止浑浊,应加入_______ 。
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是_______ 。
 Fe(OH)3+3HCl;△H>0。回答下列问题:
Fe(OH)3+3HCl;△H>0。回答下列问题:(1)加热FeCl3溶液,溶液的颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入MgCl2溶液,产生的现象为
(2)不断加热FeCl3溶液,蒸干其水分并灼烧得到的固体可能是
(3)在配制FeCl3溶液时,为防止浑浊,应加入
(4)为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入MgCO3固体,过滤后再加入足量盐酸。MgCO3固体能除去Fe3+的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填空:
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是___________ 。属于电解质的是___________ 。属于非电解质的是___________ 。
(2)向 沸水中加入
沸水中加入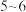 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体,生成胶体的化学方程式为___________ 。
(3)已知:Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
可推知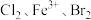 氧化性由强到弱为
氧化性由强到弱为___________ 。若反应Ⅰ中共转移 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为___________ 。
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是
(2)向
 沸水中加入
沸水中加入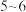 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)已知:Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。可推知
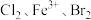 氧化性由强到弱为
氧化性由强到弱为 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列10种物质:①Na②蔗糖固体③盐酸④熔融CaO⑤ 溶液 ⑥
溶液 ⑥ ⑦熔融NaOH⑧氢氧化铁胶体⑨酒精⑩
⑦熔融NaOH⑧氢氧化铁胶体⑨酒精⑩ 固体
固体
(1)能导电且属于电解质的有__________ (填序号)。
(2)写出 在水溶液中电离的方程式
在水溶液中电离的方程式__________ 。
(3)写出 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式__________ 。
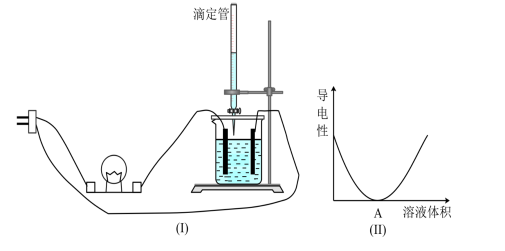
(4)图Ⅰ所示的装置中,烧杯中盛放的是 溶液,当从滴定管中逐渐加入A溶液时,溶液导电性的变化趋势如图2所示。滴加溶液A至图Ⅱ中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质是__________。
溶液,当从滴定管中逐渐加入A溶液时,溶液导电性的变化趋势如图2所示。滴加溶液A至图Ⅱ中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质是__________。
 溶液 ⑥
溶液 ⑥ ⑦熔融NaOH⑧氢氧化铁胶体⑨酒精⑩
⑦熔融NaOH⑧氢氧化铁胶体⑨酒精⑩ 固体
固体(1)能导电且属于电解质的有
(2)写出
 在水溶液中电离的方程式
在水溶液中电离的方程式(3)写出
 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式(4)图Ⅰ所示的装置中,烧杯中盛放的是
 溶液,当从滴定管中逐渐加入A溶液时,溶液导电性的变化趋势如图2所示。滴加溶液A至图Ⅱ中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质是__________。
溶液,当从滴定管中逐渐加入A溶液时,溶液导电性的变化趋势如图2所示。滴加溶液A至图Ⅱ中曲线最低点时,灯泡可能熄灭,溶液A中含有的溶质是__________。
| A.HCl | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列九种物质:①H2②铝 ③Na2O ④CO2⑤H2SO4⑥Ba(OH)2固体⑦氨水⑧稀硝酸 ⑨熔融Al2(SO4)3
(1)上述状态下可导电的是____ ;属于电解质的是____ ;属于非电解质的是____ .
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-═H2O,该离子反应对应的化学方程式为____________ 。
(3)⑨在水中的电离方程式为__________ ,34.2g ⑨溶于水配成250mL溶液,SO 的物质的量浓度为
的物质的量浓度为______________ 。
(1)上述状态下可导电的是
(2)上述九种物质中有两种物质之间可发生离子反应:H++OH-═H2O,该离子反应对应的化学方程式为
(3)⑨在水中的电离方程式为
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.现有下列物质:
①HNO3②冰醋酸③氨水④Al(OH)3⑤NaHCO3(s)⑥Cu⑦氯水⑧CaCO3⑨H2CO3⑩盐酸
(1)上述物质中属于强电解质的有__________ (填序号),属于弱电解质的有__________ (填序号)。
(2)写出下列物质的电离方程式:④__________ ;⑤__________ ;⑨__________ 。
Ⅱ.少量铁粉与100mL0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的__________ (填序号)。
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CH3COONa固体⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol/L盐酸.
①HNO3②冰醋酸③氨水④Al(OH)3⑤NaHCO3(s)⑥Cu⑦氯水⑧CaCO3⑨H2CO3⑩盐酸
(1)上述物质中属于强电解质的有
(2)写出下列物质的电离方程式:④
Ⅱ.少量铁粉与100mL0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O②加NaOH固体③滴入几滴浓盐酸④加CH3COONa固体⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用10mL0.1mol/L盐酸.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下列填空:
(1)硫酸钡的电离方程式_______ 。
(2)盐酸和小苏打反应离子方程式_______ 。
(3)向氢氧化钡溶液中加入硫酸氢钠溶液,至溶液显中性,反应的离子方程式_______ 。
(4)高锰酸钾和浓盐酸的反应为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
①其中还原剂为_______ ,还原产物为_______ 。
②还原剂与氧化剂的数目之比是_______ 。
③写出该反应的离子方程式_______ 。
(1)硫酸钡的电离方程式
(2)盐酸和小苏打反应离子方程式
(3)向氢氧化钡溶液中加入硫酸氢钠溶液,至溶液显中性,反应的离子方程式
(4)高锰酸钾和浓盐酸的反应为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O
①其中还原剂为
②还原剂与氧化剂的数目之比是
③写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】碳酸钠和碳酸氢钠的性质比较
| 名称 | 碳酸钠(Na2CO3) | 碳酸氢钠(NaHCO3) | ||
| 俗名 | ||||
| 主要性质 | 水溶性 | |||
| 稳定性 | ||||
| 主要反应 | 与H+反应 | |||
| 与碱Ca(OH)2反应 | ||||
| 与盐反应 | CaCl2 | |||
| 硫酸铝 | ||||
| 主要用途 | ||||
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在下列的空白处填写最适宜的除杂试剂或方法
①小苏打溶液中含少量苏打___________
②苏打固体中含少量小苏打___________
③Cl2气体中混有少量的HCl气体___________
(2)工业上常用氯气通入石灰乳中制取漂白粉化学方程式___________ ,漂白粉的有效成分为 ___
①小苏打溶液中含少量苏打
②苏打固体中含少量小苏打
③Cl2气体中混有少量的HCl气体
(2)工业上常用氯气通入石灰乳中制取漂白粉化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究钠及其化合物的性质有重要的意义。
(1)汽车安全气囊内装有NaN3、Fe2O3和NaHCO3等物质。
①当汽车发生严重碰撞时,引发NaN3分解:2NaN3=2Na+3N2↑,产生的Na立即与Fe2O3发生反应生成Na2O,写出反应的化学方程式___ 。
②NaHCO3作冷却剂,吸收体系释放的热量。解释原理___ (用化学方程式表示)。
(2)某同学向Na2CO3和NaHCO3的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。

①混合液中n(Na2CO3):n(NaHCO3)=___ 。
②盐酸的物质的量浓度为___ 。
(3)某兴趣小组向2mL0.5molL-1NaHCO3溶液中滴加1mL0.5molL-1CaCl2溶液,产生白色沉淀和气体,该条件下反应的离子方程式为___ 。
(1)汽车安全气囊内装有NaN3、Fe2O3和NaHCO3等物质。
①当汽车发生严重碰撞时,引发NaN3分解:2NaN3=2Na+3N2↑,产生的Na立即与Fe2O3发生反应生成Na2O,写出反应的化学方程式
②NaHCO3作冷却剂,吸收体系释放的热量。解释原理
(2)某同学向Na2CO3和NaHCO3的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。

①混合液中n(Na2CO3):n(NaHCO3)=
②盐酸的物质的量浓度为
(3)某兴趣小组向2mL0.5molL-1NaHCO3溶液中滴加1mL0.5molL-1CaCl2溶液,产生白色沉淀和气体,该条件下反应的离子方程式为
您最近一年使用:0次

 丝 ② 熔融的
丝 ② 熔融的
 溶液 ④蔗糖 ⑤
溶液 ④蔗糖 ⑤  ⑥
⑥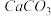 ⑦
⑦ 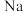 2
2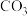 ⑧
⑧ ⑨氨水,请用相应的数字编号和化学用语回答问题:
⑨氨水,请用相应的数字编号和化学用语回答问题:

