按要求填空:
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是___________ 。属于电解质的是___________ 。属于非电解质的是___________ 。
(2)向 沸水中加入
沸水中加入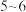 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用___________ 来证明得到的分散系是氢氧化铁胶体,生成胶体的化学方程式为___________ 。
(3)已知:Ⅰ. ;
;
Ⅱ. ;
;
Ⅲ. 。
。
可推知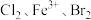 氧化性由强到弱为
氧化性由强到弱为___________ 。若反应Ⅰ中共转移 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为___________ 。
(1)现有下列物质,请用序号填空:
①硫酸钡②固体氢氧化钠③熔融氯化钠④稀盐酸⑤氨水⑥蔗糖⑦二氧化硫
上述状态下可导电的是
(2)向
 沸水中加入
沸水中加入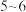 滴饱和
滴饱和 溶液,加热至产生红褐色液体,停止加热,利用
溶液,加热至产生红褐色液体,停止加热,利用(3)已知:Ⅰ.
 ;
;Ⅱ.
 ;
;Ⅲ.
 。
。可推知
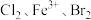 氧化性由强到弱为
氧化性由强到弱为 电子,则消耗标准状况下
电子,则消耗标准状况下 的体积为
的体积为
更新时间:2023-12-03 02:34:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)写出制备氢氧化铁胶体的离子方程式:___________ 。
(2)自来水中的NO 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平。
,产物是N2。发生的反应可表示如下,请完成方程式的配平。___________
___________Al+___________NO +___________OH-→___________AlO
+___________OH-→___________AlO +___________N2↑+___________H2O
+___________N2↑+___________H2O
(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:___________ 。
②反应中氧化剂与还原剂的物质的量之比为:___________ 。
(4)“84”消毒液的包装说明上有如下信息:含37.25%NaClO(次氯酸钠)、1000 mL、密度1.2g/cm3,请回答下列问题:
①上述“84”消毒液的物质的量浓度为___________ mol/L。
②该同学取100 mL上述“84”消毒液,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=___________ mol/L,该消毒液长时间放置在空气中能吸收标准状况下CO2的体积为___________ L。(已知酸性顺序为H2CO3>HClO> HCO )
)
(1)写出制备氢氧化铁胶体的离子方程式:
(2)自来水中的NO
 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平。
,产物是N2。发生的反应可表示如下,请完成方程式的配平。___________Al+___________NO
 +___________OH-→___________AlO
+___________OH-→___________AlO +___________N2↑+___________H2O
+___________N2↑+___________H2O(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:
②反应中氧化剂与还原剂的物质的量之比为:
(4)“84”消毒液的包装说明上有如下信息:含37.25%NaClO(次氯酸钠)、1000 mL、密度1.2g/cm3,请回答下列问题:
①上述“84”消毒液的物质的量浓度为
②该同学取100 mL上述“84”消毒液,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=
 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列关于胶体的有关问题
(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制备Fe(OH)3胶体的化学方程式为:_____ 。
(2)已知 Fe(OH)3胶粒和Al(OH)3胶粒带正电荷,H2SiO3胶粒带负电荷,则:
①Fe(OH)3胶体和H2SiO3胶体混合的现象是_____ 。
②已知Al(OH)3胶体能够净水,则Fe(OH)3胶体_____ (填“能”或“不能”)净水。
(3)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
①“卤水点豆腐,一物降一物”,这里说到的是豆腐的制作,利用的胶体性质是_____ (填字母,下同)。
②工厂采用高压静电除尘,利用的胶体性质是_____ 。
③拍照时,清晨或者大雨过后拍到“耶稣光”的概率比较高_____ 。
(4)是否能用渗析的方法除尽Fe(OH)3胶体中的Cl-?若能。请设计实验证明:若不能,请说明理由。___________ 。
(1)向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制备Fe(OH)3胶体的化学方程式为:
(2)已知 Fe(OH)3胶粒和Al(OH)3胶粒带正电荷,H2SiO3胶粒带负电荷,则:
①Fe(OH)3胶体和H2SiO3胶体混合的现象是
②已知Al(OH)3胶体能够净水,则Fe(OH)3胶体
(3)下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉 B.胶体的电泳 C.丁达尔效应
①“卤水点豆腐,一物降一物”,这里说到的是豆腐的制作,利用的胶体性质是
②工厂采用高压静电除尘,利用的胶体性质是
③拍照时,清晨或者大雨过后拍到“耶稣光”的概率比较高
(4)是否能用渗析的方法除尽Fe(OH)3胶体中的Cl-?若能。请设计实验证明:若不能,请说明理由。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义.请回答下列问题:
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观.
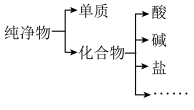
①图中所示所属的分类方法为________________ .
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是________________ (填字母).
A.能和O2反应 B.属于氧化物
C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________ (填字母).
A.甲柜 B.乙柜 C.丙柜 D.丁柜
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、氢氧化钙)”能发生反应.将一定量的稀硫酸逐滴滴入氢氧化钠溶液中,此过程中发生反应的化学方程式为________________ .
(2)含铁元素的物质有很多,在生产、生活中应用广泛.取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的化学方程式为________________ ,另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL上述棕黄色溶液,继续加热至液体呈________ 色,停止加热,证明所得分散系类型的实验方法的名称是________________ ,化学方程式为________________ .
(1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观.

①图中所示所属的分类方法为
②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是
A.能和O2反应 B.属于氧化物
C.碳元素化合价相同 D.属于电解质
③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在
药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
④“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、氢氧化钙)”能发生反应.将一定量的稀硫酸逐滴滴入氢氧化钠溶液中,此过程中发生反应的化学方程式为
(2)含铁元素的物质有很多,在生产、生活中应用广泛.取少量某油漆的原料Fe2O3(红棕色粉末),加入适量浓盐酸,反应后得到棕黄色溶液,取少量棕黄色溶液置于试管中再滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】以下9种物质为中学化学中常见的物质:①Cu②NaHSO4③SO3④H2SO4⑤C2H5OH⑥BaSO4⑦Cu(OH)2⑧NaOH⑨CH3COOH,请按下列分类标准回答问题。
(1)属于电解质的是___ ,属于非电解质的是___ 。(填序号,下同)
(2)能电离出H+的是___ ,属于酸的是___ 。
(3)属于碱的是___ ,其中属于难溶性盐的是___ 。
(4)请写出NaHSO4溶解于水的电离方程式___ 。请写出CH3COOH溶解于水的电离方程式___ 。
(1)属于电解质的是
(2)能电离出H+的是
(3)属于碱的是
(4)请写出NaHSO4溶解于水的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有①铁片 ②CaCO3 ③NH3·H2O ④NH4Cl ⑤酒精 ⑥H2S
其中属于电解质的是(填写序号)___ ,属于非电解质的是___ ,属于强电解质的是___ ,属于弱电解质的是___ 。
写出③和④的电离方程式:___ ,___ 。
写出其中可发生水解的物质的水解离子方程式___ 。
其中属于电解质的是(填写序号)
写出③和④的电离方程式:
写出其中可发生水解的物质的水解离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。现有以下物质:①Cu;②Cl2;③胆矾;④Na3PO4;⑤浓硝酸;⑥CO2;⑦HI溶液;⑧蔗糖;⑨熔融氯化钠。
(1)以上物质中属于混合物的是___________ (填序号);
(2)以上物质中属于电解质的是___________ (填序号);
(3)以上物质中能导电的是___________ (填序号);
(4)写出④在水溶液中的电离方程式___________ ;
(5)实验室制备②与⑥气体时,收集装置均可选用向___________ 排空气法;
(6)①与②反应的实验现象是___________ ,写出该化学反应方程式并用“双线桥”法标出电子转移方向和数目___________ 。
(1)以上物质中属于混合物的是
(2)以上物质中属于电解质的是
(3)以上物质中能导电的是
(4)写出④在水溶液中的电离方程式
(5)实验室制备②与⑥气体时,收集装置均可选用向
(6)①与②反应的实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列9种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤Ba(OH)2,⑥稀盐酸,⑦NaHSO4,⑧碳酸钙,⑨乙醇
(1)上述物质中能导电的是___________ ,属于电解质的有___________ ,属于非电解质的有___________ (填序号)。
(2)⑥和⑧混合,反应的离子方程式为___________ 。
(1)上述物质中能导电的是
(2)⑥和⑧混合,反应的离子方程式为
您最近一年使用:0次
【推荐2】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为_______________________________ 。
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为____________ mol;产生“气泡”的化学方程式为__________________ 。
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是_____________________ (用离子方程式表示)。工业上是将氯气通入30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1 000 kg该溶液需消耗氯气的质量为________ kg(保留整数)。
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(3)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为___ 价,盐酸中加入少量K2FeO4固体,产生黄绿色气体Cl2,K2FeO4被还原成FeCl3,该反应的化学方程式是___ 。
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目___ 。
②此反应中氧化剂与还原剂的质量之比为___ 。
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(1)高铁酸钾K2FeO4是一种新型、高效、多功能绿色水处理剂,且无二次污染。K2FeO4中Fe为
(2)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2。
①用单线桥标出电子转移的方向和数目
②此反应中氧化剂与还原剂的质量之比为
(3)已知常温下在溶液中可发生如下反应:Ce4++Fe2+=Fe3++Ce3+,Sn2++2Fe3+=2Fe2++Sn4+。由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】微型化学实验可以有效实现化学实验绿色化的要求。如下图所示在一块衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KI(含淀粉溶液)、NaOH的酚酞(C20H14O4)试液、FeCl2(含KSCN)溶液各一滴,在圆心处放置一粒芝麻大小的KMnO4的晶体,向KMnO4的晶体上滴加一滴浓盐酸,再立即用表面皿盖好。根据上述描述涉及到的元素,回答问题:
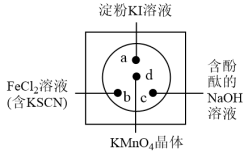
(1)KMnO4中Mn元素的化合价为:_______________ ,Fe在周期表中的位置是:_____________________ 。
(2)第三周期原子半径最小的原子共有______ 种不同能量的电子;长周期主族元素形成化合物的电子式为:__________________ 。
(3)结合已学知识分析a、c处的可能出现的现象:a:_____________________________ ;c:_________________________________ ;b处可能发生反应的离子方程式:___________________________________________________________
(4)已知溶液中,还原性为HSO3−>I-,氧化性为IO3−>I2>SO42−.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示:

①a点处的还原产物是:____________ (填离子符号); b点→c点反应的离子方程式是:_________________________________________
②当溶液中的I-为0.5mol时,加入的KIO3可能是:____________________ mol。

(1)KMnO4中Mn元素的化合价为:
(2)第三周期原子半径最小的原子共有
(3)结合已学知识分析a、c处的可能出现的现象:a:
(4)已知溶液中,还原性为HSO3−>I-,氧化性为IO3−>I2>SO42−.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示:

①a点处的还原产物是:
②当溶液中的I-为0.5mol时,加入的KIO3可能是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列向题:
(1)火药是中国的四大发明之一,黑火药在发生爆炸时,主要发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中还原产物为_______ ,每生成1个K2S,该反应转移_______ 个电子。
(2)近年来我国储氢碳纳米管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法除去,请配平并在答题卡上写出正确的化学方程式:_______
_______C+_______K2Cr2O7+_______ H2SO4→_______CO2↑+_______K2SO4+_______Cr2(SO4)3+_______H2O
氧化剂与还原剂的质量之比为_______ ;若反应中消耗5.88 g重铬酸钾,则生成CO2的质量为_______ 。
(3)按如图所示操作,充分反应后:
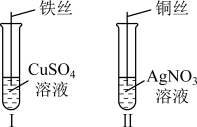
①Ⅱ中铜丝上观察到的现象是_______ 。
②结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_______ 。
(4)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多175个时,被氧化的N原子的个数为_______ 。
(1)火药是中国的四大发明之一,黑火药在发生爆炸时,主要发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中还原产物为
(2)近年来我国储氢碳纳米管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法除去,请配平并在答题卡上写出正确的化学方程式:
_______C+_______K2Cr2O7+_______ H2SO4→_______CO2↑+_______K2SO4+_______Cr2(SO4)3+_______H2O
氧化剂与还原剂的质量之比为
(3)按如图所示操作,充分反应后:

①Ⅱ中铜丝上观察到的现象是
②结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(4)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多175个时,被氧化的N原子的个数为
您最近一年使用:0次

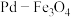 双催化剂,可实现用
双催化剂,可实现用 消除酸性废水中的
消除酸性废水中的 和
和 ,反应历程如图所示。其中
,反应历程如图所示。其中 中
中 和
和 分别用
分别用 (II)、
(II)、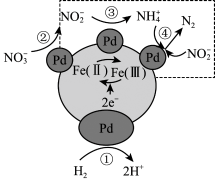

 的过程可描述为
的过程可描述为

