高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠(Na2FeO4)属于____ (“酸”、“碱”、“盐”或“氧化物”),其中铁 化合价为
化合价为____ 价;与O2互为同素异形体的物质的化学式为____ 。
(2)将上述反应的化学方程式改写成离子方程式:____ ,该反应中物质的氧化性大小关系是:____ 。
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴____ 溶液,继续煮沸至溶液呈____ ,停止加热,写出实验室制备Fe(OH)3胶体的化学方程式为____ 。
(4)当生成48gO2时,生成的NaOH的质量为____ g。
(1)高铁酸钠(Na2FeO4)属于
 化合价为
化合价为(2)将上述反应的化学方程式改写成离子方程式:
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
(4)当生成48gO2时,生成的NaOH的质量为
更新时间:2022-10-29 13:43:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】在稀硫酸、NaHCO3、CO2、铜片、铁片、生石灰、食盐和烧碱8种物质中,选择①~⑤为适当的物质,使有连线的两种物质能发生反应。回答下列问题:

(1)推断它们的化学式:①________ ;②_______ ;③______ ;④_______ ;⑤________ 。
(2)写出下列序号之间反应的化学方程式:
③和④:_________ ;
④和⑤:_________ 。
请用单线桥法表示①和②反应中电子的转移情况:___________ 。

(1)推断它们的化学式:①
(2)写出下列序号之间反应的化学方程式:
③和④:
④和⑤:
请用单线桥法表示①和②反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。CrO 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于___ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是___ (填序号)。
A.都不稳定,密封放置会产生沉淀
B.二者均有丁达尔效应
C.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的___________ (填序号)。
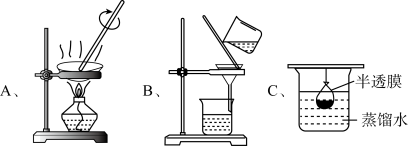
(4)现有10mL明胶的水溶液与5mL K2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO 能够透过半透膜的离子化学方程式:
能够透过半透膜的离子化学方程式:___________
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)明胶的水溶液和K2SO4溶液共同具备的性质是
A.都不稳定,密封放置会产生沉淀
B.二者均有丁达尔效应
C.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

(4)现有10mL明胶的水溶液与5mL K2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO
 能够透过半透膜的离子化学方程式:
能够透过半透膜的离子化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题。
I.现有以下物质:
①NaOH溶液 ②液氨 ③ 固体 ④熔融
固体 ④熔融 ⑤盐酸 ⑥铜 ⑦
⑤盐酸 ⑥铜 ⑦ ⑧
⑧
(1)以上物质中属于非电解质的是___________ (填序号下同),属于强电解质的有___________ ,能导电的物质有___________ 。
(2)写出①和⑧的水溶液反应的离子方程式___________ 。
(3)写出④在水溶液中的电离方程式___________ 。
(4)在含①的溶液中缓缓通少量 ,该过程的离子反应方程式为
,该过程的离子反应方程式为___________ 。
II.写出符合以下离子方程式的化学方程式各一个。
(5)
___________ 。
(6)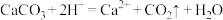
___________ 。
III.“爱化学”实验小组中甲、乙、丙三名同学分别进行 胶体制备实验
胶体制备实验
甲同学:向 稀溶液中加少量NaOH溶液。
稀溶液中加少量NaOH溶液。
乙同学:直接加热饱和 溶液。
溶液。
丙同学:向40mL沸水中逐滴加入5~6滴 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(7)其中操作正确的同学是___________ 。
(8) 胶体制备的化学方程式为
胶体制备的化学方程式为___________ 。
(9)胶体和溶液的本质区别是___________ ;可通过___________ 来区别胶体和溶液。
I.现有以下物质:
①NaOH溶液 ②液氨 ③
 固体 ④熔融
固体 ④熔融 ⑤盐酸 ⑥铜 ⑦
⑤盐酸 ⑥铜 ⑦ ⑧
⑧
(1)以上物质中属于非电解质的是
(2)写出①和⑧的水溶液反应的离子方程式
(3)写出④在水溶液中的电离方程式
(4)在含①的溶液中缓缓通少量
 ,该过程的离子反应方程式为
,该过程的离子反应方程式为II.写出符合以下离子方程式的化学方程式各一个。
(5)

(6)
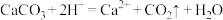
III.“爱化学”实验小组中甲、乙、丙三名同学分别进行
 胶体制备实验
胶体制备实验甲同学:向
 稀溶液中加少量NaOH溶液。
稀溶液中加少量NaOH溶液。乙同学:直接加热饱和
 溶液。
溶液。丙同学:向40mL沸水中逐滴加入5~6滴
 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(7)其中操作正确的同学是
(8)
 胶体制备的化学方程式为
胶体制备的化学方程式为(9)胶体和溶液的本质区别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】由 Ca2+、Ag+、K+、Fe3+、NO 、SO
、SO 、Cl−、CO
、Cl−、CO 这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:
这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈黄色;
②向①的四支试管中分别加入盐酸,A的溶液中有沉淀生成,B的溶液中有无色无味的气体逸出。
回答下列问题:
(1)写出A、C的化学式:A___________ ,C___________ 。
(2)向B的溶液中继续通入CO2,发生反应的离子方程式为___________ 。
(3)与C含有同一种阳离子的氯化物M,配制M的饱和溶液并进行以下实验:
①在烧杯中加入40mL蒸馏水,加热至沸腾后,向沸水中加入制取的饱和M溶液5〜6滴,继续煮沸可得红褐色的液体,该液体中分散质粒子的直径为___________ 。
②向步骤①的烧杯中逐滴加入过量的盐酸,有何现象产生?___________ 。
(4)向D的溶液中通入CO2,能否反应?若能反应请写出化学方程式;若不能,请简要叙述原因___________ 。
 、SO
、SO 、Cl−、CO
、Cl−、CO 这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:
这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈黄色;
②向①的四支试管中分别加入盐酸,A的溶液中有沉淀生成,B的溶液中有无色无味的气体逸出。
回答下列问题:
(1)写出A、C的化学式:A
(2)向B的溶液中继续通入CO2,发生反应的离子方程式为
(3)与C含有同一种阳离子的氯化物M,配制M的饱和溶液并进行以下实验:
①在烧杯中加入40mL蒸馏水,加热至沸腾后,向沸水中加入制取的饱和M溶液5〜6滴,继续煮沸可得红褐色的液体,该液体中分散质粒子的直径为
②向步骤①的烧杯中逐滴加入过量的盐酸,有何现象产生?
(4)向D的溶液中通入CO2,能否反应?若能反应请写出化学方程式;若不能,请简要叙述原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.分类法是进行化学研究的重要方法。不同的标准可以把事物分为不同的类别。现有以下物质:
①固体NaHCO3②Fe③CaCO3④Fe(OH)3胶体⑤熔融的NaHSO4⑥干冰⑦稀盐酸⑧蔗糖
(1)以上物质中属于强电解质的是______ (填序号);
(2)写出①在水溶液中的电离方程式______ ;
(3)④的实验室制备:向沸水中滴加几滴______ 溶液,加热至液体呈红褐色,停止加热。
Ⅱ.空气质量与我们的生活息息相关。SO2是主要的大气污染物之一。
(4)SO2属于______ (填“酸性”或“碱性”)氧化物。
(5)将SO2气体通入蒸馏水中,取部分溶液用pH计测定其pH,每隔10min读数一次,随着时间推移,pH逐渐变小的原因是______ 。(用化学方程式表示)
(6)下列反应中,能用同一离子方程式表示的有______(填序号)。
①固体NaHCO3②Fe③CaCO3④Fe(OH)3胶体⑤熔融的NaHSO4⑥干冰⑦稀盐酸⑧蔗糖
(1)以上物质中属于强电解质的是
(2)写出①在水溶液中的电离方程式
(3)④的实验室制备:向沸水中滴加几滴
Ⅱ.空气质量与我们的生活息息相关。SO2是主要的大气污染物之一。
(4)SO2属于
(5)将SO2气体通入蒸馏水中,取部分溶液用pH计测定其pH,每隔10min读数一次,随着时间推移,pH逐渐变小的原因是
(6)下列反应中,能用同一离子方程式表示的有______(填序号)。
| A.Ca(OH)2和稀CH3COOH | B.NaOH和稀H2SO4 |
| C.Ba(OH)2与稀HNO3 | D.Ba(OH)2与稀H2SO4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为 ,钠在反应中容易
,钠在反应中容易___________ 电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在___________ 里,以隔绝空气。
(3)汽车安全气囊的气体发生剂 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。
ⅰ.当汽车发生较严重的碰撞时,引发 分解
分解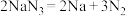 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是___________ 。
ⅱ. 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为___________ 。
ⅲ.一个安全气囊通常装有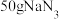 ,其完全分解所释放的
,其完全分解所释放的 为
为___________ mol。
(4)工业通过电解NaCl生产金属钠: ,过程如下:
,过程如下:

已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入 从而把熔点降至约580℃。
从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是___________ 。
②电解时,要避免产生的Na与 接触而重新生成NaCl。NaCl的电离方程式为
接触而重新生成NaCl。NaCl的电离方程式为___________ 。
③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是___________ 。
④过程Ⅰ中, 能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中
能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,用化学方程式解释原因
却不断地被重新生成,用化学方程式解释原因___________ 。
(1)钠的原子结构示意图为
 ,钠在反应中容易
,钠在反应中容易(2)金属钠非常活泼,通常保存在
(3)汽车安全气囊的气体发生剂
 可由金属钠生产。某汽车安全气囊内含
可由金属钠生产。某汽车安全气囊内含 、
、 和
和 等物质。
等物质。ⅰ.当汽车发生较严重的碰撞时,引发
 分解
分解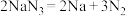 ,从而为气囊充气。产生的Na立即与
,从而为气囊充气。产生的Na立即与 发生置换反应生成
发生置换反应生成 ,化学方程式是
,化学方程式是ⅱ.
 是冷却剂,吸收产气过程释放的热量。
是冷却剂,吸收产气过程释放的热量。 起冷却作用时发生反应的化学方程式为
起冷却作用时发生反应的化学方程式为ⅲ.一个安全气囊通常装有
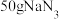 ,其完全分解所释放的
,其完全分解所释放的 为
为(4)工业通过电解NaCl生产金属钠:
 ,过程如下:
,过程如下:
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入
 从而把熔点降至约580℃。
从而把熔点降至约580℃。①把NaCl固体加热至熔融状态,目的是
②电解时,要避免产生的Na与
 接触而重新生成NaCl。NaCl的电离方程式为
接触而重新生成NaCl。NaCl的电离方程式为③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是
④过程Ⅰ中,
 能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中
能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中 却不断地被重新生成,用化学方程式解释原因
却不断地被重新生成,用化学方程式解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上用电解饱和食盐水的方法生产氯气:
(1)若电解饱和食盐水时消耗117gNaCl,则理论上最多可得到氯气(标准状况)多少升___ ?
(2)若将上述氯气和氢气完全反应制成氯化氢,并用水吸收形成200mL盐酸,则所得盐酸的物质的量浓度是多少___ ?
(1)若电解饱和食盐水时消耗117gNaCl,则理论上最多可得到氯气(标准状况)多少升
(2)若将上述氯气和氢气完全反应制成氯化氢,并用水吸收形成200mL盐酸,则所得盐酸的物质的量浓度是多少
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化合价和物质分类是认识物质的性质、实现物质之间转化的两个视角。回答下列问题。
(1)现有下列物质:
A. 溶液 B.
溶液 B. C.
C. 晶体 D.
晶体 D. E.
E. F.
F. 溶液 G.
溶液 G.
①上述物质中属于碱性氧化物的是___________ (填字母)。
② 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
③ 溶于水的电离方程式为
溶于水的电离方程式为___________ 。
④氮氧化物是大气污染物,若要将NO转化为 ,从性质考虑,以上物质
,从性质考虑,以上物质 中可以选择与NO反应的是
中可以选择与NO反应的是___________ (填字母)。
(2)下图是部分含氯物质的“价-类”二维图。

①d表示的物质的化学式为___________ 。
②过程ⅰ、ⅱ、ⅲ的转化中属于氧化还原反应的有过程___________ (填编号)。
③表示b转化为f的离子方程式可以为___________ 。
(1)现有下列物质:
A.
 溶液 B.
溶液 B. C.
C. 晶体 D.
晶体 D. E.
E. F.
F. 溶液 G.
溶液 G.
①上述物质中属于碱性氧化物的是
②
 与
与 反应的离子方程式为
反应的离子方程式为③
 溶于水的电离方程式为
溶于水的电离方程式为④氮氧化物是大气污染物,若要将NO转化为
 ,从性质考虑,以上物质
,从性质考虑,以上物质 中可以选择与NO反应的是
中可以选择与NO反应的是(2)下图是部分含氯物质的“价-类”二维图。

①d表示的物质的化学式为
②过程ⅰ、ⅱ、ⅲ的转化中属于氧化还原反应的有过程
③表示b转化为f的离子方程式可以为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钠是非常重要的一种元素,其化合物在生产、生活中有非常重要的用途。
(1)碳酸钠俗称苏打,又名纯碱,是一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。还广泛用于生活洗涤、酸类中和以及食品加工等。纯碱的生产历史悠久,先后经历了:路布兰制碱法、索尔维制碱法、侯德榜制碱法等历程。其中侯德榜制碱法又称联合制碱法,其关键反应步骤是:依次将___________ 和___________ (都填名称)两种气体通入精制饱和食盐水得到中间产物,该步骤涉及的离子方程式为___________
(2)焦亚硫酸钠( )在医药、橡胶、印染、食品等方面应用广泛。
)在医药、橡胶、印染、食品等方面应用广泛。
①生产 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式___________ 。
② 可用作食品的抗氧化剂。在测定某葡萄酒中
可用作食品的抗氧化剂。在测定某葡萄酒中 残留是时,取
残留是时,取 葡萄酒样品,用
葡萄酒样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 、滴定反应的离子方程式为
、滴定反应的离子方程式为___________ ,该样品中 的残留量为
的残留量为___________  (以
(以 计)
计)
(3)氢化钠是厨房最常见的调味品之一,而亚硝酸钠是一种重要的化工原料,有毒。由于亚硝酸钠外观与氯化钠类似且具有成味,因此偶有发生误食而中毒的事件。业上可以通过用 溶液吸收NO和
溶液吸收NO和 的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成
的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成 亚硝酸钠时理论上转移电子的数目为
亚硝酸钠时理论上转移电子的数目为___________  。
。
(1)碳酸钠俗称苏打,又名纯碱,是一种重要的无机化工原料,主要用于平板玻璃、玻璃制品和陶瓷釉的生产。还广泛用于生活洗涤、酸类中和以及食品加工等。纯碱的生产历史悠久,先后经历了:路布兰制碱法、索尔维制碱法、侯德榜制碱法等历程。其中侯德榜制碱法又称联合制碱法,其关键反应步骤是:依次将
(2)焦亚硫酸钠(
 )在医药、橡胶、印染、食品等方面应用广泛。
)在医药、橡胶、印染、食品等方面应用广泛。①生产
 ,通常是由
,通常是由 过饱和溶液经结晶脱水制得。写出该过程的化学方程式
过饱和溶液经结晶脱水制得。写出该过程的化学方程式②
 可用作食品的抗氧化剂。在测定某葡萄酒中
可用作食品的抗氧化剂。在测定某葡萄酒中 残留是时,取
残留是时,取 葡萄酒样品,用
葡萄酒样品,用 的碘标准液滴定至终点,消耗
的碘标准液滴定至终点,消耗 、滴定反应的离子方程式为
、滴定反应的离子方程式为 的残留量为
的残留量为 (以
(以 计)
计)(3)氢化钠是厨房最常见的调味品之一,而亚硝酸钠是一种重要的化工原料,有毒。由于亚硝酸钠外观与氯化钠类似且具有成味,因此偶有发生误食而中毒的事件。业上可以通过用
 溶液吸收NO和
溶液吸收NO和 的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成
的方法得到亚硝酸钠,已知该反应进行时两种氮氧化物消耗量相等且只生产一种盐,生成 亚硝酸钠时理论上转移电子的数目为
亚硝酸钠时理论上转移电子的数目为 。
。
您最近一年使用:0次

 是纯净物,属于盐类
是纯净物,属于盐类 属于同类物质的是
属于同类物质的是





