下列关于粒子性质的比较中错误的是
| A.分子的稳定性:HF>HCl>HBr>HI | B.离子半径:S2->Cl->Ca2+>Na+ |
| C.沸点:HF>HI>HCl>HBr | D.相同条件下水溶液的酸性:HF>HCl>HBr>HI |
更新时间:2022-10-04 11:40:11
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】一种广泛用于锂离子电池的物质。其结构如图所示。X、Y、Z、W为原子序数依次递增的四种短周期元素,Y、W同主族,原子半径r(X)>r(Y)>r(Z)。下列说法正确的是( )

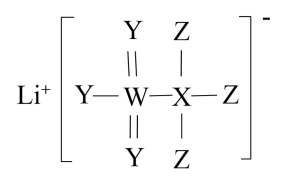

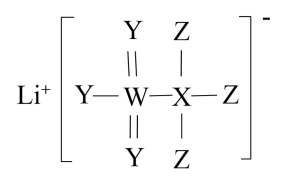
| A.电负性X<Y<Z |
| B.简单氢化物的沸点W>Z>Y>X |
| C.Y、Z、W的单质是相同的晶体类型 |
| D.简单氢化物的热稳定性Y>W>Z |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 |  |  | 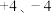 |  | 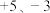 |  |  |  |
原子半径 | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A. 的单质能将 的单质能将 单质从 单质从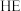 的溶液中置换出来 的溶液中置换出来 |
B.A、H、J的离子半径由大到小顺序是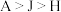 |
C. 元素的单质存在同素异形体 元素的单质存在同素异形体 |
D.I在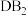 中燃烧生成两种化合物 中燃烧生成两种化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下列实验内容和解释都正确的是
| 编号 | 实验内容 | 解释 |
| A | 常温下,测得0.1  溶液和0.1 溶液和0.1  溶液的pH分别为1.3和1.0 溶液的pH分别为1.3和1.0 | 氮元素的非金属性强于碳元素 |
| B | 向 溶液中加入过量的KI溶液,充分反应后,再滴入几滴KSCN溶液,溶液颜色变红 溶液中加入过量的KI溶液,充分反应后,再滴入几滴KSCN溶液,溶液颜色变红 | KI与的反应为可逆反应 |
| C | 向10mL 0.2 NaOH溶液中滴入2滴0.1 NaOH溶液中滴入2滴0.1  溶液,产生白色沉淀后,再滴加2滴0.1 溶液,产生白色沉淀后,再滴加2滴0.1  溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 在相同温度下的 : :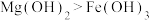 |
| D | 取1mL蔗糖溶液,加入3滴稀 ,水浴加热5min,冷却后加入NaOH溶液调至碱性,再加入少量新制 ,水浴加热5min,冷却后加入NaOH溶液调至碱性,再加入少量新制 悬浊液,加热,有砖红色沉淀产生 悬浊液,加热,有砖红色沉淀产生 | 蔗糖发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】一种广泛用于锂离子电池的物质。其结构如图所示。X、Y、Z、W为原子序数依次递增的四种短周期元素,Y、W同主族,原子半径r(X)>r(Y)>r(Z)。下列说法正确的是( )

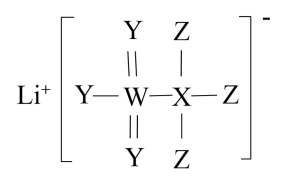

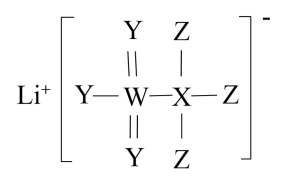
| A.电负性X<Y<Z |
| B.简单氢化物的沸点W>Z>Y>X |
| C.Y、Z、W的单质是相同的晶体类型 |
| D.简单氢化物的热稳定性Y>W>Z |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列有关化学元素周期表的说法正确的是
| A.元素周期表共有18列 |
| B.ⅦA族元素的非金属性自上而下依次减弱 |
| C.主族元素均呈现与其族序数相同的最高化合价 |
| D.第二周期主族元素的原子半径自左向右依次增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】短周期主族元素X、Y、Z、W原子序数依次增大,X与W同主族,且四种元素的最外层电子数之和为18,Z的最外层电子数是其次外层电子数的 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.元素非金属性的顺序为X>Y>W |
| B.Z的单质可以在X的单质中燃烧 |
| C.W的最高价氧化物对应的水化物为强酸 |
| D.简单离子半径X>Y>Z |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】短周期元素X、Y、Z、M原子序数依次增大,它们组成一种团簇分子,结构如图所示。X、M的族序数均等于周期序数,Y原子核外最外层电子数是其电子总数的 。下列说法正确的是
。下列说法正确的是
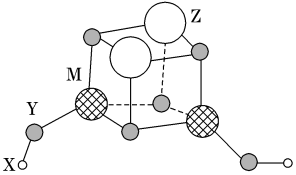
 。下列说法正确的是
。下列说法正确的是
| A.简单离子半径:Y>Z>M |
| B.常温下Z和M的单质均能溶于浓硝酸 |
C.X+与Y 结合形成的化合物是离子晶体 结合形成的化合物是离子晶体 |
| D.Z的最高价氧化物的水化物碱性强于M的最高价氧化物的水化物碱性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列有关性质的比较中正确的是
A.碱性: | B.稳定性: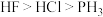 |
C.原子半径: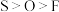 | D.酸性: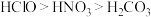 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】杯环芳烃因其结构类似于酒杯而得名,其键线式如图。下列关于杯环芳烃的说法正确的是
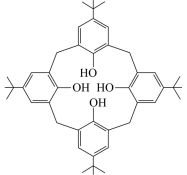

| A.杯环芳烃含有的化学键有极性共价键、非极性共价键和氢键 |
| B.最多与6 mol H2发生加成反应 |
| C.分子式为C44H56O4 |
| D.分子内所有原子一定不在同一平面上 |
您最近一年使用:0次
【推荐2】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。下列有关说法正确的是
| A.F−的半径比O2−的大 |
| B.AsH3的沸点比NH3的高 |
| C.Fe成为阳离子时首先失去4s轨道电子 |
| D.配合物Fe(CO)n可做催化剂,当Fe(CO)n内中心原子价电子数与配体提供电子总数之和为18时,n=5 |
您最近一年使用:0次

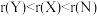
 、
、 、
、 、
、 、
、 和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法不正确的是 价电子排布为
价电子排布为
 键和
键和 键
键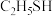 (乙硫醇)>
(乙硫醇)>


